摘要:5.下列反应的离子方程式中正确的是A.甲醇.氧气和氢氧化钾溶液组成的燃料电池的负极反应CH3OH+H2O-6e-= CO2↑+6H+B.在NaHSO4溶液中加Ba(OH)2至中性H++SO42-+Ba2++OH-= BaSO4↓+H2OC.苯酚钠的水溶液中通入少量的CO2 2C6H5O¯+CO2+H2O→2C6H5OH+CO32-D.用侯氏制碱法制得NaHCO3 Na++NH3+CO2+H2O = NaHCO3↓+NH4+[解析]选项A是近年来比较关注的燃料电池方面的问题.该原电池通甲醇的一极是负极.发生氧化反应.失去电子.但是电解质溶液是KOH.所以不能生成H+.所以选项A不正确,在NaHSO4溶液中加Ba(OH)2.也就是说NaHSO4是过量的.所以应该是Ba(OH)2按自己的组成完全反应.即H+和OH-的系数都是2.所以选项B不正确,无论CO2的量是多还是少.在苯酚钠的水溶液中通入CO2.产物都是NaHCO3.所以选项C不正确,侯氏制碱中的NaHCO3是沉淀出来的.所以选项D正确[答案]D.
网址:http://m.1010jiajiao.com/timu_id_58176[举报]
下列反应的离子方程式中正确的是
A.甲醇、氧气和氢氧化钾溶液组成的燃料电池的负极反应
CH3OH+H2O-6e-= CO2↑+6H+
B.在NaHSO4溶液中加Ba(OH)2至中性
H++SO42-+Ba2++OH-= BaSO4↓+H2O
C.苯酚钠的水溶液中通入少量的CO2
2C6H5O¯+CO2+H2O→2C6H5OH+CO32-
D.用侯氏制碱法制得NaHCO3
Na++NH3+CO2+H2O = NaHCO3↓+NH4+
查看习题详情和答案>>下列反应的离子方程式中正确的是
A.甲醇、氧气和氢氧化钾溶液组成的燃料电池的负极反应
CH3OH+H2O-6e-= CO2↑+6H+
B.在NaHSO4溶液中加Ba(OH)2至中性
H++SO42-+Ba2++OH-= BaSO4↓+H2O
C.苯酚钠的水溶液中通入少量的CO2
2C6H5O??+CO2+H2O→2C6H5OH+CO32-
D.用侯氏制碱法制得NaHCO3
Na++NH3+CO2+H2O = NaHCO3↓+NH4+
查看习题详情和答案>>下列反应的离子方程式中正确的是
Na++NH3+CO2+H2O = NaHCO3↓+NH4+
| A.甲醇、氧气和氢氧化钾溶液组成的燃料电池的负极反应 CH3OH+H2O-6e-=CO2↑+6H+ |
| B.在NaHSO4溶液中加Ba(OH)2至中性 H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| C.苯酚钠的水溶液中通入少量的CO2 2C6H5O¯+CO2+H2O→2C6H5OH+CO32- |
| D.用侯氏制碱法制得NaHCO3 |
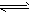 SO32-+H3O+
SO32-+H3O+