摘要:平衡浓度 2x1.0/10 /10 /10平衡常数K
网址:http://m.1010jiajiao.com/timu_id_577072[举报]
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
|
查看习题详情和答案>>
(1)反应3Fe(s)+4H2O(g)═Fe3O4(s)+4H2(g),在一可变的容积的密闭容器中进行,试回答:
①增加Fe的量,其正反应速率的变化是
②将容器的体积缩小一半,其正反应速率
③保持体积不变,充入N2使体系压强增大,其正反应速率
④保持压强不变,充入N2使容器的体积增大,其正反应速率
(2)利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)?CH3OH(g);△H=-90.8kJ?mol-1
②2CH3OH(g)?CH3OCH3(g)+H2O(g);△H=-23.5kJ?mol-1
③CO(g)+H2O(g)?CO2(g)+H2(g);△H=-41.3kJ?mol-1
总反应:3H2(g)+3CO(g)?CH3OCH3(g)+CO2 (g)的△H=
一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是
a.高温高压 b.加入催化剂 c.减少CO2的浓度
d.增加CO的浓度 e.分离出二甲醚
已知反应②2CH3OH(g)?CH3OCH3(g)+H2O(g)某温度下的平衡常数为400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
比较此时正、逆反应速率的大小:v正
查看习题详情和答案>>
①增加Fe的量,其正反应速率的变化是
不变
不变
(填增大、不变、减小,以下相同)②将容器的体积缩小一半,其正反应速率
增大
增大
,逆反应速率增大
增大
.③保持体积不变,充入N2使体系压强增大,其正反应速率
不变
不变
,逆反应速率不变
不变
.④保持压强不变,充入N2使容器的体积增大,其正反应速率
减小
减小
.(2)利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)?CH3OH(g);△H=-90.8kJ?mol-1
②2CH3OH(g)?CH3OCH3(g)+H2O(g);△H=-23.5kJ?mol-1
③CO(g)+H2O(g)?CO2(g)+H2(g);△H=-41.3kJ?mol-1
总反应:3H2(g)+3CO(g)?CH3OCH3(g)+CO2 (g)的△H=
-246.4kJ?mol-1
-246.4kJ?mol-1
;一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是
ce
ce
(填字母代号).a.高温高压 b.加入催化剂 c.减少CO2的浓度
d.增加CO的浓度 e.分离出二甲醚
已知反应②2CH3OH(g)?CH3OCH3(g)+H2O(g)某温度下的平衡常数为400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol?L-1) | 0.44 | 0.6 | 0.6 |
>
>
v逆 (填“>”、“<”或“=”).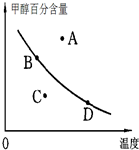 已知某气体反应的平衡常数可表示为K=c(CH3OCH3)c(H2O)/[c(CH3OH)]2,该反应在不同温度下的平衡常数:400℃,K=32;500℃,K=44.
已知某气体反应的平衡常数可表示为K=c(CH3OCH3)c(H2O)/[c(CH3OH)]2,该反应在不同温度下的平衡常数:400℃,K=32;500℃,K=44.请回答下列问题:
(1)写出上述反应的化学方程式
(2)该反应的正反应是
(3)已知在密闭容器中,测得某时刻各组分的浓度如下:
| 物质 | CH3OH(g) | CH3OCH3(g) | H2O(g) |
| 浓度/(mol?L-1) | 0.54 | 0.68 | 0.68 |
②若以甲醇百分含量为纵坐标,以温度为横坐标,此时反应点在图象的位置是图中
(4)一定条件下要提高反应物的转化率,可以采用的措施是
a.升高温度 b.加入催化剂 c.压缩容器的体积
d.增加水蒸气的浓度 e.及时分离出产物.
已知2X2(g)+Y2(g)?2Z(g)△H=-akJ/mol(a>0),在一个容积固定的容器中加入2mol X2和1mol Y2,在5000C时充分反应达平衡后Z的浓度为W mol/L,放出热量bkJ.
(1)若将温度降低到3000C,则反应平衡常数将 (填“增大”“减小”或“不变”).
(2)若原来容器中只加入2mol Z,5000C充分反应达平衡后,吸收热量ckJ,则Z的平衡浓度 W mol/L(填“>”“<”或“=”),a、b、c之间满足关系 (用代数式表示).
(3)能说明反应已达平衡状态的是 (选填字母)
A.浓度c(Z)=2c(Y2) B.容器内压强保持不变
C.v逆(X2)=2v正(Y2) D.容器内密度保持不变
(4)若将上述容器改为恒压容器(反应器开始体积相同),相同温度下起始加入2mol X2和1mol Y2达到平衡后,Y2的转化率将 (填“变大”“变小”或“不变”).
查看习题详情和答案>>
(1)若将温度降低到3000C,则反应平衡常数将
(2)若原来容器中只加入2mol Z,5000C充分反应达平衡后,吸收热量ckJ,则Z的平衡浓度
(3)能说明反应已达平衡状态的是
A.浓度c(Z)=2c(Y2) B.容器内压强保持不变
C.v逆(X2)=2v正(Y2) D.容器内密度保持不变
(4)若将上述容器改为恒压容器(反应器开始体积相同),相同温度下起始加入2mol X2和1mol Y2达到平衡后,Y2的转化率将
| (2013?合肥一模)在一定条件下,将PCl3(g)和Cl2(g)充入体积不变的2L密闭容器中发生下述反应:PCl3(g)+Cl2(g)?PCl5(g) 5min末达到平衡,有关数据如表.
|
查看习题详情和答案>>