网址:http://m.1010jiajiao.com/timu_id_576349[举报]
(一)甲组:
实验方案:镁铝合金![]() 测定剩余固体质量
测定剩余固体质量
实验步骤:
①称量用托盘天平称量
②溶解把①中药品加入烧杯中,用规格为___________mL的量筒量取一定体积1 mol·L-1 NaOH 溶液加入烧杯中,不断搅拌,充分反应
③过滤
④洗涤若未对过滤所得固体进行洗涤,测得铝的质量分数将__________(填“偏高”“偏低”或“不变”),证明固体已洗涤干净的方法为________________________________________。
⑤干燥、称量剩余固体
(二)乙组:
实验方案:

实验装置:

实验步骤:
①按上图连接好装置。
②称取两份质量均为
③通过注射器的针头向装置A左侧管中注入足量的稀盐酸,等不再有气泡产生时,调节装置C的高度,使B和C中的液面相平时记录下此时的体积为448 mL。
④通过另一针头向装置A右侧管中加入足量的稀NaOH溶液,等不再有气泡产生时,调节装置C的高度,使B和C中的液面相平时记录下此时的体积为672 mL。
问题和讨论:
(1)上述实验步骤①和②之间必须加一步________的操作,具体方法为__________________。
(2)为使气体体积测定结果不至于引起很大偏差,除了应注意使B和C中的液面相平外,在反应完全后至读数之前,还需要注意的关键问题是(只需写出一点)_________________。
(3)计算合金中铝的质量分数时,是否需要将气体体积折算为标准状况的体积。
查看习题详情和答案>>为测定镁铝合金(不含其它元素)中铝的质量分数,甲乙两个学习小组设计了下列二种不同的实验方案进行探究。请回答下列问题:
(一)甲组:
实验方案:镁铝合金![]() 测定剩余固体质量
测定剩余固体质量
实验步骤:
①称量 用托盘天平称量2.7g镁铝合金粉末
②溶解 把①中药品加入烧杯中,用规格为 mL的量筒量取一定体积1mol/L NaOH 溶液加入烧杯中,不断搅拌,充分反应
③过滤
④洗涤 若未对过滤所得固体进行洗涤,测得铝的质量分数将 (填“偏高”、“偏低”或“不变” ),证明固体已洗涤干净的方法为
⑤干燥、称量剩余固体
(二)乙组:

实验装置:

实验步骤:
①图连接好装置
②称取两份质量均为0.3g 的镁铝合金样品粉末,分别放入A装置左右两个管中,向B装置中加入一定量的水,把装置A、B的胶塞塞好,然后调节C的高度使B和C中的液面相平,记录下此时的体积为112 mL
③通过注射器的针头向装置A左侧管中注入足量的稀盐酸,等不再有气泡产生时,调节装置C的高度,使B和C中的液面相平时记录下此时的体积为448mL
④通过另一针头向装置A右侧管中加入足量的稀NaOH溶液,等不再有气泡产生时,调节装置C的高度,使B和C中的液面相平时记录下此时的体积为672mL。
问题和讨论:
(1)上述实验步骤①和②之间必须加一步 的操作,具体方法为 。
(2)为使气体体积测定结果不至于引起很大偏差,除了应注意使B和C中的液面相平外,在反应完全后至读数之前,还需要注意的关键问题是(只需写出1点) 。
(3)计算合金中铝的质量分数时,是否需要将气体体积折算为标准状况的体积 。
查看习题详情和答案>>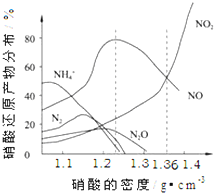 (2011?黄山模拟)如图是各种不同密度的硝酸与铁反应(相同温度)时主要还原产物的分布图.请认真读图分析,回答有关问题.
(2011?黄山模拟)如图是各种不同密度的硝酸与铁反应(相同温度)时主要还原产物的分布图.请认真读图分析,回答有关问题.(1)下列叙述中正确的是(填序号)
A.图中横坐标是硝酸的密度,硝酸的密度越大,其浓度越大
B.当还原剂和温度相同时,不同浓度的硝酸被还原的产物不是单一的,只是在某浓度时,以某种产物为主而已
C.硝酸的浓度越大,还原产物中N元素低化合价产物越多
D.当硝酸密度大于1.3g?cm-3时,还原产物主要为NO、NO2
(2)当硝酸溶液的密度为1.36g?cm-3时,下列化学方程式中,能较准确表达Fe与过量硝酸反应的是(填序号)
A.2Fe+10HNO3═2Fe(NO3)3+NO↑+3NO2↑+5H2O
B.4Fe+18HNO3═4Fe(NO3)3+3NO↑+3NO2↑+9H2O
C.3Fe+12HNO3═2Fe(NO3)3+Fe(NO3)2+2NO↑+2NO2↑+3H2O
(3)密度为1.26g?cm-3,质量分数为50.0%的硝酸,其物质的量浓度是
(4)限用下列仪器、药品验证由铁和过量1.36g?cm-3硝酸反应产生的气体中含有NO(不考虑N2O4).设计一个合理而简单的实验方案(仪器可选择使用,N2的用量可自由控制,加热装置和固定装置省略).
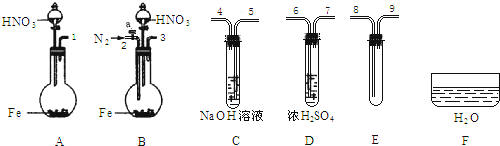
第1步:反应并收集生成的气体:
①实验中气体发生装置应选择
②装置的连接顺序是(填各装置接口的序号):[
③检查装置气密性后,开始反应.待E中充满红棕色气体,停止实验.
第2步:验证E中有NO.
④取下试管E,倒立在F中,轻轻摇动试管,
确认生成的气体中有NO的现象是
火柴是人们常用的生活用品,某兴趣小组为验证日常生活用的火柴头上含有KClO3、MnO2、S等物质,设计了以下系列实验,并回答下列各题。
Ⅰ、火柴头中硫元素的实验证明
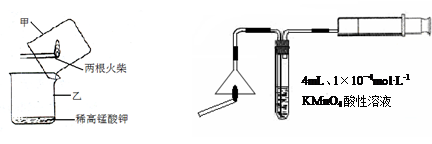
A B
⑴设计装置A中可观察到 的实验现象,即可证明火柴头上含有S元素。
⑵甲同学认为B装置中除了可选用稀高锰酸钾外还可选用:品红溶液、紫色石蕊溶液、滴有酚酞的NaOH溶液、溴水等,经大家分析后淘汰了紫色石蕊溶液和滴有酚酞的NaOH 溶液。你认为淘汰的原因可能是 。甲同学还认为在A装置中选用浓的高锰酸 钾酸性溶液更好,因为浓度越大反应速率越快,你认为对吗? (先判断再说明 原因)。
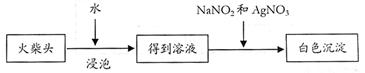
Ⅱ、火柴头中含有Cl元素的证明,设计了以下实验流程图:
⑴为验证火柴头中含有Cl元素的实验步骤是:取滤液C……请回答后续实验步骤 是 。
⑵有学生提出检验火柴头上KClO3另一套实验方案:
|
实验中发生的反应是 KClO3 + 3NaNO2 + AgNO3 = AgCl↓+3NaNO3 + KNO3,其中NaNO2 是 。剂,有人提出上述方法中出现白色沉淀并不能充分说明火柴头上 KClO3的存在,其理由是 。
Ⅲ、测定火柴头中KClO3的含量,设计了以下实验流程图:
⑴步骤②的实验操作装置如下图所示,仪器a的名称为 ,装置B的作用是 。
 则当抽滤完毕或中途停止抽滤时,最佳的正确操作是 。
则当抽滤完毕或中途停止抽滤时,最佳的正确操作是 。
⑵得到的沉淀常用95%的酒精洗涤再抽滤,试问用酒精洗涤的原因 。(3)实验测 得火柴头中KClO3的质量分数为 ;未洗涤沉淀,测得KClO3的质量分数将 (填 “偏大”、“偏小”、或“无影响”,下同)。
查看习题详情和答案>>
火柴是人们常用的生活用品,某兴趣小组为验证日常生活用的火柴头上含有KClO3、MnO2、S等物质,设计了以下系列实验,并回答下列各题。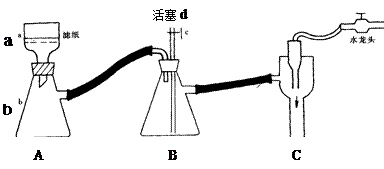
Ⅰ、火柴头中硫元素的实验证明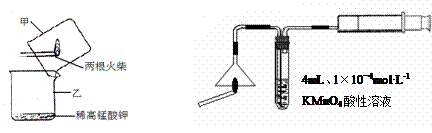
A B
⑴设计装置A中可观察到 的实验现象,即可证明火柴头上含有S元素。
⑵甲同学认为B装置中除了可选用稀高锰酸钾外还可选用:品红溶液、紫色石蕊溶液、滴有酚酞的NaOH溶液、溴水等,经大家分析后淘汰了紫色石蕊溶液和滴有酚酞的NaOH 溶液。你认为淘汰的原因可能是 。甲同学还认为在A装置中选用浓的高锰酸钾酸性溶液更好,因为浓度越大反应速率越快,你认为对吗? (先判断再说明原因)。
Ⅱ、火柴头中含有Cl元素的证明,设计了以下实验流程图: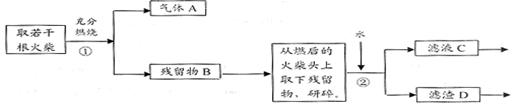
⑴为验证火柴头中含有Cl元素的实验步骤是:取滤液C……请回答后续实验步骤 是 。
⑵有学生提出检验火柴头上KClO3另一套实验方案:
|
|

⑴步骤②的实验操作装置如下图所示,仪器a的名称为 ,装置B的作用是 。
则当抽滤完毕或中途停止抽滤时,最佳的正确操作是 。
⑵得到的沉淀常用95%的酒精洗涤再抽滤,试问用酒精洗涤的原因 。(3)实验测 得火柴头中KClO3的质量分数为 ;未洗涤沉淀,测得KClO3的质量分数将 (填 “偏大”、“偏小”、或“无影响”,下同)。 查看习题详情和答案>>