网址:http://m.1010jiajiao.com/timu_id_5255[举报]
(一)选择题
1.BC2.B3.C.4.C5.C6.C7.B8.C9.BD10.AC11.BD12.D13.B14.C15.D.16.BC17.C18.B19.CD20.CD21.C22.D23.A24.CD25.A26.B27.C28.CD29.B30.A31.C32.(1)D(2)C33.C34.BC35.C36.D37.C38.D39.D40.B、C
(二)非选择题
1.(1)选用AgNO3溶液较好(CuSO4溶液次之,NaCl和H2SO4溶液更次之),①若电解NaCl、H2SO4溶液,产生的气体体积较难测定准确;②同样条件下,通过等量的电量,析出的Ag的质量大于Cu,因而称量和计算时产生的误差前者要小
(2)①电流强度;②电解(通电)时间;③电解产物的质量
(3)NA=
I:电流强度;t:通时间;mAg:析出银的质量MAg:Ag的摩尔质量。
2.(1)BH+2H2O4H2↑+BO―2
(2)pH愈小,反应速率愈大(3)1、16、8、7、4、7
3.DG+CO2M(D)==100D为MCO3,则M(M)=100-60=40M为Ca2+,A为Ca2+盐〔可溶性含氧酸钙盐可能为Ca(NO3)2〕,B为碳酸盐(可溶性碳酸盐有K+、Na+、NH+4……)
从EF+H2O,而F为非金属氧化物,则E含H、O及另一非金属,可推测E为NH4NO3
又:M(F)×+18×M(F)=44,氮的氧化物中N2O相对分子质量为44,和题意相符,可推得A:Ca(NO3)2、B:(NH4)2CO3、D:CaCO3、E:NH4NO3、F:N2O
4.13P4+10P2I4+128H2O32H3PO4+40PH4I
5.5、8、12、10、4、8、12;紫红色溶液褪去;不能用,因为KMnO4与HCl反应,HNO3的氧化性会干扰KMnO4的氧化性。
6.(1)2、5-n、2n、2、5-n、n+3(2)2、+6(3)B、C
7.(1)31.6,36.8,42.1(2)1.58×1024?(3)58.95L/mol(4)42.1g
8.(1)CO;(2)HF;(3)C+H2OCO+H2;(4)2F2+2H2O4HF+O2
9.(1)1cm3中阴、阳离子总数=
1cm3中Ni2+-O2-离子对数=
密度=
(2)设1molNi0.97O中含Ni3+xmol,Ni2+(0.97-x)mol,根据电中性;3xmol+2(0.97-x)mol=2×1mol,x=0.06
Ni2+为(0.97-x)mol=0.91mol
离子数之比Ni3+∶Ni2+=0.06∶0.91=6∶91
10.(1)1∶4;(2)0.12mol;(3)60%
11.(1)1∶50,增大O2量,平衡正向移动,提高SO2转化率(2)保证NH3∶SO2=2∶1(3)3.54t,0.912t.
12.(1)25%(2)2a(3)6(4)n>m
13.(1)BiCl3+H2OBiOCl↓+2HCl(2)不同意,因BiOCl中Cl为-1价而不是+1价。(3)将BiCl3溶解于含适量HCl的蒸馏水中(4)增大溶液中Cl―浓度,抑制BiCl3的水解。
14.(1)NH+Al3++2SO+2Ba2++4OH―2BaSO4↓+Al(OH)3↓+NH3↑+H2O
(2)Al(OH)3+OH―AlO+2H2O
15.(1)HCO+Br2HBrO+Br―+CO2↑
(2)2CO+Br2+H2O2HCO+Br―+BrO―
16.(1)该条件下D的密度ag/L;19.5+11.0-3.00L×ag/L;
(2)盐酸的物质的量浓度bmol/L;当×2≤0.01×b时,盐酸足量:V(H2)=×22.4L
当×2>0.01×b时,盐酸不足:V(H2)=×0.01×b×22.4L。
17.(1)CH3COOHCH3COO―+H+,CH3COO―+H2OCH3COOH+OH―,H2OH++OH―
18.(1)DABF→B→A→C→D→E
(2)2Cl―-2eCl2↑变蓝色Cl2+2I―2Cl―+I2
(3)①③④⑥(4)NA=
19.(1)
(2)N2+O22NO
112
说明氧气过量,过量2体积,根据NO和O2的反应
2NO+O2=2NO
212
说明反应后所得气体NO22体积,O21体积。故密闭容器中气体的体积为3体积。所以
(3)减少,不变。
20.A:NaOHB:NaNO3C:Ba(NO3)2D:HNO3X:MgSO4
(12分)自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO。
(1)在不同温度下,反应N2(g)+O2(g)2NO(g) △H=a kJ·mol-1的平衡常数K如下表:
| 温度/℃ | 1538 | 1760 | 2404 |
| 平衡常数K | 0、86×10-4 | 2、6×10-4 | 64×10-4 |
①该反应的△H 0(填“>”、“=”或“<”)。
②其他条件相同时,在上述三个温度下分别发生该反应。1538℃时,N2的转化率随时间变化如图所示,
请补充完成1760℃时N2的转化率随时间变化的示意图。
(2)科学家一直致力于研究常温、常压下“人工固氮”的新方法。曾有实验报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3。相应的热化学方程式如下:
2N2(g)+6H2O(1) =4NH3(g)+3O2(g) △H=+1530kJ·mol-1
则氨催化氧化反应4NH3(g)+5O2(g)=4NO(g)+6H2O(1) 的反应热△H= 。
(用含a的代数式表示)
(3)最近一些科学家研究采用高质子导电性的SCY陶瓷(能传递H+)实现氮的固定——氨的电解法合成,大大提高了氮气和氢气的转化率。总反应式为:N2+3H22NH3。则在电解法合成氨的过程中,应将H2不断地通入 极(填“正”、“负”、 “阴” 或“阳”);在另一电极通入N2,该电极反应式为 。
(4)合成氨的反应N2(g)+3H2(g)2NH3(g) △H =-92、4 kJ·mol-1,一定条件下的密闭容器中,该反应达到平衡,要提高N2的转化率,可以采取的措施是__________(填字母代号)。
a、升高温度 b、加入催化剂 c、增加H2的浓度
d、增加N2的浓度 e、分离出NH3
(5)在25℃下,将a mol·L-1的氨水与0、01 mol·L-1的盐酸等体积混合,反应后溶液中c(NH4+)=c(Cl-),则溶液显_____________性(填“酸”“碱”或“中”),可推断a 0、01(填大于、等于或小于)。
查看习题详情和答案>>
(12分)自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO。
(1)在不同温度下,反应N2(g)+O2(g) 2NO(g) △H=a kJ·mol-1的平衡常数K如下表:
2NO(g) △H=a kJ·mol-1的平衡常数K如下表:
|
温度/℃ |
1538 |
1760 |
2404 |
|
平衡常数K |
0、86×10-4 |
2、6×10-4 |
64×10-4 |
①该反应的△H 0(填“>”、“=”或“<”)。
②其他条件相同时,在上述三个温度下分别发生该反应。1538℃时,N2的转化率随时间变化如图所示,
请补充完成1760℃时N2的转化率随时间变化的示意图。
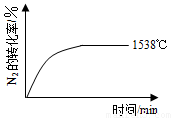
(2)科学家一直致力于研究常温、常压下“人工固氮”的新方法。曾有实验报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3。相应的热化学方程式如下:
2N2(g)+6H2O(1) =4NH3(g)+3O2(g) △H=+1530kJ·mol-1
则氨催化氧化反应4NH3(g)+5O2(g) =4NO(g)+6H2O(1) 的反应热△H= 。
(用含a的代数式表示)
(3)最近一些科学家研究采用高质子导电性的SCY陶瓷(能传递H+)实现氮的固定——氨的电解法合成,大大提高了氮气和氢气的转化率。总反应式为:N2+3H2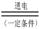 2NH3。则在电解法合成氨的过程中,应将H2不断地通入
极(填“正”、“负”、 “阴” 或“阳”);在另一电极通入N2,该电极反应式为 。
2NH3。则在电解法合成氨的过程中,应将H2不断地通入
极(填“正”、“负”、 “阴” 或“阳”);在另一电极通入N2,该电极反应式为 。
 (4)合成氨的反应N2(g)+3H2(g)
(4)合成氨的反应N2(g)+3H2(g)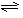 2NH3(g) △H =
-92、4 kJ·mol-1,一定条件下的密闭容器中,该反应达到平衡,要提高N2的转化率,可以采取的措施是__________(填字母代号)。
2NH3(g) △H =
-92、4 kJ·mol-1,一定条件下的密闭容器中,该反应达到平衡,要提高N2的转化率,可以采取的措施是__________(填字母代号)。
a、升高温度 b、加入催化剂 c、增加H2的浓度
d、增加N2的浓度 e、分离出NH3
(5)在25℃下,将a mol·L-1的氨水与0、01 mol·L-1的盐酸等体积混合,反应后溶液中c(NH4+)=c(Cl-),则溶液显_____________性(填“酸”“碱”或“中”), 可推断a 0、01(填大于、等于或小于)。
查看习题详情和答案>>
图1是用一氧化碳还原氧化铁实验装置图的一部分

(1)CO是通过加热草酸晶体制取的,写出相应的方程式______I部分装置可以选用______(填字母)
(2)某实验小组对上述装置进行如下改进(图2),并用改进后的装置测定铁锈样品的组成(铁锈样品中含有Fe2O3?nH2O和Fe两种成份)为得到干燥、纯净的CO气体,洗气瓶A、B中盛放的液态试剂依次可能是______、______(填字母编号).
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液 d.无水氯化钙
(3)写出图3C装置中发生的反应方程式______
(4)实验开始时,在点燃C处酒精灯之前应进行的操作及原因______
(5)E装置的作用是______
(6)准确称量样品的质量10.00g置于硬质玻璃管中,充分反应后冷却、称量(假设每步均完全反应),硬质玻璃管中剩余固体质量为8.32g,D中浓硫酸增重0.72g,则n=______.
查看习题详情和答案>>
(1)在不同温度下,反应
 N2(g
N2(g )+O2(g)
)+O2(g) 2NO(g) △H=a kJ·mol-1的平衡常数K如下表:
2NO(g) △H=a kJ·mol-1的平衡常数K如下表:| 温度/℃ | 1538 | 1760 | 2404 |
| 平衡常数K | 0、86×10-4 | 2、6×10-4 | 64×10-4 |
②其他条件相同时,在上述三个温度下分别发生该反应。1538℃时,N2的转化率随时间变化如图所示,
请补充完成1760℃时N2的转化率随时间变化的示意图。
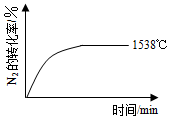
(2)科学家一直致力于研究常温、常压下“人工固氮”的新方法。曾有实验报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3。相应的热化学方
 程式如下:
程式如下:2N2(g)+6H2O(1) =4NH3
 (g)+3O2(g) △H=+1530kJ·mol-1
(g)+3O2(g) △H=+1530kJ·mol-1则氨催化氧化反应4NH3(g)+5O2(g) =4NO(g)+6H2O(1) 的反应热△H= 。
(用含a的代数式表示)
(3)最近一些科学家
 研究采用高质子导电性的SCY陶瓷(能传递H+)实现氮的固定——氨的电解法合成,大大提高了氮气和氢气的转化率。总反应式为:N2+3H2
研究采用高质子导电性的SCY陶瓷(能传递H+)实现氮的固定——氨的电解法合成,大大提高了氮气和氢气的转化率。总反应式为:N2+3H2 2NH3。则在电解法合成氨的过程中,应将H2不断地通入 极(填“正”、“负”、 “阴” 或“阳”);在另一电极通入N2,该电极反应式为 。
2NH3。则在电解法合成氨的过程中,应将H2不断地通入 极(填“正”、“负”、 “阴” 或“阳”);在另一电极通入N2,该电极反应式为 。
 (4)合成氨的反应N2(g)+3H2(g)
(4)合成氨的反应N2(g)+3H2(g) 2NH3(g) △H = -92、4 kJ·mol-1,一定条件下的密闭容器中,该反应达到平衡,要提高N2的转化率,可以采取的措施是__________(填字母代号)。
2NH3(g) △H = -92、4 kJ·mol-1,一定条件下的密闭容器中,该反应达到平衡,要提高N2的转化率,可以采取的措施是__________(填字母代号)。a、升高温度 b、加入催化剂 c、增加H2的浓度
d、增加N2的浓度 e、分离出NH3
 (5)在25℃下,将a mol·L-1的氨水与0、01 mol·L-1的盐酸等体积混合,反应后溶液中c(NH4+)=c(Cl-),则溶液显_____________性(填“酸”“碱”或“中”),可推断a 0、01(填大于、等于或小于)。
(5)在25℃下,将a mol·L-1的氨水与0、01 mol·L-1的盐酸等体积混合,反应后溶液中c(NH4+)=c(Cl-),则溶液显_____________性(填“酸”“碱”或“中”),可推断a 0、01(填大于、等于或小于)。自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO.
(1)在不同温度下,反应N2(g)+O2(g)![]() 2NO(g) ΔH=a kJ·mol-1
2NO(g) ΔH=a kJ·mol-1
![]()
①该反应的ΔH________0
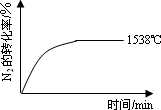
(填“>”、“=”或“<”).②其他条件相同时,在上述三个温度下分别发生该反应.1538℃时,N2的转化率随时间变化如图所示,请补充完成1760℃时N2的转化率随时间变化的示意图.
(2)
科学家一直致力于研究常温、常压下“人工固氮”的新方法.曾有实验报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3.相应的热化学方程式如下:2N2(g)+6H2O(1)=4NH3(g)+3O2(g) ΔH=+1530kJ·mol-1
则氨催化氧化反应4NH3(g)+5O2(g)=4NO(g)+6H2O(1)的反应热ΔH=________.(用含a的代数式表示)
(3)最近一些科学家研究采用高质子导电性的SCY陶瓷(能传递H+)实现氮的固定——氨的电解法合成,大大提高了氮气和氢气的转化率.总反应式为:N2+3H2 2NH3.则在电解法合成氨的过程中,
2NH3.则在电解法合成氨的过程中,
(4)合成氨的反应N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92、4 kJ·mol-1,一定条件下的密闭容器中,该反应达到平衡,要提高N2的转化率,可以采取的措施是________(填字母代号).
2NH3(g) ΔH=-92、4 kJ·mol-1,一定条件下的密闭容器中,该反应达到平衡,要提高N2的转化率,可以采取的措施是________(填字母代号).
a、升高温度
b、加入催化剂
c、增加H2的浓度
d、增加N2的浓度
e、分离出NH3
(5)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应后溶液中c(NH4+)=c(Cl-),则溶液显________性(填“酸”“碱”或“中”),可推断a________0.01(填大于、等于或小于).