网址:http://m.1010jiajiao.com/timu_id_516119[举报]
已知反应:mX(g)+ nY(g) qZ(g) △H<0,m+n>q,在恒容的密闭容器中反应达到平衡时,下列说法正确的是( )
A、通入稀有气体,压强增大,平衡正向移动
B、X的正反应速率是Y的逆反应速率的m/n倍
C、降低温度,混合气体的平均相对分子质量变小
D、增加X的物质的量,Y的转化率降低
【解析】考查外界条件对平衡的影响。该反应是体积减小的放热的可逆反应,若降低温度,则平衡向正反应方向移动,所以混合气体的平均相对分子质量变大,C不正确。通入稀有气体,压强增大,但物质的浓度没有变化,平衡不移动,A不正确。增加X的物质的量,可以增大其他物质的转化率,D也不正确。平衡时正逆反应速率相等,所以根据反应速率之比是相应的化学计量数之比可判断,B是正确的。答案选B。
查看习题详情和答案>>
下列方法能使电离平衡H2OH++OH—向右移动,且使溶液呈酸性的是 ( )
A、向水中加入少量硫酸氢钠固体 B、向水中加入少量硫酸铝固体
C、向水中加入少量碳酸钠固体 D、将水加热到100℃,使水的PH=6
【解析】考查外界条件对平衡的影响。由于水既能电离出氢离子,又能电离出OH-,所以不论是酸还是碱均能抑制水的电离,A不正确。盐类的水解可以促进水的电离,B中水解显酸性,C中水解显碱性,B正确,C错误。温度升高可以促进水的电离,但纯水在任何温度下都是显中性的。答案选B。
查看习题详情和答案>>
盐酸与块状CaCO3反应时,不能使反应的最初速率明显加快的是( )
A.将盐酸的用量增加一倍 B.盐酸的浓度增加一倍,用量减半
C.温度升高30 ℃ D.改用更小块的CaCO3
【解析】考查外界条件对反应速率的影响。A中变化的是物质的量,但浓度并没有变化,不能加快反应速率。B是通过增大盐酸的浓度来加快反应速率的,C是通过升高温度来加快反应速率的,D是通过增大固体的表面积来加快反应速率的,所以答案是A。
查看习题详情和答案>>
下列方法能使电离平衡H2O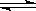 H++OH—向右移动,且使溶液呈酸性的是 ( )
H++OH—向右移动,且使溶液呈酸性的是 ( )
A、向水中加入少量硫酸氢钠固体 B、向水中加入少量硫酸铝固体
C、向水中加入少量碳酸钠固体 D、将水加热到100℃,使水的PH=6
【解析】考查外界条件对平衡的影响。由于水既能电离出氢离子,又能电离出OH-,所以不论是酸还是碱均能抑制水的电离,A不正确。盐类的水解可以促进水的电离,B中水解显酸性,C中水解显碱性,B正确,C错误。温度升高可以促进水的电离,但纯水在任何温度下都是显中性的。答案选B。
查看习题详情和答案>>
已知反应:mX(g)
+ nY(g)  qZ(g) △H<0,m+n>q,在恒容的密闭容器中反应达到平衡时,下列说法正确的是
( )
qZ(g) △H<0,m+n>q,在恒容的密闭容器中反应达到平衡时,下列说法正确的是
( )
A、通入稀有气体,压强增大,平衡正向移动
B、X的正反应速率是Y的逆反应速率的m/n倍
C、降低温度,混合气体的平均相对分子质量变小
D、增加X的物质的量,Y的转化率降低
【解析】考查外界条件对平衡的影响。该反应是体积减小的放热的可逆反应,若降低温度,则平衡向正反应方向移动,所以混合气体的平均相对分子质量变大,C不正确。通入稀有气体,压强增大,但物质的浓度没有变化,平衡不移动,A不正确。增加X的物质的量,可以增大其他物质的转化率,D也不正确。平衡时正逆反应速率相等,所以根据反应速率之比是相应的化学计量数之比可判断,B是正确的。答案选B。
查看习题详情和答案>>