网址:http://m.1010jiajiao.com/timu_id_499149[举报]
1.B 2.B 3.B 4.B 5.A 6.BD 7.A 8.A 9.AD 10.A 11.AD
12.CD 13.C 14.A 15.B 16.D 17.D 18.C 19.A 20.B 21.A 22.B
23.(1)E、 、
、 (2)D、
(2)D、 、
、 (3)A、
(3)A、 、
、 (4)D、
(4)D、 、
、 .
.
24.①
②
③
④
25.(1)磺酸基 H亦有较强的酸性
H亦有较强的酸性 w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
(2)A  (3)
(3)

26.(1) (2)
(2) (3)②⑤
(3)②⑤
(4)
n 

(2)①

②

(2)①②③④
29.


(2)可以,因为该反应的总反应式为 ,原子利用率=34/34×100%=100%,故可称为理想状态
,原子利用率=34/34×100%=100%,故可称为理想状态
30.(1)A、D (2)除去过量的硫粉 (3)
(4) 生成
生成 :
: ,∴ 未饱和
,∴ 未饱和
(5)B (6)设析出的晶体质量为x(g)
30×1.14-18.9=15.3(g) 
∴ x=23.1(g) www.ks5u.com
www.ks5u.com
.化学上鉴定S2O32-的方法之一是使用AgN03溶液作试剂,将AgN03溶液逐渐滴入含 S2O32-的溶液中,会发生以下反应:
![]()
![]()
对于S2O32-的鉴定,下列叙述不正确的是
![]() A.该鉴定可在酸性溶液中进行 B.该鉴定只能在中性溶液中进行
A.该鉴定可在酸性溶液中进行 B.该鉴定只能在中性溶液中进行
![]() C. AgN03必须过量 D. S2-对鉴定有干扰
C. AgN03必须过量 D. S2-对鉴定有干扰
化学上鉴定S2O32-的方法之一是使用AgNO3溶液作试剂,将AgNO3溶液逐滴滴入含有S2O32-的溶液中,会有以下反应发生:
①Ag++2S2O32-![]() [Ag(S2O3)2]3-
[Ag(S2O3)2]3-
②3Ag++[Ag(S2O3)]3-![]() 2Ag2S2O3↓(白)
2Ag2S2O3↓(白)
③Ag2S2O3+H2O![]() Ag2S(黑)↓+H2SO4
Ag2S(黑)↓+H2SO4
其中第②步到第三步反应的速率是很快的.对于S2O32-的鉴定,下列叙述不正确的是
[ ]
A.用此法鉴定时,在加AgNO3溶液之前应先将溶液酸化
B.该鉴定在酸性或碱性太强的环境中均不适宜
C.所加AgNO3溶液不能太少
D.S2-对该鉴定有干扰
查看习题详情和答案>>|
化学上鉴定S2O32-的方法之一是使用AgNO3溶液作试剂,将溶液逐渐滴入含有S2O32-的溶液中时,会有以下反应: Ag++2S2O32- Ag2S2O3+H2O | |
| [ ] | |
A. |
该鉴定可在酸性或碱性溶液中进行 |
B. |
该鉴定只能在中性溶液中进行 |
C. |
AgNO3必须过量 |
D. |
S2-对鉴定有干扰 |
(1)鉴别Fe(OH)3胶体和FeCl3溶液的方法是
(2)电子工业用FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:
(3)某研究性学习小组为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:
①取少量待测溶液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子是
③验证该溶液中含有Fe2+,正确的实验方法是
A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.取适量溶液,滴入氯水,再滴入KSCN溶液,若显血红色,证明原溶液中含有Fe2+
(4)工程师欲从制造印刷电路板的废水中回收铜,并获得FeCl3溶液,设计如图方案:

①滤渣C的化学式为
②加过量D发生反应的离子方程式为
③通入F发生反应的化学方程式为
铁是人类较早使用的金属之一。运用所学知识,回答下列问题。
(1)鉴别Fe(OH)3胶体和FeCl3溶液的方法是 。
(2)电子工业用FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式: 。
(3)某研究性学习小组为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:
①取少量待测溶液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子是 ;②溶液组成的测定:取50.0mL待测溶液,加入足量的AgNO3溶液,得21.525g白色沉淀。则溶液中c(Cl-)= mol·L-1。
③验证该溶液中含有Fe2+,正确的实验方法是 。
A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.取适量溶液,滴入氯水,再滴入KSCN溶液,若显血红色,证明原溶液中含有Fe2+
(4)工程师欲从制造印刷电路板的废水中回收铜,并获得FeCl3溶液,设计如下方案: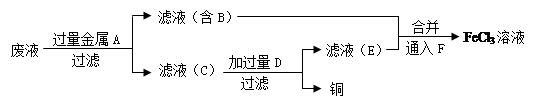
①滤渣C的化学式为 。
②加过量D发生反应的离子方程式为 。
③通入F发生反应的化学方程式为 。



