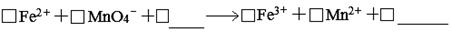摘要:(1)某温度下.SO3(g) SO2(g)+1/2O2(g),△H= +98 kJ?mol-1.开始时在100L的密闭容器中加入4.0mol SO2(g)和10.0molO2(g).当反应达到平衡时共放出热量196 kJ.该温度下平衡常数K=
网址:http://m.1010jiajiao.com/timu_id_495427[举报]
题号
1
2
3
4
5
6
7
8
9
10
11
12
13
14
答案
B
D
A
A
C
D
B
D
B
B
AC
AD
BC
C
15.(10分,每空2分)
(1)过滤(洗涤) ; 蒸发浓缩、冷却结晶,过滤
(2)连接好装置,从漏斗向量气筒内注入一定量的水,移动漏斗使左、右两侧形成液面高度差。静置后,液面高度不再变化,即表明气密性良好。(其他合理方法均给分)
16.(8分)(1)Al
(2)1.204×1024(或2NA)(2分)
(3)4NH3+5O2 4NO+6H2O(2分)
4NO+6H2O(2分)
(4)AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-(2分);
 17.(10分,每空2分) (1)HC2O4-+ OH―= C2O42-+ H2O (2)>
17.(10分,每空2分) (1)HC2O4-+ OH―= C2O42-+ H2O (2)>
(3)H2C2O4 CO↑+CO2↑+H2O
(4)温度过低反应速率缓慢;温度过高时,H2C2O4在酸性溶液中会部分分解。(每个点1分 共2分)
(5)C
18.(10分)(1)保护臭氧层(1分)
(3)A(2分)
②CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH=-49.47kJ•mol-1(2分)
CH3OH(g)+H2O(g) ΔH=-49.47kJ•mol-1(2分)

 (5)B或D(B、D都选给分)(1分)
(5)B或D(B、D都选给分)(1分)
19.(12分,每空2分)
 (1)反应①:加成反应;反应④:取代反应(2) A:CH3CCN; G:
(1)反应①:加成反应;反应④:取代反应(2) A:CH3CCN; G:
(3)B→C;CH3CCOOH CH2=CCOOH+H2O
 |
 |
||||
 |
|||||

 (3)移动漏斗保持左、右两侧液面相平
(4)
(3)移动漏斗保持左、右两侧液面相平
(4)



 2SO3(g);ΔH=-Q kJ/mol(Q>0)。下列说法正确的是
2SO3(g);ΔH=-Q kJ/mol(Q>0)。下列说法正确的是  2SO3(g),(正反应是放热反应),达到平衡后,其它条件不变时,只改变下列的某一个条件,将变化的情况(增大、减小、不变)填入空格中。
2SO3(g),(正反应是放热反应),达到平衡后,其它条件不变时,只改变下列的某一个条件,将变化的情况(增大、减小、不变)填入空格中。
 2SO3(g),该反应在体积不变的密闭容器中进行,则下列 (填序号)可作为反应达到平衡的判断依据。
2SO3(g),该反应在体积不变的密闭容器中进行,则下列 (填序号)可作为反应达到平衡的判断依据。