网址:http://m.1010jiajiao.com/timu_id_469908[举报]
6.B 7.B 8.A 9.D 10.B 11.C 12.B 13.B
26.(1)C , B (2分)
(2)5 , 在右边加入0.8agNaCl晶体 (3分)
(3)B , C 2Fe3++SO2+2H2O=2Fe2++SO42―+4H+ (4分)
(4)C , C C(Na+)>C(CO32-)>C(OH―)>C(HCO3―) >C(H+) (4分)
 27.(1)Cu(NO3)2 ,CO2 , CH3OH
(6分)
27.(1)Cu(NO3)2 ,CO2 , CH3OH
(6分)

(2) (2分)
(3)pH=2 (2分)
(4)3Cu2O+2NO3-+14H+ =6Cu2++2H2O+2 NO↑ (2分)
HCHO+4Cu(OH)2 2Cu2O↓+CO2↑+5H2O (2分)
28.(1)g j 、 c 、n、 p (5分)
避免H2O蒸汽与C反应生成H2对CO的还原性验证产生干扰 (2分)
(2)打开A中的活塞产生CO2排除装置中的O2 (2分)
(3)2C+CO2 2CO (2分)
(4)E反应管内黑色固体变为红色 (2分)
(5)点燃(或者用气球收集) (2分)
(6)D、E q 干燥管(或者U形管) (3分)
 |
29.(1)CH3CHO C(CH2OH)4 (6分)
(2)酯化反应(或者取代反应) 加成反应(或者还原反应) (4分)
(3)CH3CHO+3HCHO
 (HOCH2)3CCHO
(2分)
(HOCH2)3CCHO
(2分)
物理参考答案:
一、选择题:全部选对的给6分,选对但不全的给3分,有选错的给0分。
题号
14
15
16
17
18
19
20
21
答案
A
AC
B
C
B
C
AD
D
22、(18分)
(Ⅰ)(6分)
① A (3分)
 ② 漏斗重心变化导致单摆有效摆长变化,从而改变单摆周期,影响加速度的测量值
(3分)
② 漏斗重心变化导致单摆有效摆长变化,从而改变单摆周期,影响加速度的测量值
(3分)
(Ⅱ)(12分)
① G1 G2 (4分)
② 55.8 KΩ (4分)
③ 如图 (安培表外接也可以) (4分)
23、(14分)解:(1)A在斜面上运动的加速度为 a1=gsinθ (2分)
设到达底部的时间为t1,速度为v1,则v1= gsinθ?t1 (2分)
(2)设A在水平面上运动时间为t2 ,A恰好追上B的条件为位移和速度满足:
v1 = a(t1+ t2) (2分)
24、(18分)
解:(1)小物块落到圆弧上的B点,B、A两点关于O点上下对称,则AB=R,
方向竖直向下 1分
(2)小物块到达B点后沿切线方向的分速度
小物块从B点滑到C点,机械能守恒,取圆弧最低点C为重力势能零点,
小物块在长木板上滑行,系统动量守恒,设小物块刚滑到木板右端时共同速度为v
则 mvC=(M+m)v ⑥ 2分
滑动摩擦力对系统做功,对系统用动能定律
解得: s=2.5m ⑨ 2分
25.解:(1)粒子在电场中加速,根据动能定律得: (3分)
(3分)
(2)粒子进入磁场后,受洛伦兹力做匀速圆周运动,
要使粒子不能到达大圆周,其最大的圆半径为轨迹圆与大圆周相切,如图,
则粒子在磁场中转过φ=270°,然后沿半径进入电场减速到达金属球表面,再经电场加速原路返回磁场,如此重复,恰好经过4个回旋后,沿与原出射方向相反的方向回到原出发点。 (2分)
①B能使湿润的红色石蕊试纸变蓝,D、F不能使湿润的石蕊试纸变色;
②A能使湿润的蓝色石蕊试纸先变红,后褪色;将红热的铜丝放入装有A的瓶中,瓶内充满棕黄色的烟;
③将点燃的镁条放入装有E的瓶中,镁条剧烈燃烧,生成白色粉末,瓶内壁附着黑色颗粒;
④D是最简单的有机物;F是空气中含量最多的气体.
⑤实验室中可用浓的C溶液与某黑色固体共热制A气体.
回答下列问题:
(1)B的化学式为
(2)③中发生反应的化学方程式是
| ||
. |
| ||
. |
(3)⑤中发生反应的化学方程式是
| ||
| ||
(4)已知标准状况下体积为1.12L的D完全燃烧生成E和液态水时,放出热量44.5kJ,写出表示1molD燃烧的热化学方程式
(5)一定条件下,向废水中加入CH3OH,将HNO3还原成F.若该反应消耗16gCH3OH转移3mol电子;该反应的化学方程式为
①B能使湿润的红色石蕊试纸变蓝,D、F不能使湿润的石蕊试纸变色;
②A能使湿润的蓝色石蕊试纸先变红,后褪色;将红热的铜丝放入装有A的瓶中,瓶内充满棕黄色的烟;
③将点燃的镁条放入装有E的瓶中,镁条剧烈燃烧,生成白色粉末,瓶内壁附着黑色颗粒;
④D是最简单的有机物;F是空气中含量最多的气体.
⑤实验室中可用浓的C溶液与某黑色固体共热制A气体.
回答下列问题:
(1)B的化学式为______,固态E可用作______(写一种重要用途)
(2)③中发生反应的化学方程式是______;
(3)⑤中发生反应的化学方程式是______;
(4)已知标准状况下体积为1.12L的D完全燃烧生成E和液态水时,放出热量44.5kJ,写出表示1molD燃烧的热化学方程式______.
(5)一定条件下,向废水中加入CH3OH,将HNO3还原成F.若该反应消耗16gCH3OH转移3mol电子;该反应的化学方程式为______.
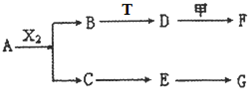 下列物质有如下转化关系(有的生成物未列出,反应条件均省略),其中:A在常温下是一种气体,能使湿润的红色石蕊试纸显蓝色,D为碱,G为酸,金属甲在G 的浓溶液中会钝化;F的溶液中只含一种溶质.
下列物质有如下转化关系(有的生成物未列出,反应条件均省略),其中:A在常温下是一种气体,能使湿润的红色石蕊试纸显蓝色,D为碱,G为酸,金属甲在G 的浓溶液中会钝化;F的溶液中只含一种溶质.A、B、C、D、E均由Q、R、X、T四种短周期元素中的两种或三种组成,且Q、R、X、T原子序数依次增大;X的最外层电子数是电子层数的3倍;R和X相邻;Q和T同主族,Q为非金属元素,T为金属元素.则:
(1)X在周期表中的位置是
(2)A和G等物质的量反应生成的产物的水溶液显
(3)A和X2反应的化学方程式为
| ||
| △ |
| ||
| △ |
(4)为保护环境,通过安装汽车尾气处理装置,使尾气中的E和一氧化碳反应转化为两种空气的成分,当有22.4L的E(标准状况)转化时,转移的电子数为
C和CuO在高温下反应可能生成Cu、Cu20、C02、CO.现将1g碳粉跟8gCuO混合,在硬质试管中隔绝空气高温加热,生成的气体全部通过足量NaOH溶液,收集残余气体.测得溶液增重1.1g,残余气体在标准状况下的体积为560mL.下列说法错误的
- A.固体混合物高温加热时,有0.6g碳参加了反应
- B.试管中的所有氧化还原反应共转移电子0.15mol
- C.反应后的试管中固体混合物总质量为7.2g
- D.反应生成铜和氧化亚铜的总物质的量为0.1mol
X、Y、Z、W均为含有10电子的微粒,W为金属阳离子,X、Y、Z常温下为气体,
(1)已知: W + X + H2O → 白色沉淀。
①若实验室用下图所示装置、干燥和收集装置制取并收集干燥的X,A中分液漏斗中的液态试剂的仪器的名称是________,仪器的连接顺序为a→________________________;
②由W离子形成的可溶性盐WCln,其水溶液显_________性,原因是(用离子方程式表示)_____________________________________________________
③为进一步确定W,进行如下实验,请补全实验操作、现象和结论:取上述白色沉淀少量置于试管中,_____________________________________________________
(2)常温下,取10 mL pH= a的Y的稀溶液,加水稀释时pH随溶液体积V的变化如图所示,则①Y的化学式为__________。
②下列有关Y的叙述正确的是__________
A.Y溶于水后部分发生电离
B.Y的水溶液中滴加石蕊试液会变红
C.稀释后溶液中所有离子的浓度均减小
D.稀释后,阴离子的物质的量浓度之和不变
③一定量X溶液和一定量的Y的溶液混合,所得溶液中离子浓度的等式关系为:
(用实际离子符号表示)
(3)已知H2的燃烧热为285.8 kJ·mol-1。现有Z和H2 的混合气体共0.2 mol,与O2完全燃烧生成H2O(l)和CO2(g),转移电子的物质的量为1.0 mol,放出的热量为117.6 kJ。写出Z完全燃烧的热化学反应方程式__________________________________
查看习题详情和答案>>





 (4)
(3分)
(4)
(3分)



















