网址:http://m.1010jiajiao.com/timu_id_46307[举报]
一、选择题(每小题1分,共30分)
题号
1
2
3
4
5
6
7
8
9
10
答案
A
A
C
C
C
D
D
C
A
B
题号
11
12
13
14
15
16
17
18
19
20
答案
B
B
D
C
D
C
C
B
B
D
题号
21
22
23
24
25
26
27
28
29
30
答案
A
D
C
C
A
C
C
A
A
A
二、填空题(每空1分,共26分)
31.(7分)(1) Fe2O3+3CO高温 2Fe+3CO2 ; (12 + 1×2 +19×2) ×n
(2) ① B 、D 、E ; ② A ; ③ 隔绝空气做保护气
(3)① A ; ② A
 32.(6分)(1)物理变化
32.(6分)(1)物理变化
(2)① CH4 + 2O2 CO2 + 2H2O
②A、B、C、D
 (3)① 玻璃棒
(3)① 玻璃棒
 ② CaCl2 + Na2CO3 CaCO3
↓ +
2NaCl
② CaCl2 + Na2CO3 CaCO3
↓ +
2NaCl
③ Na2CO3 + 2HCl 2NaCl + H2O + CO2 ↑
33.(4分) ① 6:7:2:1
② 防食品被氧化和挤压破碎
③ 铁粉
④ 相同条件时,气体分子比液态物质分子运动的快

 34.(5分)(1)① 2Al +
6HCl
2AlCl3 + 3H2 ↑(写H2SO4也可)
34.(5分)(1)① 2Al +
6HCl
2AlCl3 + 3H2 ↑(写H2SO4也可)
② 2H2O 2H2O + O2 ↑
 ③ CaO + H2O Ca(OH)2
③ CaO + H2O Ca(OH)2
 ④ NaHCO3 + HCl NaCl
+ H2O + CO2 ↑
④ NaHCO3 + HCl NaCl
+ H2O + CO2 ↑
(2) NH4NO3
35.(4分)(1) CO2
(2) 纯碱

 (3) Ca(OH)2 + CO2
CaCO3↓+
H2O
(3) Ca(OH)2 + CO2
CaCO3↓+
H2O
(4) Ca(OH)2 + Na2CO3 CaCO3↓+ 2NaOH
三、实验题(共18分)
 36. (6分)(1) ①试管 ②锥形瓶
36. (6分)(1) ①试管 ②锥形瓶
(2)A、B ;D、F ;2KMnO4 K2MnO4 + MnO2 + O2 ↑
(3)B、D
37. (6分)【查阅资料】①
请你完成下表中空余部分。
猜想
实验设计及装置
观察到的实验现象
猜想②
果肉表面出现咖啡色
猜想④
果肉表面未出现咖啡色
猜想⑤
B、F
【反思与评价】氧气溶于水,会慢慢氧化果肉。
【应用】使用保护气和煮沸过的凉水,保存时加保护气或抽出空气且密闭。
38.(6分) (1)填充实验过程空格项:
实 验 步 骤
实 验 现 象
实 验 结 论
步骤①
溶液变红 。

步骤②
边加边搅拌 。
步骤③


步骤④
有无色晶体析出 。
浓硫酸有吸水性。
(3)总结:A. H+ 、OH-
B. 25%
四、计算题(共6分)
 39. (1)解:设样品未被氧化的镁的质量为X
39. (1)解:设样品未被氧化的镁的质量为X
Mg + H2SO4 = MgSO4 + H2 ↑
24 2 (1分)
X
24:2 = X:
(2)解:样品MgO的质量=

 样品被氧化前的质量=
样品被氧化前的质量=
答: 略 (1分)
40.(1) 2.8 (1分)
(2) 82.5% (1分)
(3)由试题分析20g稀盐酸恰好能与石灰石中的5g碳酸钙完全反应
解:设盐酸溶液中溶质的质量分数为x。
CaCO3 + 2HCl =CaCl2+H2O+CO2↑
100 73
100∶73 =
x=18.25% (1分)
房山区2008学年初三化学第二次统测试卷参考答案
一、选择题(每小题1分,共30分)
题号
1
2
3
4
5
6
7
8
9
10
答案
A
A
C
C
C
D
D
C
A
B
题号
11
12
13
14
15
16
17
18
19
20
答案
B
B
D
C
D
C
C
B
B
D
题号
21
22
23
24
25
26
27
28
29
30
答案
A
D
C
C
A
C
C
A
A
A
二、填空题(每空1分,共26分)
31.(7分)(1) Fe2O3+3CO高温 2Fe+3CO2 ; (12 + 1×2 +19×2) ×n
(2) ① B 、D 、E ; ② A ; ③ 隔绝空气做保护气
(3)① A ; ② A
 32.(6分)(1)物理变化
32.(6分)(1)物理变化
(2)① CH4 + 2O2 CO2 + 2H2O
②A、B、C、D
 (3)① 玻璃棒
(3)① 玻璃棒
 ② CaCl2 + Na2CO3 CaCO3
↓ +
2NaCl
② CaCl2 + Na2CO3 CaCO3
↓ +
2NaCl
③ Na2CO3 + 2HCl 2NaCl + H2O + CO2 ↑
33.(4分) ① 6:7:2:1
② 防食品被氧化和挤压破碎
③ 铁粉
④ 相同条件时,气体分子比液态物质分子运动的快

 34.(5分)(1)① 2Al +
6HCl
2AlCl3 + 3H2 ↑(写H2SO4也可)
34.(5分)(1)① 2Al +
6HCl
2AlCl3 + 3H2 ↑(写H2SO4也可)
② 2H2O 2H2O + O2 ↑
 ③ CaO + H2O Ca(OH)2
③ CaO + H2O Ca(OH)2
 ④ NaHCO3 + HCl NaCl
+ H2O + CO2 ↑
④ NaHCO3 + HCl NaCl
+ H2O + CO2 ↑
(2) NH4NO3
35.(4分)(1) CO2
(2) 纯碱

 (3) Ca(OH)2 + CO2
CaCO3↓+
H2O
(3) Ca(OH)2 + CO2
CaCO3↓+
H2O
(4) Ca(OH)2 + Na2CO3 CaCO3↓+ 2NaOH
三、实验题(共18分)
 36. (6分)(1) ①试管 ②锥形瓶
36. (6分)(1) ①试管 ②锥形瓶
(2)A、B ;D、F ;2KMnO4 K2MnO4 + MnO2 + O2 ↑
(3)B、D
37. (6分)【查阅资料】①
请你完成下表中空余部分。
猜想
实验设计及装置
观察到的实验现象
猜想②
果肉表面出现咖啡色
猜想④
果肉表面未出现咖啡色
猜想⑤
B、F
【反思与评价】氧气溶于水,会慢慢氧化果肉。
【应用】使用保护气和煮沸过的凉水,保存时加保护气或抽出空气且密闭。
38.(6分) (1)填充实验过程空格项:
实 验 步 骤
实 验 现 象
实 验 结 论
步骤①
溶液变红 。

步骤②
边加边搅拌 。
步骤③


步骤④
有无色晶体析出 。
浓硫酸有吸水性。
(3)总结:A. H+ 、OH-
B. 25%
四、计算题(共6分)
 39. (1)解:设样品未被氧化的镁的质量为X
39. (1)解:设样品未被氧化的镁的质量为X
Mg + H2SO4 = MgSO4 + H2 ↑
24 2 (1分)
X
24:2 = X:
(2)解:样品MgO的质量=

 样品被氧化前的质量=
样品被氧化前的质量=
答: 略 (1分)
40.(1) 2.8 (1分)
(2) 82.5% (1分)
(3)由试题分析20g稀盐酸恰好能与石灰石中的5g碳酸钙完全反应
解:设盐酸溶液中溶质的质量分数为x。
CaCO3 + 2HCl =CaCl2+H2O+CO2↑
100 73
100∶73 =
x=18.25% (1分)
【方案一】气体转化法
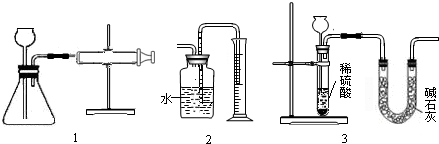
(1)如图1所示,把wg的混合物与足量稀硫酸反应后,测定产生的CO2的体积,检查该装置气密性的方法是
(2)有同学提出用图2代替图1中的收集装置,则所测得CO2气体的体积
(填偏大、偏小或不变)理由是
(3)也有人用图3装置测定CO2的质量(碱石灰的成分是CaO和NaOH的混合物)则图3实验装置中主要存在哪些缺陷?这些缺陷对实验结果有何影响?
| 主 要 缺 陷 | 对实验结果的影响 |
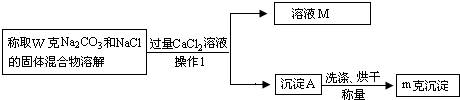
(1)沉淀A的化学式是
(2)确定CaCl2溶液是否过量的方法是
(3)该固体混合物中Na2CO3的质量分数的计算式为
(4)导致测定结果偏大的原因可能是
【方案三】盐酸滴定法

(1)“操作2”的名称是
(2)根据实验数据计算该固体混合物中Na2CO3的质量分数为
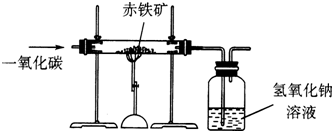 (2006?南平)小明在学完铁的冶炼原理后,借鉴CO还原CuO的实验,设计了如图所示的装置,测定20g某赤铁矿石中氧化铁(Fe2O3)的质量分数.假设赤铁矿石中氧化铁全部还原为铁且CO2被氢氧化钠溶液完全吸收(有关反应方程式:3CO+Fe2O3
(2006?南平)小明在学完铁的冶炼原理后,借鉴CO还原CuO的实验,设计了如图所示的装置,测定20g某赤铁矿石中氧化铁(Fe2O3)的质量分数.假设赤铁矿石中氧化铁全部还原为铁且CO2被氢氧化钠溶液完全吸收(有关反应方程式:3CO+Fe2O3
| ||
| 实验前 | 实验后 | |
| 洗气瓶(包括氢氧化钠溶液) | 156.8g | 170.0g |
(1)20g赤铁矿石中氧化铁(Fe2O3)的质量分数?
(2)指出上述实验设计中的不合理之处,并说明理由.
| 实验前 | 试验后 | |
| 玻璃管(包括样品) | 85.6g | 80.8g |
| 洗气瓶(包括药品) | 156.8g | 170.0g |
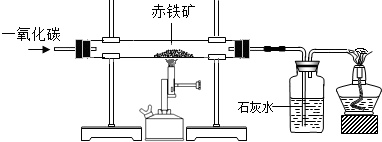
根据实验数据计算:
(1)赤铁矿中氧化铁的质量分数;
(2)实验结束后,玻璃管中剩余粉末里的铁的质量分数.(杂质不含其他可被还原的氧化物)
①用天平称量10g该金属的小颗粒;②将金属放在烧杯中,加入100g稀硫酸,充分反应至没有气泡放出,有金属剩余;③用
请你帮助该实验小组的同学,根据实验数据计算:
(1)金属R的相对原子质量. (2)本实验所用稀硫酸的质量分数. 查看习题详情和答案>>
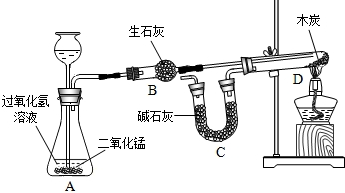
探究过程如下:I.称量装有干燥块状木炭的试管D,质量为50.7g,装有碱石灰的干燥管质量为112.3g,连接A、B、D装置;
II.从从长颈漏斗中加入3%的过氧化氢溶液,连接C装置,点燃酒精灯;
III.待D中发生反应,熄灭酒精灯,冷却;
IV.称量试管D及剩余固体质量为50.1g,装置C的质量为114.5g.
已知:碱石灰主要成分是氧化钙和氢氧化钠,木炭中的杂质不参加反应,B、C中所装药品是足量的能够完全吸收相关物质.请回答下列问题:
(1)装置A中发生反应的化学方程式为
| ||
| ||
(2)酒精灯的作用是
(3)为减少误差,步骤III冷却过程中需要注意的问题是
(4)根据实验数据计算参加反应的氧气质量为