摘要:23.从20世纪中叶开始.硅成了信息技术的关键材料.是目前应用最多的半导体材料.请回答-下列问题: (1)地壳里各种元素的含量如右图所示.其中表示硅元素的是 . (2)根据元素周期表可知.原子序数为6的碳原子和原子序数为14的硅原子最外层电子数均为4.则常温下硅的化学性质 (选琐“活泼 . “不活泼 ). (3)制备硅半导体材料必须先得到高纯硅.三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法.生产过程示意如下: ①整个制备过程必须达到无水无氧.在H2还原SiHCl3过程中若混入O2 .可能引起的后果是 . ②在生产过程中物质A可循环使用.A的化学式是 ,在生产过程中还有一种可循环使用的物质是 . 23.碘元素对人体健康起着重要的作用.在食盐中加碘科有效预防甲状腺肿大的发生. 如图是某品牌加碘盐的标签.请回答下列问题.(相对原子质量:K-39 I-127 O-16) (1)写出碘酸钾中阳离子的符号 ▲ .碘酸钾中K.I. O三种元素的质量比为 ▲ . (2)下列物质遇到碘(I2)显蓝色的是 ▲ .(填字母序 号) A.蔗糖水 B.米汤 C.食盐水 (3)高温烹饪会使含碘量降低.说明碘酸钾的化学性质之一是 ▲ . (4)根据有关数据估算.每500g该加碘食盐中碘酸钾(KIO3)的质量范围是 ▲ .(填 字母序号) A.15~30mg B.25~51mg C.60~120mg
网址:http://m.1010jiajiao.com/timu_id_4456700[举报]
(09南京)(6分)化学就在我们身边。
(1)现有下列四种物质;尿素、石油、汞、合成橡胶、请选择相应的物质填空:
①可做汽车轮胎的材料是 ②温度计中填充的液态金属是
③可作氮肥的是 ④被称为“工业的血液”的化石燃料是
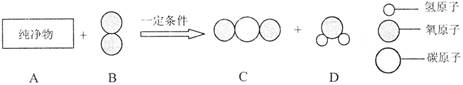
(2)A物质常用于焊接或切割金属。把一定质量的纯净物A和40 g的纯净物B在—定条件下按下图所示充分反应,当B物质反应完时,可生成44g C物质和9 g D物质。

①参加反应的A物质的质量是 。
②A物质中各元素的质量比为 。
查看习题详情和答案>>
(09南京)(6分)化学就在我们身边。
(1)现有下列四种物质;尿素、石油、汞、合成橡胶、请选择相应的物质填空:
①可做汽车轮胎的材料是 ②温度计中填充的液态金属是
③可作氮肥的是 ④被称为“工业的血液”的化石燃料是
(2)A物质常用于焊接或切割金属。把一定质量的纯净物A和40 g的纯净物B在—定条件下按下图所示充分反应,当B物质反应完时,可生成44g C物质和9 g D物质。

①参加反应的A物质的质量是 。
②A物质中各元素的质量比为 。
查看习题详情和答案>>
(09南京)(6分)化学就在我们身边。
(1)现有下列四种物质;尿素、石油、汞、合成橡胶、请选择相应的物质填空:
①可做汽车轮胎的材料是 ②温度计中填充的液态金属是
③可作氮肥的是 ④被称为“工业的血液”的化石燃料是
(2)A物质常用于焊接或切割金属。把一定质量的纯净物A和40 g的纯净物B在—定条件下按下图所示充分反应,当B物质反应完时,可生成44g C物质和9 g D物质。

①参加反应的A物质的质量是 。
②A物质中各元素的质量比为 。 查看习题详情和答案>>
(1)现有下列四种物质;尿素、石油、汞、合成橡胶、请选择相应的物质填空:
①可做汽车轮胎的材料是 ②温度计中填充的液态金属是
③可作氮肥的是 ④被称为“工业的血液”的化石燃料是
(2)A物质常用于焊接或切割金属。把一定质量的纯净物A和40 g的纯净物B在—定条件下按下图所示充分反应,当B物质反应完时,可生成44g C物质和9 g D物质。

①参加反应的A物质的质量是 。
②A物质中各元素的质量比为 。 查看习题详情和答案>>