摘要:14. ⑴A:CaCO3 B:CaO C:Ca(OH)2 D:HCl ⑵Ca(OH)2+CO2 = CaCO3↓+H2O CaCO3+2HCl = CaCl2+H2O+CO2↑
网址:http://m.1010jiajiao.com/timu_id_4456640[举报]
(2006?宣武区二模)A、E、F是自然界万物离不开的物质,B、C、D是重要的燃料,W、X、Y、Z是四种不同类别的物质,它们之间能发生如下变化,请你根据初中化学学习过的常见物质的知识和以下信息作出推断.(图中略去部分反应的产物)
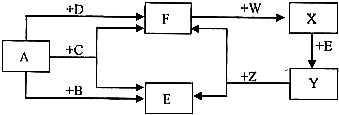
(1)写出下列物质的化学式:A
(2)写出下列变化的化学方程式
F→X
X→Y
Y→E
(3)在A~Z中,能使紫色石蕊试液显红色的物质是(填化学式)
查看习题详情和答案>>

(1)写出下列物质的化学式:A
O2
O2
;CCH4
CH4
;DH2
H2
;(2)写出下列变化的化学方程式
F→X
H2O+CaO=Ca(OH)2
H2O+CaO=Ca(OH)2
;X→Y
Ca(OH)2+CO2═CaCO3↓+H2O
Ca(OH)2+CO2═CaCO3↓+H2O
;Y→E
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
;(3)在A~Z中,能使紫色石蕊试液显红色的物质是(填化学式)
CO2,HCl
CO2,HCl
.(2009?怀柔区一模)在化学反应中,物质所含元素的化合价发生变化的反应就是氧化还原反应.
如:2
+
2═2
反应前后,Na、Cl的化合价发生了变化,该反应是氧化还原反应.
(1)请根据化合价是否变化进行分析,下列反应属于氧化还原反应的是
A.2Mg+O2
2MgO B.CaO+H2O═Ca(OH)2
C.2KClO3
2KCl+3O2↑ D.CaCO3
CaO+CO2↑
E.H2+CuO
Cu+H2O F.HCl+NaOH═NaCl+H2O
(2)请根据上面的分析和推理,对四种反应类型是否发生氧化还原反应作出概括:
置换反应
查看习题详情和答案>>
如:2
| 0 |
| Na |
| 0 |
| Cl |
| +1 |
| Na |
| -1 |
| Cl |
(1)请根据化合价是否变化进行分析,下列反应属于氧化还原反应的是
A、C、E
A、C、E
A.2Mg+O2
| ||
C.2KClO3
| ||
| △ |
| ||
E.H2+CuO
| ||
(2)请根据上面的分析和推理,对四种反应类型是否发生氧化还原反应作出概括:
置换反应
是
是
,化合反应不一定
不一定
,分解反应不一定
不一定
,复分解反应否
否
.按下列要求书写的化学方程式正确的是( )
A.铁在氧气中燃烧:4Fe + 3O2===2Fe2O3
B.澄清石灰水和盐酸发生中和反应:CaO+2HCl===CaCl2+H2O
C.用碳酸氢钠治疗过多胃酸:NaHCO3+HCl===NaCl+H2O+CO2↑
D.检验混合气体中是否含有二氧化碳:CO2+Ca(OH)2 ===CaCO3+H2O
查看习题详情和答案>>某化学兴趣小组以不同的化学思维方式或者规律给下列化学反应的类型进行分类,你认为分类合理的一组是:( )
①CaO+H2O═Ca(OH)2; ②CaCO3煅烧Ca O+CO2↑;
③NaOH+HCl═NaCl+H2O; ④Zn+H2SO4═ZnSO4+H2↑;
⑤2Mg+O2 2MgO.
2MgO.
| A.属于化合反应的是①② | B.属于复分解反应的是③④ |
| C.属于有热量放出的反应的是②③ | D.属于有元素化合价变化的是④⑤ |
(4分)在化学反应中,有元素的化合价发生变化的反应就是氧化还原反应。例:
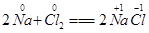 ,反应前后,Na、Cl的化合价发生了变化,该反应是氧化还原反应。(1)根据化合价是否变化分析,下列反应属于氧化还原反应的是(填序号)_________。
,反应前后,Na、Cl的化合价发生了变化,该反应是氧化还原反应。(1)根据化合价是否变化分析,下列反应属于氧化还原反应的是(填序号)_________。
A.2Mg+O22MgO B .CaO+H2O=== Ca(OH)2
C.2KClO3 2KCl+3O2↑ D .CaCO3
CaO + CO2↑
E.H2 + CuO Cu + H2O F.HCl +NaOH===NaCl + H2O
(2)含有高价态的化合物,通常具有氧化性,如在氯化铁溶液中,氯化铁能将单质铜氧化成氯化铜,自身被还原成氯化亚铁。该反应的化学方程式可表示为____________________。
查看习题详情和答案>>