摘要: l g炭与适量水蒸气反应生成CO和H2.需吸收10.94 kJ热量.此反应的热化学方程式为 A.C+H2O==CO+H2 △H=+131.3 kJ/mol B.C(s)+H2O+H2(g) △H=+10.94 kJ/mol C.C(s)+H2O+H2(g) △H=+131.3 kJ/mol D.C(s)+H2O+H2(g) △H=+131.3 kJ/mol
网址:http://m.1010jiajiao.com/timu_id_4455677[举报]
合成氨生产技术的创立开辟了人工固氮的途径,对化学工业技术也产生了重大影响.合成氨反应的化学方程式为:N2(g)+3H2(g) 2(((NH3(g)△H=-92.2kJ/mol.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得.
2(((NH3(g)△H=-92.2kJ/mol.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得.
(1)在一容积固定的密闭容器中注入N2和H2两种气体,发生上述反应.在某温度下达到平衡时各物质的浓度分别为c(H2)=9.00mol/L,c(N2)=3.00mol/L,c(NH3)=4.00mol/L,此温度下该反应的平衡常数为
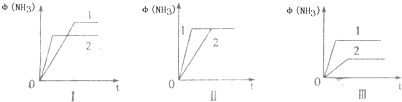
(2)三个相同容器中各充入1molN2和3molH2,在不同条件下反应并达到平衡,氨的体积分数随时间的变化如图所示.下列说法正确的是
A.图I可能是不同压强对反应的影响,且P2>P1
B.图Ⅱ可能是不同压强对反应的影响,且P1>P2
C.图Ⅲ可能是不同温度对反应的影响,且T1>T2
D.图Ⅱ一定是在同温同压下不同催化剂对反应的影响,且催化剂效果1>2
(3)将水蒸气通过红热的炭即产生水蒸气,化学方程式为:C(s)+H2O(g)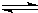 H2(g)+CO(g)△H=+131.3kJ,△S=+133.7J/K该反应在低温下能否自发
H2(g)+CO(g)△H=+131.3kJ,△S=+133.7J/K该反应在低温下能否自发
(4)甲烷在高温下与水蒸气反应反应方程式为:CH4(g)+H2O(g)=CO(g)+3H2(g).部分物质的燃烧热数据如下表:
已知1mol H2O(g)转变为1mol H2O(l)时放出44.0kJ热量.写出CH4和H2O在高温下反应的热化学方程式
(5)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制取新型燃料电池.请写出该电池的正极反应式
查看习题详情和答案>>
 2(((NH3(g)△H=-92.2kJ/mol.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得.
2(((NH3(g)△H=-92.2kJ/mol.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得.
(1)在一容积固定的密闭容器中注入N2和H2两种气体,发生上述反应.在某温度下达到平衡时各物质的浓度分别为c(H2)=9.00mol/L,c(N2)=3.00mol/L,c(NH3)=4.00mol/L,此温度下该反应的平衡常数为
7.32×10-3
7.32×10-3
.(2)三个相同容器中各充入1molN2和3molH2,在不同条件下反应并达到平衡,氨的体积分数随时间的变化如图所示.下列说法正确的是
D
D
(填序号).A.图I可能是不同压强对反应的影响,且P2>P1
B.图Ⅱ可能是不同压强对反应的影响,且P1>P2
C.图Ⅲ可能是不同温度对反应的影响,且T1>T2
D.图Ⅱ一定是在同温同压下不同催化剂对反应的影响,且催化剂效果1>2
(3)将水蒸气通过红热的炭即产生水蒸气,化学方程式为:C(s)+H2O(g)
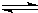 H2(g)+CO(g)△H=+131.3kJ,△S=+133.7J/K该反应在低温下能否自发
H2(g)+CO(g)△H=+131.3kJ,△S=+133.7J/K该反应在低温下能否自发否
否
(填:能或否).(4)甲烷在高温下与水蒸气反应反应方程式为:CH4(g)+H2O(g)=CO(g)+3H2(g).部分物质的燃烧热数据如下表:
| 物 质 | 燃烧热(kJ?mol-1) |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.1kJ?mol-1
CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.1kJ?mol-1
.(5)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制取新型燃料电池.请写出该电池的正极反应式
N2+6e-+8H+=2NH4+
N2+6e-+8H+=2NH4+
.合成氨生产技术的创立开辟了人工固氮的途径,对化学工业技术也产生了重大影响.合成氨反应的化学方程式为:N2(g)+3H2(g)

2(((NH3(g)△H=-92.2kJ/mol.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得.

(1)在一容积固定的密闭容器中注入N2和H2两种气体,发生上述反应.在某温度下达到平衡时各物质的浓度分别为c(H2)=9.00mol/L,c(N2)=3.00mol/L,c(NH3)=4.00mol/L,此温度下该反应的平衡常数为______.
(2)三个相同容器中各充入1molN2和3molH2,在不同条件下反应并达到平衡,氨的体积分数随时间的变化如图所示.下列说法正确的是______(填序号).
A.图I可能是不同压强对反应的影响,且P2>P1
B.图Ⅱ可能是不同压强对反应的影响,且P1>P2
C.图Ⅲ可能是不同温度对反应的影响,且T1>T2
D.图Ⅱ一定是在同温同压下不同催化剂对反应的影响,且催化剂效果1>2
(3)将水蒸气通过红热的炭即产生水蒸气,化学方程式为:C(s)+H2O(g)

H2(g)+CO(g)△H=+131.3kJ,△S=+133.7J/K该反应在低温下能否自发______(填:能或否).
(4)甲烷在高温下与水蒸气反应反应方程式为:CH4(g)+H2O(g)=CO(g)+3H2(g).部分物质的燃烧热数据如下表:
已知1mol H2O(g)转变为1mol H2O(l)时放出44.0kJ热量.写出CH4和H2O在高温下反应的热化学方程式______.
(5)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制取新型燃料电池.请写出该电池的正极反应式______.
查看习题详情和答案>>

2(((NH3(g)△H=-92.2kJ/mol.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得.

(1)在一容积固定的密闭容器中注入N2和H2两种气体,发生上述反应.在某温度下达到平衡时各物质的浓度分别为c(H2)=9.00mol/L,c(N2)=3.00mol/L,c(NH3)=4.00mol/L,此温度下该反应的平衡常数为______.
(2)三个相同容器中各充入1molN2和3molH2,在不同条件下反应并达到平衡,氨的体积分数随时间的变化如图所示.下列说法正确的是______(填序号).
A.图I可能是不同压强对反应的影响,且P2>P1
B.图Ⅱ可能是不同压强对反应的影响,且P1>P2
C.图Ⅲ可能是不同温度对反应的影响,且T1>T2
D.图Ⅱ一定是在同温同压下不同催化剂对反应的影响,且催化剂效果1>2
(3)将水蒸气通过红热的炭即产生水蒸气,化学方程式为:C(s)+H2O(g)

H2(g)+CO(g)△H=+131.3kJ,△S=+133.7J/K该反应在低温下能否自发______(填:能或否).
(4)甲烷在高温下与水蒸气反应反应方程式为:CH4(g)+H2O(g)=CO(g)+3H2(g).部分物质的燃烧热数据如下表:
| 物 质 | 燃烧热(kJ?mol-1) |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
(5)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制取新型燃料电池.请写出该电池的正极反应式______.
合成氨生产技术的创立开辟了人工固氮的途径,对化学工业技术也产生了重大影响.合成氨反应的化学方程式为:N2(g)+3H2(g) 2(((NH3(g)△H=-92.2kJ/mol.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得.
2(((NH3(g)△H=-92.2kJ/mol.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得.

(1)在一容积固定的密闭容器中注入N2和H2两种气体,发生上述反应.在某温度下达到平衡时各物质的浓度分别为c(H2)=9.00mol/L,c(N2)=3.00mol/L,c(NH3)=4.00mol/L,此温度下该反应的平衡常数为______.
(2)三个相同容器中各充入1molN2和3molH2,在不同条件下反应并达到平衡,氨的体积分数随时间的变化如图所示.下列说法正确的是______(填序号).
A.图I可能是不同压强对反应的影响,且P2>P1
B.图Ⅱ可能是不同压强对反应的影响,且P1>P2
C.图Ⅲ可能是不同温度对反应的影响,且T1>T2
D.图Ⅱ一定是在同温同压下不同催化剂对反应的影响,且催化剂效果1>2
(3)将水蒸气通过红热的炭即产生水蒸气,化学方程式为:C(s)+H2O(g) H2(g)+CO(g)△H=+131.3kJ,△S=+133.7J/K该反应在低温下能否自发______(填:能或否).
H2(g)+CO(g)△H=+131.3kJ,△S=+133.7J/K该反应在低温下能否自发______(填:能或否).
(4)甲烷在高温下与水蒸气反应反应方程式为:CH4(g)+H2O(g)=CO(g)+3H2(g).部分物质的燃烧热数据如下表:
已知1mol H2O(g)转变为1mol H2O(l)时放出44.0kJ热量.写出CH4和H2O在高温下反应的热化学方程式______.
(5)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制取新型燃料电池.请写出该电池的正极反应式______.
查看习题详情和答案>>
 2(((NH3(g)△H=-92.2kJ/mol.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得.
2(((NH3(g)△H=-92.2kJ/mol.合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得.
(1)在一容积固定的密闭容器中注入N2和H2两种气体,发生上述反应.在某温度下达到平衡时各物质的浓度分别为c(H2)=9.00mol/L,c(N2)=3.00mol/L,c(NH3)=4.00mol/L,此温度下该反应的平衡常数为______.
(2)三个相同容器中各充入1molN2和3molH2,在不同条件下反应并达到平衡,氨的体积分数随时间的变化如图所示.下列说法正确的是______(填序号).
A.图I可能是不同压强对反应的影响,且P2>P1
B.图Ⅱ可能是不同压强对反应的影响,且P1>P2
C.图Ⅲ可能是不同温度对反应的影响,且T1>T2
D.图Ⅱ一定是在同温同压下不同催化剂对反应的影响,且催化剂效果1>2
(3)将水蒸气通过红热的炭即产生水蒸气,化学方程式为:C(s)+H2O(g)
 H2(g)+CO(g)△H=+131.3kJ,△S=+133.7J/K该反应在低温下能否自发______(填:能或否).
H2(g)+CO(g)△H=+131.3kJ,△S=+133.7J/K该反应在低温下能否自发______(填:能或否).(4)甲烷在高温下与水蒸气反应反应方程式为:CH4(g)+H2O(g)=CO(g)+3H2(g).部分物质的燃烧热数据如下表:
| 物 质 | 燃烧热 |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
(5)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制取新型燃料电池.请写出该电池的正极反应式______.
查看习题详情和答案>>