摘要:某温度下.相同pH值的盐酸和醋酸溶液分别加水稀释.平衡pH值随溶液体积变化的曲线如右图所示.据图判断正确的是 A.Ⅱ为盐酸稀释时pH值变化曲线 B.b点溶液的导电性比c点溶液的导电性强 C.a点Ka的数值比c点Ku的数值大 D.b点酸的总浓度大于a点酸的总浓度 [答案]B [解析]醋酸在稀释时会继续电离.则在稀释相同体积的过程中醋酸中的H+大.pH小.A项错误,随着稀释体积的增大.醋酸电离程度虽增大.但离子浓度在减小.B项正确,温度一定.任何稀的水溶液中的Kw都是一定值. C项错误,由于醋酸是弱酸.要使盐酸和醋酸溶液pH值相同.醋酸的浓度比盐酸大得多.D项错误. [考点分析]本题考查了弱电解质溶液稀释时有关量的变化与分析.
网址:http://m.1010jiajiao.com/timu_id_4450119[举报]
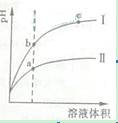 某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH 值随溶液体积
某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH 值随溶液体积![]() 变化的曲线如右图所示。据图判断正确的是( )
变化的曲线如右图所示。据图判断正确的是( )
![]() A.Ⅱ为盐酸稀释时pH值变化曲线
A.Ⅱ为盐酸稀释时pH值变化曲线
![]() B.b点溶液的导电性比c点溶液的导电性强
B.b点溶液的导电性比c点溶液的导电性强
![]() C.a点Ka的数值比c点Ku的数值大
C.a点Ka的数值比c点Ku的数值大
![]() D.b点酸的总浓度大于a点酸的总浓度
D.b点酸的总浓度大于a点酸的总浓度
某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积变化的曲线如下图所示。据图判断正确的是( )

A.Ⅱ为盐酸稀释时的pH值变化曲线
B.b点溶液的导电性比c点溶液的导电性强
C.a点KW的数值比c点KW的数值大
D.b点酸的总浓度大于a点酸的总浓度
查看习题详情和答案>>某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积![]() 变化的曲线如右图所示。据图判断正确的是
变化的曲线如右图所示。据图判断正确的是
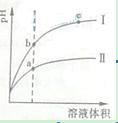
![]() A.Ⅱ为盐酸稀释时pH值变化曲线
A.Ⅱ为盐酸稀释时pH值变化曲线
![]() B.b点溶液的导电性比c点溶液的导电性强
B.b点溶液的导电性比c点溶液的导电性强
![]() C.a点Ka的数值比c点Ku的数值大
C.a点Ka的数值比c点Ku的数值大
![]() D.b点酸的总浓度大于a点酸的总浓度
D.b点酸的总浓度大于a点酸的总浓度
 某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积
某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积