摘要: 难挥发性二硫化钽(TaS2 )可采用如下装置提纯.将不纯的TaS2 粉末装入石英管一端.抽真空后引入适量碘并封管.置于加热炉中.反应如下: TaS2 (s)+2I2 (g)TaI4 (g)+S2 (g) 下列说法正确的是 A.在不同温度区域.TaI4 的量保持不变 B. 在提纯过程中.I2 的量不断减少 C.在提纯过程中.I2 的作用是将TaS2 从高温区转移到低温区 D. 该反应的平衡常数与TaI4 和S2 的浓度乘积成反比 [答案]C [解析]根据反应条件可知当温度不同时反应进行的主要方向不同所以A错误.因为是在同一密闭系统中有质量守恒定律可知I2的量不可能不断减少.而是充当一个“搬运工 的角色.将TaS2从高温区转移到低温区.B错误.根据平衡常数表达式可知K与Tal4 和S2 的浓度乘积成正比.D错误. [考点分析]考查物质的提纯.平衡常数概念.
网址:http://m.1010jiajiao.com/timu_id_4449965[举报]
难挥发性二硫化钽(TaS2)可采用如下装置提纯。将不纯的TaS2粉末装入石英管一端,抽真空后引入适量碘并封管,置于加热炉中。反应如下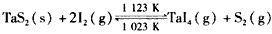 下列说法正确的是
下列说法正确的是
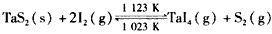 下列说法正确的是
下列说法正确的是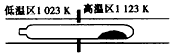
[ ]
A.在不同温度区域,TaI4的量保持不变
B.在提纯过程中,I2的量不断减少
C.在提纯过程中,I2的作用是将TaS2从高温区转移到低温区
D.该反应的平衡常数与TaI4和S2的浓度乘积成反比
查看习题详情和答案>>
B.在提纯过程中,I2的量不断减少
C.在提纯过程中,I2的作用是将TaS2从高温区转移到低温区
D.该反应的平衡常数与TaI4和S2的浓度乘积成反比
难挥发性二硫化钽(TaS2)可采用如下图所示装置提纯。将不纯的TaS2粉末装入石英管一端,抽真空后引入适量碘并封管,置于加热炉中。反应如下TaS2(s)+2I2(g)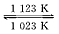 TaI4(g)+S2(g) 下列说法正确的是
TaI4(g)+S2(g) 下列说法正确的是
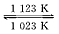 TaI4(g)+S2(g) 下列说法正确的是
TaI4(g)+S2(g) 下列说法正确的是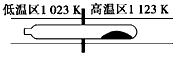
[ ]
A.在不同温度区域,TaI4的量保持不变
B.在提纯过程中,I2的量不断减少
C.在提纯过程中,I2的作用是将TaS2从高温区转移到低温区
D.该反应的平衡常数与TaI4和S2的浓度乘积成反比
查看习题详情和答案>>
B.在提纯过程中,I2的量不断减少
C.在提纯过程中,I2的作用是将TaS2从高温区转移到低温区
D.该反应的平衡常数与TaI4和S2的浓度乘积成反比
难挥发性二硫化钽(TaS2)可采用如下图所示装置提纯。将不纯的TaS2粉末装入石英管一端,抽真空后引入适量碘并封管,置于加热炉中。反应如下TaS2(s)+2I2(g)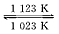 TaI4(g)+S2(g) 下列说法正确的是
TaI4(g)+S2(g) 下列说法正确的是
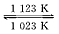 TaI4(g)+S2(g) 下列说法正确的是
TaI4(g)+S2(g) 下列说法正确的是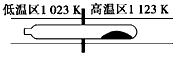
[ ]
A.在不同温度区域,TaI4的量保持不变
B.在提纯过程中,I2的量不断减少
C.在提纯过程中,I2的作用是将TaS2从高温区转移到低温区
D.该反应的平衡常数与TaI4和S2的浓度乘积成反比
查看习题详情和答案>>
B.在提纯过程中,I2的量不断减少
C.在提纯过程中,I2的作用是将TaS2从高温区转移到低温区
D.该反应的平衡常数与TaI4和S2的浓度乘积成反比
 TaI4(g)+S2(g)
TaI4(g)+S2(g)
