摘要:(2009年马鞍山市高中毕业班第三次教学质量检测)A.B.C.D是原子序数依次增大的四种短周期元素.请根据表中信息回答下列问题. 元素 A B C D 性质或结构信息 与同主族元素原子序数相差2 原子的最外层电子排布式为nsnnp2n-1 原子序数是A.B两元素原子序数之和的2倍 原子半径在所属周期中最小 (1)写出B原子的最外层轨道排布式 . (2) A与B的单质可化合生成M.A与D的单质可化合生成N.M的空间构型为 .M与N可以在空气中化合生成E.E的电子式为 .写出在E溶于水所得的溶液中各离子浓度由大到小的顺序 . (3)C的单质在空气中燃烧可生成气体F.写出F与A.C形成的化合物反应的方程式.并标出电子转移的方向和数目 .F与A.B.D单质中的一种在溶液中充分反应可生成两种酸.写出该反应的离子方程式 . [解析]A与同主族元素原子序数相差2.在短周期中只有H与Li差2.所以A为H,B原子的最外层电子排布式为nsnnp2n-1.n=2,所以B为N,C的原子序数是A.B两元素原子序数之和的2倍.所以C为S,D的原子半径在所属周期中最小.D在第三周期.所以为Cl. [答案] (1) (2)三角锥形. c(Cl-)>c(NH4+)>c(H+)>c(OH-) (3) SO2 +Cl2 +2H2O = 4H+ + SO42- + 2Cl- [考点分析]本题主要考查学生对元素周期表的熟练程度以及半径大小规律.在此基础上推导元素.结合问题考查轨道表示式.空间构型.电子式书写.离子浓度大小比较.单线桥的表示.离子反应的书写.
网址:http://m.1010jiajiao.com/timu_id_4449296[举报]
2009年的诺贝尔物理奖得主之一--美籍华裔物理学家高锟被誉为“光纤之父”,光纤通信是70年代后期发展起来的一种新型通信技术,目前长距离光纤通信系统已投入使用,光纤通信的光学纤维是由下列哪种物质经特殊工艺制成的( )
| A、碳 | B、石英 | C、锗 | D、硅 |
2009年1月18日电,由552名中国科学院院士和中国工程院院士投票评选出的2008年世界十大科技进展新闻揭晓,“铁基超导材料研究获重大进展”名列榜单.由日本和中国科学家相继发现的新的高温超导材料--铁基超导材料:其成分是氟掺杂镧(La)氧铁砷(As)化合物.下列有关该材料的判断正确的是( )
查看习题详情和答案>>
(2010?南宁二模)2009年12月7日-18日在丹麦首都哥本哈根召开了世界气候大会,商讨《京都议定书》一期承诺到期后的后续方案,即2012年至2020年的全球减排协议.大会倡导“节能减排”,下列做法不符合这一理念或说法错误的是( )
查看习题详情和答案>>
2009年“甲流”在我国流行,民间都用过氧乙酸(CH3COOOH)作为消毒剂,因它具有很强的氧化性和腐蚀性,可以迅速杀灭多种微生物,包括多种病毒(如:SARS病毒)、细菌、真菌及芽孢.有关过氧乙酸的叙述不正确的是( )
| A、过氧乙酸与羟基乙酸(HOCH2COOH)互为同分异构体 | B、过氧乙酸与苯酚混合使用杀菌能力更强 | C、过氧乙酸因具有强氧化性,所以有杀菌作用 | D、在使用过氧乙酸消毒时浓度越大越不好 |
 2009年7月21日,山东省某金矿发生硝酸泄露事故.由于浓硝酸易挥发且不稳定,事故发生时,有大量黄色、刺激性气味的烟雾产生.消防官兵到达后,立即对泄露硝酸进行处理(大量抛洒某种固体粉末等),及时地消除了事故带来的危害.
2009年7月21日,山东省某金矿发生硝酸泄露事故.由于浓硝酸易挥发且不稳定,事故发生时,有大量黄色、刺激性气味的烟雾产生.消防官兵到达后,立即对泄露硝酸进行处理(大量抛洒某种固体粉末等),及时地消除了事故带来的危害.(1)请用化学方程式解释烟雾呈黄色的原因:
4HNO3
4NO2↑+O2↑+2H2O
| ||
4HNO3
4NO2↑+O2↑+2H2O
.
| ||
(2)消防官兵向泄露的硝酸抛洒的粉末可能是
A
A
.A.生石灰;B.铁粉;C.食盐;D.石膏
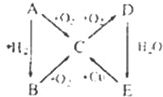
(3)若图中的E物质代表硝酸,请按要求表示下列转化:
B→C的化学方程式:
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
;
| ||
| △ |
D→E的化学方程式:
3NO2+H2O=2HNO3+NO
3NO2+H2O=2HNO3+NO
;E→C的离子方程式:
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
.