网址:http://m.1010jiajiao.com/timu_id_4435100[举报]
铁单质及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2 6SO2+Fe3O4,3 mol
FeS2参加反应转移________mol
电子。
6SO2+Fe3O4,3 mol
FeS2参加反应转移________mol
电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为
________________________________________________________________________。
从腐蚀废液回收得到金属铜还需要的试剂为
________________________________________________________________________。
(3)与明矾相似,硫酸铁也可用作絮凝剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是____________________________________________________ 。
(4)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是________(填字母)。
|
选项 |
陈述Ⅰ |
陈述Ⅱ |
判断 |
|
A |
铁是地壳中含量最高的金属元素 |
铁是人类最早使用的金属材料 |
Ⅰ对;Ⅱ对;有 |
|
B |
常温下铁与稀硫酸反应生成氢气 |
高温下氢气能还原氧化铁生成铁 |
Ⅰ 对;Ⅱ对;无 |
|
C |
铁属于过渡元素 |
铁和铁的某些化合物可以用作催化剂 |
Ⅰ 错;Ⅱ对;无 |
|
D |
铁在空气中表面生成致密氧化膜 |
可用铁罐储存运输浓硫酸、浓硝酸 |
Ⅰ 对;Ⅱ对;有 |
查看习题详情和答案>>
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2
 6SO2+Fe3O4,3 mol FeS2参加反应转移________mol 电子。
6SO2+Fe3O4,3 mol FeS2参加反应转移________mol 电子。 (2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为 ________________________________________________。从腐蚀废液回收得到金属铜还需要的试剂为 ________________________________。
(3)与明矾相似,硫酸铁也可用作絮凝剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是_____________________________________________。
(4)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是________(填字母)。
铁及其化合物在生活、生产中有广泛应用.请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料.其中一个反应为
3FeS2+8O2![]() 6SO2+Fe3O4,有3 molFeS2参加反应,转移________mol电子.
6SO2+Fe3O4,有3 molFeS2参加反应,转移________mol电子.
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为________;从腐蚀废液回收得到金属铜,还需要的试剂是________.
(3)与明矾相似,硫酸铁也可用作净水剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是________.
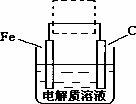
(4)钢铁的电化腐蚀简单示意图如下,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在下图虚线框内作出修改,并用箭头标出电子流动方向.
铁及其化合物在生活、生产中有广泛应用.请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料.其中一个反应为
3FeS2+O2![]() 6SO2+Fe3O4,有3 mol FeS2参加反应,转移________mol电子.
6SO2+Fe3O4,有3 mol FeS2参加反应,转移________mol电子.
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为________;从腐蚀废液回收得到金属铜,还需要的试剂是________.
(3)与明矾相似,硫酸铁也可用作净水剂,其原理是________.
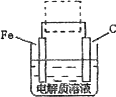
(4)钢铁的电化腐蚀简单示意图如下,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在下图虚线框内作出修改,并用箭头标出电子流动方向.

(1)酸溶过程中Fe2O3与稀硫酸反应的化学方程式是
(2)还原过程中加入FeS2是将溶液中的Fe3+还原为Fe2+,而本身被氧化为SO
2- 4 |
(3)氧化过程中通入空气和加入NaOH是为了将溶液中的铁元素充分转化为沉淀而析出,写出有关的离子方程式:
(4)生产过程中,为了确保铁红的质量,氧化过程需要调节溶液的pH至3~4,其目的是