网址:http://m.1010jiajiao.com/timu_id_4434842[举报]
现代社会中铜在电气、交通、机械和冶金、能源及石化工业、高科技等领域有广泛的应用。某铜矿石含氧化铜、氧化亚铜、三氧化二铁和脉石(Si02) ,现采用酸浸法从矿石中提取铜,其工艺流程图如下。其中铜的萃取(铜从水层进人有机层的过程)和反萃取(铜从有机层进人水层的过程)是现代湿法炼铜的重要工艺手段。

已知:①Cu2O+2H+=Cu2++Cu + H2O;②当矿石中三氧化二铁含量太低时,可用硫酸和硫酸铁的混合液浸出铜;③反萃取后的水层2是硫酸铜溶液。回答下列问题:
(1)矿石用稀硫酸处理过程中发生反应的离子方程式为:Cu2O+2H+=Cu2++Cu + H2O、
、 。(写出其中2个)
(2)“循环I”经多次循环后的水层1不能继续循环使用,但可分离出一种重要的硫酸盐晶体.若水层1暴露在空气中一段时间后,可以得到另一种重要的硫酸盐,写出水层l暴露在空气中发生反应的离子方程式 。
(3)“循环n”中萃取剂是一类称作为肟类的有机化合物,如N-510、N-530等。某肟类化合物A的分子结构中仅含n1个-CH3、n2个-OH和n3个![]() 三种基团,无环状结构,三种基团的数目关系为n3= 。若A的相对分子质量为116,上述基团连接时碳原子跟碳原子相连,则A的结构简式是 。
三种基团,无环状结构,三种基团的数目关系为n3= 。若A的相对分子质量为116,上述基团连接时碳原子跟碳原子相连,则A的结构简式是 。
(4)写出电解过程中阳极(惰性电极)发生反应的电极反应式 。
(5)该工艺最大亮点是它符合下列原理 (填字母,下同)。
A.化学平衡 B.绿色化学 C.质量守恒 D.能量守恒
E.相似相溶 F.酸碱中和 G.氧化还原反应
(6)铜、银、金是人类认识最早的三种金属,因为很早就被人们用作钱币,因而有“货币金属”之称。由于铁的金属性比铜、银、金强,相对而言,人类认识铁稍晚。某研究性学习小组为了证明铁的金属活动性比铜强,他设计了如下方案:①铁片置于硫酸铜溶液中有铜析出;②铁、铜和氯气反应分别生成FeCl3和CuCl2;③足量的铁粉和铜粉和浓硫酸反应生成FeSO4和CuSO4;④铜片置于FeCl3溶液中铜片逐渐溶解;⑤把铁片和铜片置于盛有稀硫酸的烧杯中,交用导线连接,铁片上无气泡产生,而铜片上有气泡产生;⑥把铁片和铜片置于盛有浓硝酸的烧杯中,并用导线连接,铁片上有气泡产生,而铜片上无气泡产生。以上设计合理的有 。
A.两种方案 B.三种方案 C.四种方案 D.五种方案
查看习题详情和答案>>(16分)氯碱工业是最基本的化学工业之一,它的产品除应用于化学工业本身外,还广泛应用于轻工业、纺织工业、冶金工业、石油化学工业以及公用事业。
⑴以前采用无隔膜电解冷的食盐水时,Cl2会与NaOH接触,产物中肯定有NaClO,从而影响产品的纯度。能包含这一过程的总反应方程式为
⑵现代氯碱工业多采用隔膜法进行电解,即用隔膜将电解槽分隔成阳极区和阴极区,则从阴极区排出的是 ,电解时用盐酸控制阳极区的PH在2~3,用化学平衡移动原理解释盐酸的作用:
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。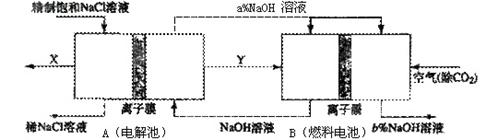 ①分析比较图中氢氧化鈉质量分数大小:a% (填“>”、“<”或“=”) b%, 理由是
①分析比较图中氢氧化鈉质量分数大小:a% (填“>”、“<”或“=”) b%, 理由是
②这样设计的主要节(电))能之处在于 (至少写一处)
⑷科研人员为减少火力发电厂对环境的污染,曾经考虑让火力发电厂和氯碱厂进行就近联合。请你判断该方案是否可行? (填可行或不可行),理由是
(16分)氯碱工业是最基本的化学工业之一,它的产品除应用于化学工业本身外,还广泛应用于轻工业、纺织工业、冶金工业、石油化学工业以及公用事业。
⑴以前采用无隔膜电解冷的食盐水时,Cl2会与NaOH接触,产物中肯定有NaClO,从而影响产品的纯度。能包含这一过程的总反应方程式为
⑵现代氯碱工业多采用隔膜法进行电解,即用隔膜将电解槽分隔成阳极区和阴极区,则从阴极区排出的是 ,电解时用盐酸控制阳极区的PH在2~3,用化学平衡移动原理解释盐酸的作用:
(3) 氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
 ①分析比较图中氢氧化鈉质量分数大小:a%
(填“>”、“<”或“=”) b%, 理由是
①分析比较图中氢氧化鈉质量分数大小:a%
(填“>”、“<”或“=”) b%, 理由是
②这样设计的主要节(电))能之处在于 (至少写一处)
⑷ 科研人员为减少火力发电厂对环境的污染,曾经考虑让火力发电厂和氯碱厂进行就近联合。请你判断该方案是否可行? (填可行或不可行),理由是
查看习题详情和答案>>
(1)实验室制取氯气也可用下图装置

①实验原理(写化学方程式):______________________________。
②收集原理:因Cl2溶于水,密度比空气大,故用向上排空气法;因Cl2在饱和食盐水中的溶解度小,故可用排饱和食盐水法收集。A、B为两个位置上的止水夹,采用向上排空气法和排饱和食盐水法收集Cl2时的正确操作是_________________________________________。
A.采用向上排空气法收集Cl2时应将A关闭,B打开
B.采用向上排空气法收集Cl2时应将B关闭,A打开
C.采用排饱和食盐水法收集Cl2时应将A关闭,B打开
D.采用排饱和食盐水法收集Cl2时应将B关闭,A打开
③尾气处理,氢氧化钠溶液的作用是处理尾气,防止氯气污染空气,该反应的离子方程式为:__________________________________________________________________。
(2)科学研究中可以用多种方法来测定阿伏加德罗常数。X射线衍射法就是其中的一种。X射线法是通过X射线衍射仪测出离子化合物离子间的间隔,再根据该化合物质量与体积的关系(密度)来确定。已知:X射线衍射仪测出的NaCl晶体中相邻钠离子与氯离子间距为a cm,NaCl相对分子质量为b。某同学为了测定阿伏加德罗常数,做了如下实验:用分析天平称取一定质量研细的NaCl固体,装入25 mL容量瓶中,然后用滴定管向容量瓶中滴加苯并不断振荡,使苯、氯化钠晶体充分混匀,标定,其实验结果如下表:
实验序号 | m NaCl/g | 消耗苯体积/cm3 | VNaCl | NA |
1 | 5.879 3 | 22.27 |
|
|
2 | 9.456 6 | 20.67 |
|
|
根据实验数据,请填写第一次实验中的空格(阿伏加德罗常数项只要求写出计算式,对原始数据不进行处理)。
查看习题详情和答案>>(1)“绿色化学”的最大特点在于它是在始端就采用预防实际污染的科学手段,因而过程和终端均为零排放和零污染,具有“原子经济性”.下列化学反应不符合“绿色化学”思想的是
A.制备环氧乙烷:2CH2=CH2+O2
| 催化剂 |
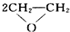
B.制备硫酸铜:Cu+2H2SO4
| ||
C.制备甲醇:2CH4+O2
| 催化剂 |
| 加热加压 |
D.制备硝酸铜:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(2)冶金废水中含有[Au(CN)2],其电离出的CN-有毒,当与H+结合生成HCN时,其毒性更强.工业上处理这种废水是在碱性条件下,用NaClO将CN-氧化为CO32-和一种无毒气体,该反应的方程式为
(3)工业上目前使用两种方法制取乙醛--“乙炔水化法”和“乙烯氧化法”.下面两表提供生产过程中原料、反应条件、原料平衡转化率和产量等的有关信息:
表一:原料、反应条件、平衡转化率、日产量
| 乙炔水化法 | 乙烯氧化法 | |
| 原料 | 乙炔、水 | 乙烯、空气 |
| 反应条件 | HgSO4、100~125℃ | PdCl2-CuCl2、100~125℃ |
| 平衡转化率 | 乙炔平衡转化率90%左右 | 乙烯平衡转化率80%左右 |
| 日产量 | 2.5吨(某设备条件下) | 3.6吨(相同设备条件下) |
| 原料生产工艺过程 | ||||||||
| 乙炔 | CaCO3
| |||||||
| 乙烯 | 来源于石油裂解气 |
①从产率和产量角度分析
②从环境保护和能耗角度分析