摘要:将一定量的NaHCO3和NH4HCO3的混合物放入坩埚内.用酒精加热到质量不变时.最终称得残留物得质量是原来的一半.则原混合物中NH4HCO3的质量数为 20.75% 26.45% [简析]因NH4HCO3分解后无残留物:2NaHCO3?Na2CO3+H2O+CO2á 残留物只是Na2CO3.巧设未知数.设wNaHCO3为84g则wNH4HCO3为xg.则必有 =53得x=22.故 ×100%=20.75%选(C)
网址:http://m.1010jiajiao.com/timu_id_4405604[举报]
(2012?浦东新区二模)将一定量的氯气通入30mL浓度为10.00mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系.下列判断正确的是( )
查看习题详情和答案>>
将一定量的锌与100mL 18.5mol/L浓硫酸充分反应后,锌完全溶解,同时生成气体A 33.6L(标准状况).将反应后的溶液稀释至1L,测得溶液的pH=1,则下列叙述中错误的是( )
查看习题详情和答案>>
(2010?西城区模拟)如图所示反应I、反应II和反应III均是工业生产中常见的反应.其中A、B为化合物,C是温室气体之一,D和K均可用做干燥剂,H常温下为液态化合物,J是一种具有漂白作用的盐,反应III和E与G反应的原理相同.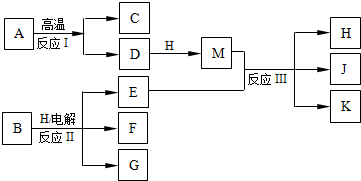
(1)C的电子式是
 .
.
(2)反应II的离子方程式是
(3)J久置后,即便不接触水、空气,本身也逐渐分解生成K,并放出气体,该反应的化学方程式是
(4)工业上测定反应III产品的有效成分J的含量,先将一定量的产品的溶液加入过量的KI溶液和稀硫酸中,使之反应生成I2,然后用Na2S2O3标准溶液滴定I2,计算出结果.
①用Na2S2O3标准溶液滴定I2时选用的指示剂是
②生成I2的反应的离子方程式是
(5)已知:2Fe2++Br2=2Fe3++2Br-.若将0.1mol E通入100mL FeBr2溶液中,溶液中有三分之一的Br-被氧化成Br2,则此反应离子方程式是
查看习题详情和答案>>

(1)C的电子式是


(2)反应II的离子方程式是
2Cl-+2H2O
2OH-+H2↑+Cl2↑
| ||
2Cl-+2H2O
2OH-+H2↑+Cl2↑
.
| ||
(3)J久置后,即便不接触水、空气,本身也逐渐分解生成K,并放出气体,该反应的化学方程式是
Ca(ClO)2═CaCl2+O2↑
Ca(ClO)2═CaCl2+O2↑
.(4)工业上测定反应III产品的有效成分J的含量,先将一定量的产品的溶液加入过量的KI溶液和稀硫酸中,使之反应生成I2,然后用Na2S2O3标准溶液滴定I2,计算出结果.
①用Na2S2O3标准溶液滴定I2时选用的指示剂是
淀粉
淀粉
.②生成I2的反应的离子方程式是
ClO-+2I-+2H+=Cl-+I2+H2O
ClO-+2I-+2H+=Cl-+I2+H2O
.(5)已知:2Fe2++Br2=2Fe3++2Br-.若将0.1mol E通入100mL FeBr2溶液中,溶液中有三分之一的Br-被氧化成Br2,则此反应离子方程式是
6Fe2++4Br-+5Cl25Cl2-═6Fe3++2Br2+10Cl-
6Fe2++4Br-+5Cl25Cl2-═6Fe3++2Br2+10Cl-
,原FeBr2溶液的物质的量浓度为1.2 mol/L
1.2 mol/L
.(2012?长宁区二模)将一定量的H2、CO和CO2的混合气体通入盛有足量Na2O2粉末(Na2O2体积忽略不计)的密闭容器中,用电火花引燃直至反应完全.恢复到原温度,容器内的压强为原来的
,则原混合气体的平均相对分子质量不可能是( )
| 1 |
| 4 |
查看习题详情和答案>>
将一定量的SO2和含0.7mol氧气的空气(忽略CO2)放入一定体积的密闭容器中,550℃时,在催化剂作用下发生反应:2SO2+O2
2SO3(正反应放热).反应达到平衡时,将容器中的混合气体通过过量NaOH溶液,气体体积减少了21.28L;再将剩余气体通过一种碱性溶液吸收O2,气体的体积又减少了5.6L(以上气体体积均为标准状况下的体积).
(1)判断该反应达到平衡状态的标志是
a.SO2和SO3浓度相等 b.SO2百分含量保持不变
c.容器中气体的压强不变 d.SO3的生成速率与SO2的消耗速率相等
e.容器中混合气体的密度保持不变
(2)欲提高SO2的转化率,下列措施可行的是
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.升高温度
(3)该反应达到平衡时SO2的转化率为
查看习题详情和答案>>
| 催化剂 | 加热 |
(1)判断该反应达到平衡状态的标志是
bc
bc
(填字母)a.SO2和SO3浓度相等 b.SO2百分含量保持不变
c.容器中气体的压强不变 d.SO3的生成速率与SO2的消耗速率相等
e.容器中混合气体的密度保持不变
(2)欲提高SO2的转化率,下列措施可行的是
b
b
(填字母)a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.升高温度
(3)该反应达到平衡时SO2的转化率为
94.7%
94.7%
(用百分数表示).