摘要:4.下列叙述正确的是( ) A.95℃纯水的pH<7.说明加热可导致水呈酸性 B.pH=3的醋酸溶液.稀释至10倍后pH=4 C.0.2mol/L的盐酸.与等体积水混合后pH=1 D.pH=3的醋酸溶液.与pH=11的氢氧化钠溶液等体积混合后pH=7 答案:C 考点:本题考查了电离平衡移动以及酸碱中和后溶液pH的变化规律. 解析:水的电离与温度有关.温度越高.电离度越大.但[H+]=[OH-]水仍呈中性.A错,我们知道pH每升高一个单位.对于强酸需要稀释10倍.而对于弱酸稀释的倍数超过了10倍.B中由于醋酸为弱酸.稀释至原来的10倍后.pH<4.B错,在D中.当酸与碱的pH之和等于14时.等体积混合后.谁弱显谁性.即pH<7.D错.
网址:http://m.1010jiajiao.com/timu_id_4403008[举报]
(2007,海南,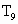 )由海水制备无水氯化镁,主要有以下步骤:①在一定条件下脱水干燥;②加熟石灰;③加盐酸;④过滤;⑤浓缩结晶。其先后顺序正确的是
)由海水制备无水氯化镁,主要有以下步骤:①在一定条件下脱水干燥;②加熟石灰;③加盐酸;④过滤;⑤浓缩结晶。其先后顺序正确的是
[ ]
|
A.②④⑤③① |
B.③②④①⑤ |
|
C.③④②⑤① |
D.②④③⑤① |