摘要:52.在抗日义勇军基础上建立起来的东北抗日武装力量的核心是 A. 东北军 B.八路军 C.新四军 D.抗日联军
网址:http://m.1010jiajiao.com/timu_id_4401251[举报]
甲、乙两同学为探究SO2与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验)
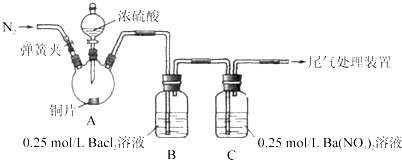
实验操作和现象:(BaCl2提示:A中产生的白雾,是H2SO4的酸雾)
(1)A中反应的化学方程式是
(2)C中白色沉淀是
(3)C中液面上方生成浅棕色气体的化学方程式是
(4)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应.
①为证实各自的观点,在原实验基础上:
甲在原有操作之前增加一步操作,该操作是
乙在A、B间增加洗气瓶D,D中盛放的试剂是足量饱和NaHSO3溶液.其目的是
②甲、乙分别进行实验,B中现象:
检验白色沉淀,发现均不溶于稀盐酸.结合离子方程式解释白色沉淀产生原因:
甲:
(5)合并(4)中两同学的方案进行试验.B中无沉淀生成,而C中产生白色沉淀,由此得出的结论是
查看习题详情和答案>>

实验操作和现象:(BaCl2提示:A中产生的白雾,是H2SO4的酸雾)
| 操作 | 现象 |
| 关闭弹簧夹,滴加一定量浓硫酸,加热 | A中有白雾生成,铜片表面产生气泡 B中有气泡冒出,产生大量白色沉淀 C中产生白色沉淀,液面上方略显浅棕色并逐渐消失 |
| 打开弹簧夹,通入N2,停止加热,一段时间后关闭 | |
| 从B、C中分别取少量白色沉淀,加稀盐酸 | 均未发现白色沉淀溶解 |
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
| ||
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
.
| ||
(2)C中白色沉淀是
BaSO4
BaSO4
,该沉淀的生成表明SO2具有还原
还原
性.(3)C中液面上方生成浅棕色气体的化学方程式是
2NO+O2=2NO2
2NO+O2=2NO2
.(4)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应.
①为证实各自的观点,在原实验基础上:
甲在原有操作之前增加一步操作,该操作是
通N2一段时间,排除装置的空气
通N2一段时间,排除装置的空气
;乙在A、B间增加洗气瓶D,D中盛放的试剂是足量饱和NaHSO3溶液.其目的是
吸收H2SO4酸雾
吸收H2SO4酸雾
.②甲、乙分别进行实验,B中现象:
| 甲 | 大量白色沉淀 |
| 乙 | 少量白色沉淀 |
甲:
SO42-+Ba2+=BaSO4↓
SO42-+Ba2+=BaSO4↓
;乙:2Ba2++2SO2+O2+2H2O=2BaSO4+4H+
2Ba2++2SO2+O2+2H2O=2BaSO4+4H+
.(5)合并(4)中两同学的方案进行试验.B中无沉淀生成,而C中产生白色沉淀,由此得出的结论是
SO2与可溶性钡的强酸盐不能反应生成BaSO3沉淀
SO2与可溶性钡的强酸盐不能反应生成BaSO3沉淀
.喷泉是一种常见的现象,其产生的原因是存在压强差.
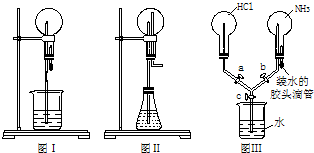
(1)图Ⅰ为化学教学中常用的喷泉实验装置.在烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体.下列组合中不可能形成喷泉的是
A. SO2和H2O B.CO2和NaOH溶液 C.NH3和H2O D.NO和H2O
(2)在图Ⅱ的锥形瓶中,分别加入足量的下列物质后,能产生喷泉的是
A.Cu与稀硫酸 B.Cu与稀硝酸 C.Al与浓硫酸 D.Fe与浓硝酸
(3)比较图Ⅰ和图Ⅱ两套装置,从产生喷泉的原理来分析,图Ⅰ是
(4)某学生积极思考喷泉原理的应用,设计了如图Ⅲ所示的装置.
①如果关闭活塞c,打开活塞a、b,再挤压胶头滴管.则可能出现的现象为
②在①操作的基础上,打开活塞c,产生的现象是
查看习题详情和答案>>

(1)图Ⅰ为化学教学中常用的喷泉实验装置.在烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体.下列组合中不可能形成喷泉的是
D
D
A. SO2和H2O B.CO2和NaOH溶液 C.NH3和H2O D.NO和H2O
(2)在图Ⅱ的锥形瓶中,分别加入足量的下列物质后,能产生喷泉的是
B
B
A.Cu与稀硫酸 B.Cu与稀硝酸 C.Al与浓硫酸 D.Fe与浓硝酸
(3)比较图Ⅰ和图Ⅱ两套装置,从产生喷泉的原理来分析,图Ⅰ是
减小
减小
上部烧瓶内气体压强;图Ⅱ是增大
增大
下部锥形瓶内气体压强(填“增大”或“减小”).(4)某学生积极思考喷泉原理的应用,设计了如图Ⅲ所示的装置.
①如果关闭活塞c,打开活塞a、b,再挤压胶头滴管.则可能出现的现象为
HCl气体进入到盛有NH3的集气瓶,产生大量的白烟
HCl气体进入到盛有NH3的集气瓶,产生大量的白烟
.②在①操作的基础上,打开活塞c,产生的现象是
①②两烧瓶同时产生喷泉
①②两烧瓶同时产生喷泉
. (I)Li-SOCl2电池可用于心脏起搏器.该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2.电池的总反应可表示为:4Li+2SOCl2=4LiCl+S+SO2.
(I)Li-SOCl2电池可用于心脏起搏器.该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2.电池的总反应可表示为:4Li+2SOCl2=4LiCl+S+SO2.请回答下列问题:
(1)电池的负极材料为
(2)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成. 如果把少量水滴到SOCl2中,实验现象是
(3)组装该电池必须在无水、无氧的条件下进行,原因是
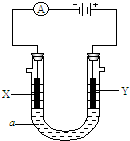
(Ⅱ)电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
(1).如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:①X的电极反应式是
(2).在图的基础上,用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得溶液中加入0.1molCu(OH)2后恰好恢复到电解前的浓度和pH.则电解过程中转移的电子数为
同学们为探究Na2SO3和SO2有关性质进了相关的实验(已知:H2S是一种酸性气体,且具有很强的还原性).
(1)取一定量没有变质纯净的Na2SO3?7H2O晶体,经600℃以上的强热至恒重,通过分析及计算表明,恒重后的样品质量恰好等于无水亚硫酸钠质量的计算值,而且各元素的组成也同样与亚硫酸钠组成符合.但将加热恒重后的样品溶于水,却发现溶液的碱性大大高于亚硫酸钠溶液的期望值.经过仔细思考,同学们提出了对这种反常现象的合理解析.
①你对这结论的解释是(用化学方程式表达) ;
②请设计相应的实验方案,验证以上的解释.(只要求写出实验设计的原理和判断结论,不要求具体的实验操作) .
(2)为探究SO2与氯化钡溶液能否生成白色BaSO3沉淀,甲、乙两同学共同设计了下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验).关闭装置A中弹簧夹,滴加一定量浓硫酸,加热,A中有白雾生成,铜片表面产生气泡,B中有气泡冒出,产生大量白色沉淀,C中产生白色沉淀,液面上方略显浅棕色并逐渐消失.打开弹簧夹,通入N2,停止加热,一段时间后关闭.从B、C中分别取少量白色沉淀,加稀盐酸,均未发现白色沉淀溶解.

①写出构成装置A的玻璃仪器的名称 .
②A中发生反应的化学方程式是 .
③生成C中白色沉淀的离子方程式 .
④分析B中不溶于稀盐酸的沉淀产生的原因,请你提出合理的解释(只要求讲出一种情况) .为证实你自己的观点,只要在原实验基础上,再多进行一步实验操作,该操作是 .
⑤通过本实验探究,可以得出的结论是 .
查看习题详情和答案>>
(1)取一定量没有变质纯净的Na2SO3?7H2O晶体,经600℃以上的强热至恒重,通过分析及计算表明,恒重后的样品质量恰好等于无水亚硫酸钠质量的计算值,而且各元素的组成也同样与亚硫酸钠组成符合.但将加热恒重后的样品溶于水,却发现溶液的碱性大大高于亚硫酸钠溶液的期望值.经过仔细思考,同学们提出了对这种反常现象的合理解析.
①你对这结论的解释是(用化学方程式表达)
②请设计相应的实验方案,验证以上的解释.(只要求写出实验设计的原理和判断结论,不要求具体的实验操作)
(2)为探究SO2与氯化钡溶液能否生成白色BaSO3沉淀,甲、乙两同学共同设计了下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验).关闭装置A中弹簧夹,滴加一定量浓硫酸,加热,A中有白雾生成,铜片表面产生气泡,B中有气泡冒出,产生大量白色沉淀,C中产生白色沉淀,液面上方略显浅棕色并逐渐消失.打开弹簧夹,通入N2,停止加热,一段时间后关闭.从B、C中分别取少量白色沉淀,加稀盐酸,均未发现白色沉淀溶解.

①写出构成装置A的玻璃仪器的名称
②A中发生反应的化学方程式是
③生成C中白色沉淀的离子方程式
④分析B中不溶于稀盐酸的沉淀产生的原因,请你提出合理的解释(只要求讲出一种情况)
⑤通过本实验探究,可以得出的结论是
(2012?奉贤区二模)为探究SO2与可溶性钡盐能否反应生成白色BaSO3沉淀,甲、乙两同学用下图所示装置进行实验(夹持装置、加热装置已略,气密性已检验)
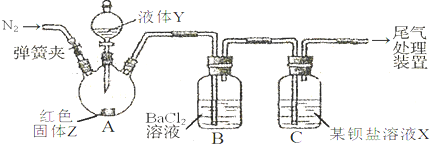
实验操作和现象:
(1)A中反应的化学方程式是
(2)C中可溶性钡盐溶液X为
(3)分析B中不溶于稀盐酸的沉淀的产生原因,甲同学认为是
甲、乙各自进行实验,B中现象分别如下表:由此得出的结论是
(4)丙将甲乙两同学的方案进行联合试验,发现B中无沉淀生成,而C中产生白色沉淀,但无红棕色气体.C中反应的化学方程式是
(5)丁同学认为丙选择的两种钡盐比较相似,于是丁在丙的基础上将B、C中的钡盐分别换成过量新制的醋酸钡溶液、Ba(AlO2)2溶液,发现B、C中均立即产生大量白色沉淀,该沉淀可溶于稀盐酸,并产生能使澄清石灰水浑浊的气体.C中沉淀为
(6)结合实验目的,根据四位同学的实验操作和实验现象,你得出的结论是
查看习题详情和答案>>

实验操作和现象:
| 操 作 | 现 象 |
| 关闭弹簧夹,滴加一定量液体Y,加强热; | A中有白雾生成,红色固体Z的表面产生气泡.B中有气泡冒出,产生大量白色沉淀.C中产生白色沉淀,液面上方略显红棕色并逐渐消失. |
| 打开弹簧夹,通入气体N2,停止加热,一段时间后关闭; | |
| 从B、C中分别取少量白色沉淀,加稀盐酸. | 均未发现白色沉淀溶解 |
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
| ||
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
.
| ||
(2)C中可溶性钡盐溶液X为
硝酸钡
硝酸钡
.实验过程中,发现液体Y不能很顺利地滴下,则可如何改进:将分液漏斗改为恒压漏斗
将分液漏斗改为恒压漏斗
.(3)分析B中不溶于稀盐酸的沉淀的产生原因,甲同学认为是
空气参与了反应
空气参与了反应
,乙同学认为是白雾参与反应.为证实各自的观点,在原实验基础上;甲同学在原有操作之前,先通N2一段时间.乙同学则在A、B间增加盛有饱和NaHSO3溶液的洗气瓶D.甲、乙各自进行实验,B中现象分别如下表:由此得出的结论是
空气、白雾均是产生白色沉淀的原因,白雾是主要原因
空气、白雾均是产生白色沉淀的原因,白雾是主要原因
.| 甲 | 大量不溶于稀盐酸的白色沉定 |
| 乙 | 少量不溶于稀盐酸的白色沉淀 |
3SO2+2H2O+3Ba(NO3)2═3BaSO4↓+2NO↑+4HNO3
3SO2+2H2O+3Ba(NO3)2═3BaSO4↓+2NO↑+4HNO3
.(5)丁同学认为丙选择的两种钡盐比较相似,于是丁在丙的基础上将B、C中的钡盐分别换成过量新制的醋酸钡溶液、Ba(AlO2)2溶液,发现B、C中均立即产生大量白色沉淀,该沉淀可溶于稀盐酸,并产生能使澄清石灰水浑浊的气体.C中沉淀为
BaSO3、氢氧化铝
BaSO3、氢氧化铝
.实验室里欲获得该沉淀,所需要的玻璃仪器是烧杯、漏斗、玻璃棒
烧杯、漏斗、玻璃棒
.(6)结合实验目的,根据四位同学的实验操作和实验现象,你得出的结论是
SO2与可溶性钡的强酸盐不能反应生成BaSO3沉淀,SO2与可溶性钡的弱酸盐能反应生成BaSO3沉淀
SO2与可溶性钡的强酸盐不能反应生成BaSO3沉淀,SO2与可溶性钡的弱酸盐能反应生成BaSO3沉淀
.