网址:http://m.1010jiajiao.com/timu_id_435333[举报]
选择题答案
题号
1
2
3
4
5
6
7
8
9
10
答案
D
D
B
D
C
C
D
D
C
C
题号
11
12
13
14
15
16
17
18
19
20
答案
C
A
D
A
C
C
B
A
D
A
21(5分). (1) (2分) ① ④ (每空1分)
(2)(3分)
1 Na2Cr2O7+ 6 KI+ 14 HCl→ 2 CrCl3+2 NaCl+ 6 KCl+ 3 I2+ 7 H2O (2分)
电子转移(略) (1分)
22(6分)、(1) Cl2 Ca(OH)2 (2分)
(2)MnO2+4H++2Cl-=Mn2++Cl2+2H2O (2分)
(3)C+2H2SO4(浓)=CO2+SO2+2H2O (2分)
23(9分)、(1)A:碳(或C)(1分) C:钠(或Na)(1分)
(2) Na2S电子式(略) (1分) 离子键和非极性键(2分)
(3)2CO2+2Na2O2=2Na2CO3+O2 (2分)
(4)Na2O2+S2-+2H2O=4OH-+S↓+2Na+ (2分)
24(8分)、KAl(SO4)2?12H2O BaSO4 NaAlO2 AlCl3(每空1分,共4分)
(1)(2分)Al3++3H2O A(OH)3+3H+(2)(2分)Al(OH)3+OH-=AlO2-+2H2O
A(OH)3+3H+(2)(2分)Al(OH)3+OH-=AlO2-+2H2O
25.(14分)(1)(3分)1:2 (1分) 使氧气过量,提高SO2的转化率(2分)
(2)(3分)该反应是放热的可逆反应,温度过高平衡逆向移动,不利于 的生成,且影响催化剂的活性。
的生成,且影响催化剂的活性。
(3)(3分)向锥形瓶中滴加 溶液,直至沉淀量不再增加(或静置后向上层清液中滴入
溶液,直至沉淀量不再增加(或静置后向上层清液中滴入 溶液,若产生沉淀,继续加入
溶液,若产生沉淀,继续加入 溶液后,重复上述过程至清液中不再产生沉淀)(2分) c(1分)
溶液后,重复上述过程至清液中不再产生沉淀)(2分) c(1分)
(4)(5分)
a d (2分) 
26.(8分)(1)①6 ②MgCO3和NaHCO3;KHCO3和CaC03(2)0.200 (每空2分)
(1)实验前,必须进行的操作是(填操作名称,不必写具体过程)
(2)在A装置中加入Na2SO3固体的同时,还需加几滴水,然后再滴加浓硫酸.加几滴水的作用是
(3)小试管C的作用是
(4)广口瓶D内盛的试剂是浓硫酸,装置D的三个作用是:
①
②
③
(5)实验中当Cr2O3表面红热时,应将酒精灯移开一会儿再加热,以防温度过高,这样做的原因是
(6)装置G的作用是
(7)从G装置导出的尾气处理方法是
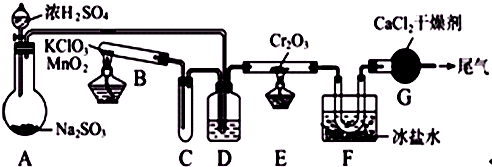
实验室中根据2SO2+O2![]() 2SO3;ΔH=-196.6 kJ?mol-1设计如图所示实验装置来制备SO3固体。请完成下列问题:
2SO3;ΔH=-196.6 kJ?mol-1设计如图所示实验装置来制备SO3固体。请完成下列问题:

(1)实验前,必须进行的操作是(填操作名称,不必写具体过程)____________________。
(2)在A装置中加入Na2SO3固体的同时,还需加几滴水,然后再滴加浓硫酸。加几滴水的作用是______________________________________________________________________。
(3)小试管C的作用是______________________________________________________。
(4)广口瓶D内盛的试剂是__________________________________________________。
装置D的三个作用是:
①_________________________________________________________________;
②_________________________________________________________________;
③_________________________________________________________________。
(5)实验中当Cr2O3表面红热时,应将酒精灯移开一会儿再加热,以防温度过高,这样做的原因是________________________________。
(6)装置F中U形管内收集到的物质的颜色、状态是____________。
(7)装置G的作用是________________________________________。
(8)从G装置导出的尾气处理方法是________________________________________。
查看习题详情和答案>>(1)提出假设:A是FeCl3,B是FeCl2.
(2)设计实验方案:
分别取A、B的溶液均进行以下实验,但实验现象相同.请填写下表中的相应空格.
| 实验方法 | 实验现象 | 结 论 |
| 分别向A、B溶液中加 KSCN溶液 |
固体物质中有FeCl3 | |
| 分别向KMnO4溶液中 加适量A、B溶液 |
KMnO4溶液颜色无明显变化 | 固体物质中不含 |
(4)为进一步探究FeCl3溶液的性质,他又利用A溶液做了如下一些实验,其中明显错误的是:
A.将A溶液滴入沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔现象
B.向A溶液中加入少量铁粉,铁粉溶解,溶液颜色加深
C.在A溶液中滴加NaOH浓溶液,出现红褐色沉淀
D.将A溶液加热蒸干并灼烧,得到FeCl3固体
(5)实际应用:
①半导体、多媒体行业要用FeCl3溶液做印刷电路铜板腐蚀剂,请写出FeCl3溶液腐蚀印刷电路铜板的离子方程式:
②腐蚀铜板后的混合溶液中,若Cu2+和Fe3+的浓度均为0.1mol/L,则溶液中Fe2+的浓度为
③请参照下表给出的数据和药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤:
| 氢氧化物 开始沉淀时的pH |
氢氧化物 沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Cu2+ | 4.7 | 6.7 |
| 提供的药品:Cl2、浓H2SO4、NaOH溶液、CuO、Cu | ||
有关反应的化学方程式
类比是化学学习中常用的方法之一,已知硝酸能把铁氧化成Fe(NO3)3,但当铁过量时,产物是Fe(NO3)2.某同学受此启发,提出一个相似的观点:氯气与铁粉反应,当Cl2足量时生成FeCl3,当铁粉过量时产物是FeCl2.为验证此观点是否正确,该同学将一根细的纯铁丝分别在足量和少量的Cl2中点燃,取其表面生成物并分别编号为A、B,然后通过实验确定其成分.探究过程如下:
(1)提出假设:A是FeCl3,B是FeCl2.
(2)设计实验方案:分别取A、B的溶液均进行以下实验,但实验现象相同.请填写下表中的相应空格
| 实验方法 | 实验现象 | 结论 |
| 分别向A、B溶液中加KSCN溶液 | ______ | 固体物质中FeCl3 |
| 分别向KMnO4溶液中加入适量A、B溶液 | KMnO4溶液颜色无明显变化 | 固体物质中不含______ |
(4)为进一步探究FeCl3溶液的性质,他又利用A溶液做了如下一些实验,其中明显错误的是______ (填写序号).
A.将A溶液滴入淀粉碘化钾溶液中,可得到蓝色液体,该液体能产生丁达尔现象
B.向A溶液中加入少量铁粉,铁粉溶解,溶液颜色加深
C.在A溶液中滴加NaOH浓溶液,出现红褐色沉淀
D.将A溶液加热蒸干并灼烧,得到FeCl3固体
(5)FeCl3溶液常作印刷电路铜板腐蚀剂,写出反应的离子方程式______.腐蚀后的废液中含有FeCl2、FeCl3、CuCl2,某研究性学习小组的同学们设计了两种从废液中回收Cu的方案:
方案1:向废液中加入过量的铁粉,充分反应后,过滤.在所得滤渣中加入足量的盐酸,充分反应后,再过滤即得到铜,该方案中涉及的四种阳离子的氧化性由强到弱的顺序为:______.
方案2:在废液中加入适量的盐酸调节溶液的pH=1,用铜和石墨作电极进行电解,当观察到阴极上有少量气泡产生时,即停止电解,这时要回收的Cu已全部析出.该方案中铜作______极,该电极上所发生的电极反应为 (若有多个电极反应,请全部写出)______.方案2在电极上直接回收铜,操作上比方案1简便,但方案2也有不足之处,主要表现为:______. 查看习题详情和答案>>
(1)提出假设:A是FeCl3,B是FeCl2.
(2)设计实验方案:分别取A、B的溶液均进行以下实验,但实验现象相同.请填写下表中的相应空格
| 实验方法 | 实验现象 | 结论 |
| 分别向A、B溶液中加KSCN溶液 | ______ | 固体物质中FeCl3 |
| 分别向KMnO4溶液中加入适量A、B溶液 | KMnO4溶液颜色无明显变化 | 固体物质中不含______ |
(4)为进一步探究FeCl3溶液的性质,他又利用A溶液做了如下一些实验,其中明显错误的是______ (填写序号).
A.将A溶液滴入淀粉碘化钾溶液中,可得到蓝色液体,该液体能产生丁达尔现象
B.向A溶液中加入少量铁粉,铁粉溶解,溶液颜色加深
C.在A溶液中滴加NaOH浓溶液,出现红褐色沉淀
D.将A溶液加热蒸干并灼烧,得到FeCl3固体
(5)FeCl3溶液常作印刷电路铜板腐蚀剂,写出反应的离子方程式______.腐蚀后的废液中含有FeCl2、FeCl3、CuCl2,某研究性学习小组的同学们设计了两种从废液中回收Cu的方案:
方案1:向废液中加入过量的铁粉,充分反应后,过滤.在所得滤渣中加入足量的盐酸,充分反应后,再过滤即得到铜,该方案中涉及的四种阳离子的氧化性由强到弱的顺序为:______.
方案2:在废液中加入适量的盐酸调节溶液的pH=1,用铜和石墨作电极进行电解,当观察到阴极上有少量气泡产生时,即停止电解,这时要回收的Cu已全部析出.该方案中铜作______极,该电极上所发生的电极反应为 (若有多个电极反应,请全部写出)______.方案2在电极上直接回收铜,操作上比方案1简便,但方案2也有不足之处,主要表现为:______.