网址:http://m.1010jiajiao.com/timu_id_43106[举报]
1、C 2、A 3、B 4、D 5、C
30、(22分,每空2分)
(1)基因突变可以产生新的等位基因(2分)
(2)显性(2分) 该雌果蝇与纯种黑身雄果蝇杂交,子代中雌雄个体均既有灰身,又有黑身。(2分)
(3)不能,因为无论控制体色的基因位于常染色体还是X染色体上其后代均有两种表现型,每种表现型的性别比例均为1:1,故不能确定。(4分)
(4)方案1:选取F1中的黑身雌果蝇和灰身雄果蝇杂交,(2分)若子代中雄性个体全为黑身,雌性个体全为灰身,则突变基因位于X染色体上;若子代中雌雄个体都既有灰身又有黑身,则空变基因位于常染色体上。(4分)
(方案2:选取F1中的灰身雌果蝇和灰身雄果蝇杂交,(2分)若子代中雄性个体既有黑身又有灰身,雌性个体全为灰身,则突变基因位于X染色体上;若子代雌雄个体既有灰身又有黑身,则突变基因位于常染色体上。)(4分)
(5)①截毛 刚毛 (2分) ②刚毛 截毛(4分)
31. (20分)
(1)水 (2分)
(2)种群密度(2分)
(3)75 (2分) 0.6 (2分)
(4)第二步:一只孤立性蝗虫2置于开放的黑色玻璃容器中,容器外放置孤立性蝗虫4(使蝗虫不能相互看到) (2分)
预期实验结果及结论:
②A与B均不表现出较明显的合群化行为,证明视觉、嗅觉两种刺激都不是有效的合群化触发机制。(2分)
③A表现出较明显的合群化行为,B不表现出较明显的合群化行为,证明视觉是较嗅觉刺激更为有效的合群化触发机制 (2分)
④A不表现出较明显的合群化行为,B表现出较明显的合群化行为,证明嗅觉是较视觉刺激更为有效的合群化触发机制 (2分)
问题:不能(2分)。
缺乏雄性实验组,缺乏重复实验(2分) (即应反复做相同实验并能得到相同的结论)
《化学部分》参考答案
6、C 7、C 8、A 9、B 10、C 11、B 12、D 13、A
26。(14分)(每空2分)
试题及答案%20.files/image052.jpg) |
(1) ; 极性和非极性
(2)Si+2OH-+H2O=SiO32-+2H2↑
(3) NH3 、 NH3+H3O+=NH4++H2O
(4)2H2O+O2+4e-=4OH-
(5)90%
27.(16分)(每空3分)
(1)第三周期(1分) VIIA族(1分) AlCl3 (1分) 分子(1分)
(2)2Al+2OH-+2H2O=2AlO2-+3H2↑(3分)
(3)H2S+Cl2=2HCl+S ↓(3分) Al2S3+6H2O=2Al(OH)3↓+3H2S↑(3分)
(4)
28.(16分,每空2分)
(Ⅰ) (1)C26H26 (2)16.25mol
试题及答案%20.files/image054.jpg) |
(Ⅱ)
(2)氢氧化钠溶液 浓硫酸,加热
试题及答案%20.files/image056.jpg) |
(4)②⑥⑦。(全对才给分)
29.(14分,每空2分)
(1)分液漏斗
(2)Cl2+SO2+2H2O=4H++2Cl-+SO试题及答案%20.files/image058.gif)
(3)红色鲜花褪色 吸收未反应的氯气等有毒气体
(4)61.0%
(5)偏低
(6)D
《物理部分》参考答案
14.B 15.A 16.ACD 17.BC 18.D 19.B 20.A 21.A
22.(18分)
(1)①A点离桌面的高度h1;出口到地面O点的高度h2;球的落地点P到O点的距离s.
(3分)
②s2=4h1h2 (3分)
(2)对于甲图不合理之处:①不能多次测量;②超过电流表量程不安全;③电压表量程太大,读数误差较大。 (2分)
对于乙图不合理之处:①电流表量程太小;②电压表量程太大;③电丈夫调节范围太小。 (2分)
较为合理的电路图如图所示。 (4分)
Rx的计算公式:Rx=UR0/I (2分)
其中U是电压表V1表示,I是电流表A1示数,R0是电阻箱示数。 (2分)
试题及答案%20.files/image060.gif) |
23.(16分)
(1)设跳离跳台时运动员的速度为v,规定向上为正方向,则由运动学公式有
试题及答案%20.files/image062.gif) ① (4分)
① (4分)
解得:试题及答案%20.files/image064.gif) ② (2分)
② (2分)
(2)设手触及水面时,运动员的速度为试题及答案%20.files/image066.gif) ,
,
试题及答案%20.files/image068.gif) ③ (4分)
③ (4分)
在入水至重心速度减为零的过程中设水对运动的平均阻力为f,由动能定理得:
试题及答案%20.files/image070.gif) ④ (4分)
④ (4分)
解得:试题及答案%20.files/image072.gif) ⑤ (2分)
⑤ (2分)
24.(18分)
(1)C与A碰撞由动量守恒定律有:mCv=(mc+mA)v1 (2分)
v1=mcv/(mC+mA)=
C与A碰撞损失的机械能为:E损=mCv2/2-(mC+mA)v12/2=6J (4分)
(2)当C、A共同运动至速度为零时,弹簧有最大弹性势能,则:
Epm=(mC+mA)v12/2=12J (4分)
(3)B离开墙时,A、C速度仍为v1,方向向左;以后,当C、A与B有共同速度v2,弹簧有最大弹性势能EP’,则:(mC+mA)v1=(mC+mA+mB)v2 (3分)
EP’=(mc+mA)v12/2-(mC+mA+mB)v22/2=3J (4分)
25.(20分)
(1)试题及答案%20.files/image074.gif) (2分)
(2分)
试题及答案%20.files/image076.gif) (2分)
(2分)
试题及答案%20.files/image078.gif) (2分)
(2分)
射出电场后做匀速直线运动,则在磁场中的速度为2.5×
(2)与速度x轴的夹角试题及答案%20.files/image080.gif)
经过电场的偏距试题及答案%20.files/image082.gif) (2分)
(2分)
故有试题及答案%20.files/image084.gif) (2分)
(2分)
(3)作出粒子在磁场中的运动轨迹,如图
则试题及答案%20.files/image086.gif) (3分)
(3分)
因为试题及答案%20.files/image088.gif)
解得试题及答案%20.files/image090.gif) (2分)
(2分)
根据试题及答案%20.files/image092.gif) (3分)
(3分)
试题及答案%20.files/image094.jpg)
K2Cr2O7。实验室对含铬废液(含有Cr3+、Fe3+、K+、SO42-、NO3-和少量Cr2O72-)回收与再利用工艺如下:
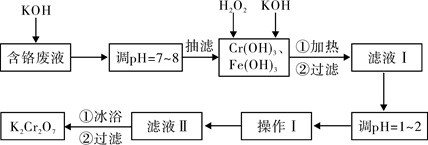
已知:①Cr(OH)3+OH-=CrO2-+2H2O;
②2CrO2-+3H2O2+2OH-=2CrO42-+4H2O;
③H2O2在酸性条件下具有还原性,能将+6价Cr还原为+3价Cr。
(1)实验中所用KOH浓度为6 mol·L-1,现用KOH固体配制250mL 6 mol·L-1 的KOH溶液,除烧杯、玻璃棒外,还必需用到的玻璃仪器有 。
(2)由于含铬废液中含有少量的K2Cr2O7,抽滤时可用 代替布氏漏斗;抽滤过程
中要及时观察吸滤瓶内液面高度,当快达到支管口位置时应进行的操作为 。
(3)滤液Ⅰ酸化前,进行加热的目的是 。冰浴、过滤后,应用少量冷水洗涤K2Cr2O7,其目的是 。
(4)下表是相关物质的溶解度数据:
| 物质 | 0℃ | 20℃ | 40℃ | 60℃ | 80℃ | 100℃ |
| KCl | 28.0 | 34.2 | 40.1 | 45.8 | 51.3 | 56.3 |
| K2SO4 | 7.4 | 11.1 | 14.8 | 18.2 | 21.4 | 24.1 |
| K2Cr2O7 | 4.7 | 12.3 | 26.3 | 45.6 | 73.0 | 102.0 |
| KNO3 | 13.9 | 31.6 | 61.3 | 106 | 167 | 246.0 |
根据溶解度数据,操作Ⅰ具体操作步骤为① 、② 。
(5)称取产品重铬酸钾试样2.000g配成250mL溶液,取出25.00mL于锥形瓶中,加入10mL 2 mol·L-1H2SO4和足量碘化钠(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200 mol·L-1Na2S2O3标准溶液滴定(I2+2S2O32-=2I-+S4O62-)。
①若实验中共用去Na2S2O3标准溶液30.00mL,所得产品的中重铬酸钾的纯度为 (设整个过程中其它杂质不参与反应)。
②若滴定管在使用前未用Na2S2O3标准溶液润洗,测得的重铬酸钾的纯度将: (填“偏高”、“偏低”或“不变”)。
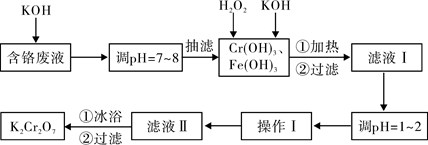
已知:①Cr(OH)3 + OH- ="=" CrO2- + 2H2O;②2CrO2- + 3H2O2 + 2OH- ="=" 2CrO42- + 4H2O;
③H2O2在酸性条件下具有还原性,能将+6价Cr还原为+3价Cr。
(1)实验中所用KOH浓度为6 mol·L-1,现用KOH固体配制250mL 6 mol·L-1 的KOH溶液,除烧杯、玻璃棒外,还必需用到的玻璃仪器有 。
(2)抽滤过程中要及时观察吸滤瓶内液面高度,当快达到支管口位置时应进行的操作为 。
(3)滤液Ⅰ酸化前,进行加热的目的是 。冰浴、过滤后,应用少量冷水洗涤K2Cr2O7,其目的是 。
(4)下表是相关物质的溶解度数据:
| 物质 | 0℃ | 20℃ | 40℃ | 60℃ | 80℃ | 100℃ |
| KCl | 28.0 | 34.2 | 40.1 | 45.8 | 51.3 | 56.3 |
| K2SO4 | 7.4 | 11.1 | 14.8 | 18.2 | 21.4 | 24.1 |
| K2Cr2O7 | 4.7 | 12.3 | 26.3 | 45.6 | 73.0 | 102.0 |
| KNO3 | 13.9 | 31.6 | 61.3 | 106 | 167 | 246.0 |
(5)称取产品重铬酸钾试样2.000g配成250mL溶液,取出25.00mL于锥形瓶中,加入10mL 2mol/LH2SO4和足量碘化钠(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200 mol·L-1Na2S2O3标准溶液滴定(I2+2S2O32-=2I-+S4O62-)。
①若实验中共用去Na2S2O3标准溶液30.00mL,所得产品的中重铬酸钾的纯度为 (设整个过程中其它杂质不参与反应)。
②若滴定管在使用前未用Na2S2O3标准溶液润洗,测得的重铬酸钾的纯度将 (填“偏高”、“偏低”或“不变”)。
(11分)(Ⅰ)下列实验操作或实验叙述正确的是 。
A.可用过滤的方法除去氢氧化铁胶体中少量的氯化铁
B.用酸式滴定管量取18.80mL的碳酸钠溶液
C.配制0.1mol/L的硫酸时,用量筒量取浓硫酸,要洗涤量筒,否则配制的溶液浓度偏低
D.振荡用饱和的碳酸钠溶液吸收乙酸乙酯的试管,发现有气泡冒出,它是CO2气体
E.实验室制取氨气时,常用无水氯化钙进行干燥
F.加入BaCl2溶液有白色沉淀产生,再加稀盐酸,沉淀不消失,一定有SO42-
(Ⅱ)某研究性学习小组将一定浓度的Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀。
甲同学认为沉淀可能是CuCO3; 乙同学认为沉淀可能是Cu(OH)2;
丙同学认为沉淀可能是CuCO3,和Cu(OH)2的混合物。
[查阅资料知:CuCO3和Cu(OH)2均不带结晶水]
(1)按照甲同学的观点,发生反应的离子方程式为______________________ ;在探
究沉淀成分前,须将沉淀从溶液中分离并净化。其具体操作依次为 。
(2)若丙同学的观点正确,可利用下列装置通过实验测定其组成。
①实验装置的连接顺序为_________________________________。
②装置C中碱石灰的作用是__________,实验开始和结束时都要通过量的空气,请说明结束时通入过量空气的作用是__________________________________ 。
③若沉淀样品的质量为mg,装置B质量增加了ng,则沉淀中CuCO3的质量分数为 ______________。
查看习题详情和答案>>
(11分)(Ⅰ)下列实验操作或实验叙述正确的是 。
| A.可用过滤的方法除去氢氧化铁胶体中少量的氯化铁 |
| B.用酸式滴定管量取18.80mL的碳酸钠溶液 |
| C.配制0.1mol/L的硫酸时,用量筒量取浓硫酸,要洗涤量筒,否则配制的溶液浓度偏低 |
| D.振荡用饱和的碳酸钠溶液吸收乙酸乙酯的试管,发现有气泡冒出,它是CO2气体 |
F.加入BaCl2溶液有白色沉淀产生,再加稀盐酸,沉淀不消失,一定有SO42-
(Ⅱ)某研究性学习小组将一定浓度的Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀。
甲同学认为沉淀可能是CuCO3; 乙同学认为沉淀可能是Cu(OH)2;
丙同学认为沉淀可能是CuCO3,和Cu(OH)2的混合物。
[查阅资料知:CuCO3和Cu(OH)2均不带结晶水]
(1)按照甲同学的观点,发生反应的离子方程式为______________________ ;在探究沉淀成分前,须将沉淀从溶液中分离并净化。其具体操作依次为
(2)若丙同学的观点正确,可利用下列装置通过实验测定其组成。

①实验装置的连接顺序为_________________________________。
②装置C中碱石灰的作用是__________,实验开始和结束时都要通过量的空气,请说明结束时通入过量空气的作用是__________________________________ 。
③若沉淀样品的质量为mg,装置B质量增加了ng,则沉淀中CuCO3的质量分数为 ______________。 查看习题详情和答案>>
(11分)(Ⅰ)下列实验操作或实验叙述正确的是 。
A.可用过滤的方法除去氢氧化铁胶体中少量的氯化铁
B.用酸式滴定管量取18.80mL的碳酸钠溶液
C.配制0.1mol/L的硫酸时,用量筒量取浓硫酸,要洗涤量筒,否则配制的溶液浓度偏低
D.振荡用饱和的碳酸钠溶液吸收乙酸乙酯的试管,发现有气泡冒出,它是CO2气 体
E.实验室制取氨气时,常用无水氯化钙进行干燥
F.加入BaCl2溶液有白色沉淀产生,再加稀盐酸,沉淀不消失,一定有SO42-
(Ⅱ)某研究性学习小组将一定浓度的Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀。
甲同学认为沉淀可能是CuCO3; 乙同学认为沉淀可能是Cu(OH)2;
丙同学认为沉淀可能是CuCO3,和Cu(OH)2的混合物。
[查阅资料知:CuCO3和Cu(OH)2均不带结晶水]
(1)按照甲同学的观点,发生反应的离子方程式为______________________ ;在探
究沉淀成分前,须将沉淀从溶液中分离并净化。其具体操作依次为 。
(2)若丙同学的观点正确,可利用下列装置通过实验测定其组成。

①实验装置的连接顺序为_________________________________。
②装置C中碱石灰的作用是__________,实验开始和结束时都要通过量的空气,请说明结束时通入过量空气的作用是__________________________________ 。
③若沉淀样品的质量为mg,装置B质量增加了ng,则沉淀中CuCO3的质量分数为 ______________。
查看习题详情和答案>>