摘要:2Fe(OH)3 == Fe2O3 + 3H2O 2Al(OH)3 == Al2O3 + 3H2O(一).实验用到的气体要求是比较纯净.除去常见杂质具体方法:① 除水蒸气可用:浓流酸.CaCl2固体.碱石灰.无水CuSO4(并且可以检验杂质中有无水蒸气.有则颜色由白色→蓝色).生石灰等② 除CO2可用:澄清石灰水(可检验出杂质中有无CO2).NaOH溶液.KOH溶液.碱石灰等③ 除HCl气体可用:AgNO3溶液(可检验出杂质中有无HCl).石灰水.NaOH溶液.KOH溶液除气体杂质的原则:用某物质吸收杂质或跟杂质反应.但不能吸收或跟有效成份反应.或者生成新的杂质.(二).实验注意的地方:①防爆炸:点燃可燃性气体(如H2.CO.CH4)或用CO.H2还原CuO.Fe2O3之前.要检验气体纯度.②防暴沸:稀释浓硫酸时.将浓硫酸倒入水中.不能把水倒入浓硫酸中.③防中毒:进行有关有毒气体(如:CO.SO2.NO2)的性质实验时.在通风厨中进行,并要注意尾气的处理:CO点燃烧掉,SO2.NO2用碱液吸收.④防倒吸:加热法制取并用排水法收集气体.要注意熄灯顺序.(三).常见意外事故的处理:①酸流到桌上.用NaHCO3冲洗,碱流到桌上.用稀醋酸冲洗.② 沾到皮肤或衣物上:Ⅰ.酸先用水冲洗.再用3 - 5% NaHCO3冲洗,Ⅱ.碱用水冲洗.再涂上硼酸,Ⅲ.浓硫酸应先用抹布擦去.再做第Ⅰ步.(四).实验室制取三大气体中常见的要除的杂质:1.制O2要除的杂质:水蒸气(H2O)2.用盐酸和锌粒制H2要除的杂质:水蒸气(H2O).氯化氢气体3.制CO2要除的杂质:水蒸气(H2O).氯化氢气体(HCl)除水蒸气的试剂:浓流酸.CaCl2固体.碱石灰.生石灰.无水CuSO4(并且可以检验杂质中有无水蒸气.有则颜色由白色→蓝色)等除HCl气体的试剂:AgNO3溶液(并可检验出杂质中有无HCl).澄清石灰水.NaOH溶液.KOH溶液 [生石灰.碱石灰也可以跟HCl气体反应](五).常用实验方法来验证混合气体里含有某种气体1.有CO的验证方法:(先验证混合气体中是否有CO2.有则先除掉)将混合气体通入灼热的CuO.再将经过灼热的CuO的混合气体通入澄清石灰水.现象:黑色CuO变成红色.且澄清石灰水要变浑浊.2.有H2的验证方法:(先验证混合气体中是否有水份.有则先除掉) 将混合气体通入灼热的CuO.再将经过灼热的CuO的混合气体通入盛有无水CuSO4中.现象:黑色CuO变成红色.且无水CuSO4变蓝色.3.有CO2的验证方法:将混合气体通入澄清石灰水.现象:澄清石灰水变浑浊.(六).自设计实验 1. 试设计一个实验证明蜡烛中含有碳氢两种元素.实验步骤实验现象结论①将蜡烛点燃.在火焰上方罩一个干燥洁净的烧杯烧杯内壁有小水珠生成证明蜡烛有氢元素②在蜡烛火焰上方罩一个蘸有澄清石灰水的烧杯澄清石灰水变浑浊证明蜡烛有碳元素2.试设计一个实验来证明CO2具有不支持燃烧和密度比空气大的性质.实验步骤实验现象结论图把两支蜡烛放到具有阶梯的架上.把此架放在烧杯里.点燃蜡烛.再沿烧杯壁倾倒CO2阶梯下层的蜡烛先灭.上层的后灭.证明CO2具有不支持燃烧和密度比空气大的性质
网址:http://m.1010jiajiao.com/timu_id_428608[举报]
(2012?通州区一模)有四种短周期元素,它们的结构、性质等信息如下表所述:
请根据表中信息填写:
(1)X元素在周期表中的位置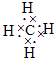
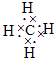 ;
;
(2)工业上制取Y单质常用的方法是
(3)Y离子半径比Z离子的半径
(4)Z的单质和氧化铁反应可用于野外焊接钢轨,写出反应的化学方程式
(5)Z的某种盐是常用的净水剂,用离子方程式表示其净水原理
(6)举出实例说明M的非金属性比X强(用化学方程式表示)
查看习题详情和答案>>
| 元素 | 结构、性质等信息 |
| X | 构成有机物的主角,该元素的一种氧化物和气态氢化物都是典型的温室气体. |
| Y | 短周期中(除稀有气体外)原子半径最大的元素,该单质液态时可用作核反应堆的传热介质. |
| Z | 与Y同周期,其最高价氧化物的水化物呈两性. |
| M | 海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂. |
(1)X元素在周期表中的位置
第二周期第IVA族
第二周期第IVA族
;其气态氢化物的电子式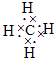
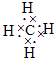
(2)工业上制取Y单质常用的方法是
电解法
电解法
;(3)Y离子半径比Z离子的半径
大
大
(填“小”或“大”);(4)Z的单质和氧化铁反应可用于野外焊接钢轨,写出反应的化学方程式
2Al+Fe2O3
Al2O3+2Fe
| ||
2Al+Fe2O3
Al2O3+2Fe
;
| ||
(5)Z的某种盐是常用的净水剂,用离子方程式表示其净水原理
Al3++3H2O?Al(OH)3(胶体)+3H+
Al3++3H2O?Al(OH)3(胶体)+3H+
;(6)举出实例说明M的非金属性比X强(用化学方程式表示)
Na2CO3+2HClO4=2NaClO4+CO2↑+H2O
Na2CO3+2HClO4=2NaClO4+CO2↑+H2O
.