网址:http://m.1010jiajiao.com/timu_id_428002[举报]
根据以下叙述和元素周期表的有关知识,回答下题:主族元素的性质主要由其原子的最外层电子数和电子层数决定,若元素的最外层电子数为m,电子层数为n,一般具有这样的规律:m>n的元素为非金属元素,m≤n的元素为金属元素。
下列有关推断符合实际的是 ( )
A.第n周期的最后一种金属元素处在第n主族(n>1)
B.m=1与m=7的元素单质相互化合时,都能形成离子化合物
C.第n周期有8-n种非金属元素(n>1,包括稀有气体元素)
D.m-n=5的主族元素存在本周期最强的对应含氧酸
查看习题详情和答案>>
| A、峰值最高的过渡元素在周期表中的位置是第四周期第Ⅷ族 | B、上述元素分析图中,同一周期的两种主族元素可形成1:1型离子化合物只有一种,其电子式为Na+ | C、氯比硫的非金属性强的依据之一是HCl比H2S稳定 | D、工业上常用电解氧化铝的方法制备铝 |
(13分)铁是生活中的常见金属,也是高中所学的过渡元素,由于其结构特点,在与其化物质反应时往往表现出不同的价态。某研究性学习小组对铁和硫反应产物中铁的化合价进行了探究,并设计了以下实验,其实验的步骤为:
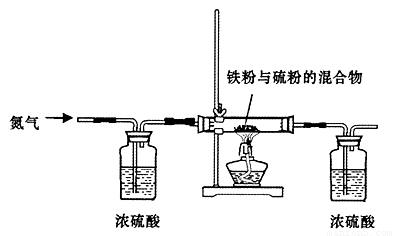
步骤一:将铁粉和硫粉按一定质量比混合,如图所示在氮气环境中,加热后反立即可发生并持续进行,冷却后得到黑色固体。
步骤二:取黑色固体少许,加入浓NaOH溶液并稍稍加热,冷却后过滤,得到黑色滤渣。
在取得黑色滤渣后,同学们经过讨论分析,对其成分提出了各种猜想,其中代表性的为:
猜想一:由于硫和氧是同一主族元素,所以黑色固体的可能是Fe3S4
猜想二:硫和氧虽是同一主族元素,但硫的非金属性弱,则黑色固体为Fe
为了验证以上猜想又进行了以下操作:
步骤三:在滤渣中加入已煮沸的稀硫酸。
步骤四:取步骤三所得溶液少许,……。
请回答下列问题:
(1)查阅资料:实验室可以用氯化铵饱和溶液和亚硝酸钠(NaNO2)饱和溶液混合加热反应得氮气。请写出该反应的离子方程式: 。
(2)实验中通入氮气的作用 。
(3)若猜想一正确,则步骤三应该观察到试管内有 出现(填实验现象)。
(4)若猜想二正确,请完成步骤四的实验操作、现象和结论 。
(5)步骤一中铁粉和硫粉的混合粉末中硫要过量些,其原因是 。
(6)步骤二中加入浓NaOH溶液并稍稍加热的目的是 。
查看习题详情和答案>>
(13分)铁是生活中的常见金属,也是高中所学的过渡元素,由于其结构特点,在与其化物质反应时往往表现出不同的价态。某研究性学习小组对铁和硫反应产物中铁的化合价进行了探究,并设计了以下实验,其实验的步骤为:
步骤一:将铁粉和硫粉按一定质量比混合,如图所示在氮气环境中,加热后反立即可发生并持续进行,冷却后得到黑色固体。
步骤二:取黑色固体少许,加入浓NaOH溶液并稍稍加热,冷却后过滤,得到黑色滤渣。
在取得黑色滤渣后,同学们经过讨论分析,对其成分提出了各种猜想,其中代表性的为:
猜想一:由于硫和氧是同一主族元素,所以黑色固体的可能是Fe3S4
猜想二:硫和氧虽是同一主族元素,但硫的非金属性弱,则黑色固体为Fe
为了验证以上猜想又进行了以下操作:
步骤三:在滤渣中加入已煮沸的稀硫酸。
步骤四:取步骤三所得溶液少许,……。
请回答下列问题:
(1)查阅资料:实验室可以用氯化铵饱和溶液和亚硝酸钠(NaNO2)饱和溶液混合加热反应得氮气。请写出该反应的离子方程式: 。
(2)实验中通入氮气的作用 。
(3)若猜想一正确,则步骤三应该观察到试管内有 出现(填实验现象)。
(4)若猜想二正确,请完成步骤四的实验操作、现象和结论 。
(5)步骤一中铁粉和硫粉的混合粉末中硫要过量些,其原因是 。
(6)步骤二中加入浓NaOH溶液并稍稍加热的目的是 。
查看习题详情和答案>>
(13分)铁是生活中的常见金属,也是高中所学的过渡元素,由于其结构特点,在与其化物质反应时往往表现出不同的价态。某研究性学习小组对铁和硫反应产物中铁的化合价进行了探究,并设计了以下实验,其实验的步骤为: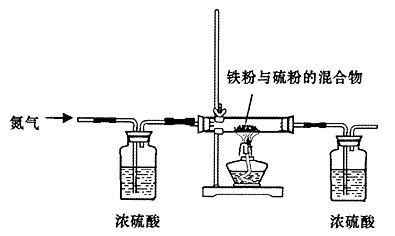
步骤一:将铁粉和硫粉按一定质量比混合,如图所示在氮气环境中,加热后反立即可发生并持续进行,冷却后得到黑色固体。
步骤二:取黑色固体少许,加入浓NaOH溶液并稍稍加热,冷却后过滤,得到黑色滤渣。
在取得黑色滤渣后,同学们经过讨论分析,对其成分提出了各种猜想,其中代表性的为:
猜想一:由于硫和氧是同一主族元素,所以黑色固体的可能是Fe3S4
猜想二:硫和氧虽是同一主族元素,但硫的非金属性弱,则黑色固体为FeS
为了验证以上猜想又进行了以下操作:
步骤三:在滤渣中加入已煮沸的稀硫酸。
步骤四:取步骤三所得溶液少许,……。
请回答下列问题:
(1)查阅资料:实验室可以用氯化铵饱和溶液和亚硝酸钠(NaNO2)饱和溶液混合加热反应得氮气。请写出该反应的离子方程式: 。
(2)实验中通入氮气的作用 。
(3)若猜想一正确,则步骤三应该观察到试管内有 出现(填实验现象)。
(4)若猜想二正确,请完成步骤四的实验操作、现象和结论 。
(5)步骤一中铁粉和硫粉的混合粉末中硫要过量些,其原因是 。
(6)步骤二中加入浓NaOH溶液并稍稍加热的目的是 。