摘要:大茴香醇具有清甜的茴青香气.广泛用于花香型日化香精和可可.香草等食用香精.已知大茴香醇仅由C.H.O三种元素组成.其相对分子质量为138.将0.1mol该醇充分燃烧后.产物依次通过足量的浓H2SO4和NaOH溶液.浓H2SO4增重9g.NaOH溶液增重35.2g.请回答下列问题:⑴该醇的分子式为 .⑵该醇的结构有如下特点:①苯环上一溴代物有两种结构,②分子结构中含有―OCH3.则该醇的结构简式为 .⑶该醇不可能发生的反应类型是 .A.氧化反应 B.消去反应 C.加成反应 ⑷大茴香醇可与醋酸在浓H2SO4存在并加热的条件下发生反应生成酯类香料.试写出该反应的化学方程式: .
网址:http://m.1010jiajiao.com/timu_id_419337[举报]
(2012?和平区一模)已知:(I)B的产量可以用来衡量-个国家的石油化工发展水平.

有机物A是一种香料化合物,其化学性质稳定,香气柔和清雅,具有新鲜苹果和草莓的香气,广泛用于花香型和果香型香精的调配.其合成过程如下:
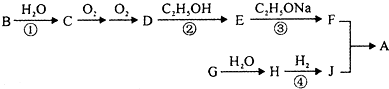
(1)J的相对分子质量为76,不能与NaHCO3溶液反应,1mol J能与足量的Na反应生成1mol H2,J的一氯代物有两种,写出J的结构简式
(2)有机物G中含有一种与B相同的官能团,还能与新制的Cu(OH)2生成红色沉淀,G中的含氧官能团的名称为
(3)写出②的化学反应方程式
(4)反应①、②、④中属于取代反应的是
(5)关于H下列说法正确的是.
a.含有两种不同的官能团
b.能发生银镜反应,与H互为同分异构体的有机物还有一种
c.H可以发生加成反应,消去反应,氧化反应和还原反应
d.H具有弱酸性
(6)E有多种同分异构体.能发生水解反应且能发生银镜反应的同分异构体有
(7)写出制备A的化学方程式:
 .
.
查看习题详情和答案>>

有机物A是一种香料化合物,其化学性质稳定,香气柔和清雅,具有新鲜苹果和草莓的香气,广泛用于花香型和果香型香精的调配.其合成过程如下:

(1)J的相对分子质量为76,不能与NaHCO3溶液反应,1mol J能与足量的Na反应生成1mol H2,J的一氯代物有两种,写出J的结构简式
CH2OHCH2CH2OH
CH2OHCH2CH2OH
.(2)有机物G中含有一种与B相同的官能团,还能与新制的Cu(OH)2生成红色沉淀,G中的含氧官能团的名称为
醛基
醛基
.(3)写出②的化学反应方程式
CH3COOH+C2H5OH
CH3COOC2H5+H2O
| 浓硫酸 |
| △ |
CH3COOH+C2H5OH
CH3COOC2H5+H2O
.| 浓硫酸 |
| △ |
(4)反应①、②、④中属于取代反应的是
②
②
.(5)关于H下列说法正确的是.
a.含有两种不同的官能团
b.能发生银镜反应,与H互为同分异构体的有机物还有一种
c.H可以发生加成反应,消去反应,氧化反应和还原反应
d.H具有弱酸性
(6)E有多种同分异构体.能发生水解反应且能发生银镜反应的同分异构体有
2
2
种,写出其中一种核磁共振氢谱有四个峰,且峰面积之比为1:2:2:3的同分异构体的结构简式HCOOCH2CH2CH3
HCOOCH2CH2CH3
.(7)写出制备A的化学方程式:


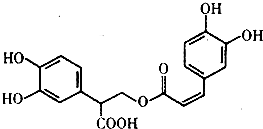 迷迭香酸具有很强的抗氧化性,可用于制备多种药品,也被用于食品防腐.其结构如图.
迷迭香酸具有很强的抗氧化性,可用于制备多种药品,也被用于食品防腐.其结构如图.(1)迷迭香酸在酸性条件下水解生成A和B,A在浓硫酸作用下可发生消去反应生成有机物C.A中的含氧官能团有
a.同系物 b.同分异构体 c.同素异形体 d.同一物质
(2)迷迭香酸在碱性条件下也能发生水解,1mol迷迭香酸最多能和含
(3)B在一定条件下能和H2O反应生成D,D中有四个含氧官能团,且有两个连在同一个碳原子上.
下列物质在一定条件下能与D反应的是
a.H2 b.NaHCO3 c.CH3CH2OH d.CH3COOH
(4)B→D的化学方程式为
(5)B在一定条件下发生加聚反应生成高分子化合物E.E的结构简式是
下列有关物质性质和用途的说法,正确的是( )
| A、光导纤维具有很强的导电能力,所以大量用于制造通信光缆 | B、明矾常用作净水剂,是因为它具有消毒杀菌的作用 | C、氨常用作制冷剂,是因为其沸点极低,很容易液化 | D、SiCl4在战争中常用作烟雾弹,是因为它水解时生成白色烟雾 |
钒具有众多优异的性能,用途十分广泛,有金属“维生素”之称.
完成下列填空:
(1)将废钒催化剂(主要成分V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应,所得溶液显酸性、含VO2+、K+、SO42-等.写出该反应的化学方程式
(2)向上述所得溶液中加入KClO3溶液,充分反应后,溶液中新增加了VO2+、Cl-.写出并配平该反应的离子方程式,并标出电子转移的数目和方向
 .
.
(3)在20.00mL的0.1mol/LVO2+溶液中,加入0.195g锌粉,恰好完成反应,则还原产物可能是
a.V b.V2+ c.VO2+ d.VO2+
(4)已知V2O5能和盐酸反应生成氯气和VO2+.请再写一个离子反应方程式,说明还原性:SO32->Cl->VO2+
查看习题详情和答案>>
完成下列填空:
(1)将废钒催化剂(主要成分V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应,所得溶液显酸性、含VO2+、K+、SO42-等.写出该反应的化学方程式
V2O5+K2SO3+2H2SO4=2VOSO4+K2SO4+2H2O
V2O5+K2SO3+2H2SO4=2VOSO4+K2SO4+2H2O
.(2)向上述所得溶液中加入KClO3溶液,充分反应后,溶液中新增加了VO2+、Cl-.写出并配平该反应的离子方程式,并标出电子转移的数目和方向


(3)在20.00mL的0.1mol/LVO2+溶液中,加入0.195g锌粉,恰好完成反应,则还原产物可能是
b
b
.a.V b.V2+ c.VO2+ d.VO2+
(4)已知V2O5能和盐酸反应生成氯气和VO2+.请再写一个离子反应方程式,说明还原性:SO32->Cl->VO2+
Cl2+SO32-+H2O=2Cl-+2H++SO42-
Cl2+SO32-+H2O=2Cl-+2H++SO42-
.