摘要:A.0.025mol B.0.050mol
网址:http://m.1010jiajiao.com/timu_id_417732[举报]
 已知2A(g)+B(g)?2C(g),向容积为1L的密闭容器中加入0.050mol A和0.025mol B,在500℃时充分反应,达平衡后测得c(C)=0.040mol.L-1,放出热量Q1 kJ.
已知2A(g)+B(g)?2C(g),向容积为1L的密闭容器中加入0.050mol A和0.025mol B,在500℃时充分反应,达平衡后测得c(C)=0.040mol.L-1,放出热量Q1 kJ.(1)能说明上述反应已经达到化学平衡状态的是
bc
bc
(填字母编号)a.v(C)=2v(B)
b.单位时间内生成2mol A的同时消耗1molB
c.容器内压强保持不变d.容器内气体的密度保持不变
(2)若在相同的容器中只加入0.050mol C,500℃时充分反应达平衡后,吸收热量Q2 kJ,则Q1与Q2之间的关系式可表示为
Q1=4Q2
Q1=4Q2
(用含Q1、Q2的代数式表示).(3)500℃时,上述反应的化学平衡常数K=
3200L?mol-1
3200L?mol-1
.(4)已知K(300℃)>K(350℃),该反应是
放
放
(填“放”或“吸”)热反应;若反应温度升高,A的转化率减小
减小
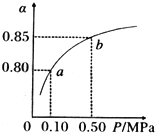
(填“增大”、“减小”或“不变”).(5)某温度下,A的平衡转化率(a))与体系总压强(P)的关系如图所示,平衡状态由a变到b时,化学平衡常数K(A)
=
=
K(B)(填“>”、“<”或“=”. )实验室用铅蓄电池电解饱和食盐水制取氯气,已知铅蓄电池放电时发生反应:
负极
正极
![]()
当制得![]() 0.050mol时,电池内消耗的
0.050mol时,电池内消耗的![]() 的物质的量至少是
的物质的量至少是
[ ]
A.0.025mol
B.0.050mol
C.0.10mol
D.0.20mol
实验室用铅蓄电池电解饱和食盐水制取氯气,已知铅蓄电池放电时发生反应:
负极
正极
![]()
当制得![]() 0.050mol时,电池内消耗的
0.050mol时,电池内消耗的![]() 的物质的量至少是
的物质的量至少是
[ ]
A.0.025mol
B.0.050mol
C.0.10mol
D.0.20mol
实验室用铅蓄电池作电源电解饱和食盐水制取氯气,已知铜蓄电池放电时发生如下反应:
负极:Pb+![]() ══
══![]() +2e- ; 正极:
+2e- ; 正极:![]() +4H++
+4H++![]() +2e-══
+2e-══![]() +
+![]()
今若制得Cl2 0.050mol,这时电池内消耗的H2SO4的物质的量至少是( )
A.0.025mol B.0.050mol
C.0.10mol D.0.20mol
查看习题详情和答案>>
 已知298K时:
已知298K时:反应Ⅰ:2H2(g)+O2(g)=2H2O(g)△H=-484.0kJ?mol-1
反应Ⅱ:CO(g)+1/2O2(g)?CO2(g)△H=-283.0kJ?mol-1
(1)298K时,将a mol CO2与b mol H2混合气体充入容积为1L的密闭容器中,2min后反应达到平衡状态时测得产物CO的浓度为c mol?L-1.则:
①v(H2)=
| c |
| 2 |
| c |
| 2 |
②CO2与H2发生反应生成CO和水蒸气的热化学方程式为
CO2(g)+H2(g)?CO(g)+H2O(g)△H=+41.0kJ?mol-1
CO2(g)+H2(g)?CO(g)+H2O(g)△H=+41.0kJ?mol-1
.若不同温度下发生上述反应,其化学平衡常数K(700℃)<
<
K(830℃)(填写“<”、“>”或“=”)(2)向容积为1L的密闭容器中加入0.050mol CO和0.025mol O2,在一定温度下发生反应Ⅱ,达平衡后测得c(CO2)=0.040mol?L-1.则:①能说明反应Ⅱ已经达到化学平衡状态的是
bc
bc
(填写序号).a.v(CO2)=2v (O2) b.容器内压强保持不变
c.v逆(CO)=2v正(O2) d.容器内气体的密度保持不变
②该温度条件下,反应Ⅱ的化学平衡常数K=
56.56
56.56
.③某温度下,CO的平衡转化率(a)与体系总压强(P)的关系如下图所示.
平衡状态由a变到b时,平衡常数K(a)
=
=
K(b)(填“>”、“<”或“=”).