摘要:25. 2H+ + 2e = H2 ↑ 4 (3)Zn片上有较多气泡.石墨上有少量气泡 [或能够与对比说明]
网址:http://m.1010jiajiao.com/timu_id_413792[举报]
 (1)写出图①中电解池阴阳两极的电极反应式和该电解池的总反应式:
(1)写出图①中电解池阴阳两极的电极反应式和该电解池的总反应式:阴极:
Cu2++2e-=Cu
Cu2++2e-=Cu
;阳极:
4OH--4e-=O2↑+2H2O
4OH--4e-=O2↑+2H2O
;电解池总反应式:
2CuSO4+2H2O
2Cu+O2↑+2H2SO4
| ||
2CuSO4+2H2O
2Cu+O2↑+2H2SO4
.
| ||
(2)写出图②中原电池正负两极的电极反应式和该原电池的总反应式:
正极:
2H++2e-=H2↑
2H++2e-=H2↑
;负极:
Zn-2e-=Zn2+
Zn-2e-=Zn2+
;原电池总反应式:
Zn+2HCl=ZnCl2+H2↑
Zn+2HCl=ZnCl2+H2↑
.在由铜锌组成的原电池(电解质是稀硫酸)中,有位同学在铜电极收集到了12g的气体,
(1)铜锌原电池的正、负极的电极反应:正极:
(2)铜电极产生12g气体的过程中有
(3)铜电极产生12g气体的过程中有
查看习题详情和答案>>
(1)铜锌原电池的正、负极的电极反应:正极:
2H++2e-=H2↑
2H++2e-=H2↑
负极:Zn-2e-=Zn2+
Zn-2e-=Zn2+
(2)铜电极产生12g气体的过程中有
390
390
g的锌溶解.(3)铜电极产生12g气体的过程中有
12
12
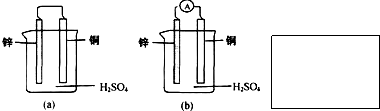
mol的电子发生了转移.(1)将一块纯净的锌片插入盛有稀硫酸的烧杯里,可观察到锌片逐渐溶解,并有气体产生,再平行地插入一块铜片,可观察到铜片上
(2)用导线连接灵敏电流计的两端后,再与溶液中的锌片和铜片相连接(如图b所示),观察到灵敏电流计的指针发生偏转,说明导线中有电流通过.从上述现象可以归纳出构成原电池的某些条件是:
(3)可见,图b是一个将
所需物品及仪器:
实验操作步骤及现象:
查看习题详情和答案>>
没有
没有
(填“有”或“没有”)气泡产生.用导线将锌片和铜片连接起来(如图a所示),可观察到铜片上有
有
(填“有”或“没有”)气泡产生.(2)用导线连接灵敏电流计的两端后,再与溶液中的锌片和铜片相连接(如图b所示),观察到灵敏电流计的指针发生偏转,说明导线中有电流通过.从上述现象可以归纳出构成原电池的某些条件是:
两电极要同时插入电解质溶液中,并用导线连接起来形成闭合回路
两电极要同时插入电解质溶液中,并用导线连接起来形成闭合回路
,电极反应式是:锌片Zn-2e-=Zn2+
Zn-2e-=Zn2+
;铜片2H++2e-=H2↑
2H++2e-=H2↑
.(3)可见,图b是一个将
化学
化学
能转化为电
电
能的装置,被称为原电池.我们也可以用家庭常见的一些仪器和物品,自制一个原电池,请你尝试涉及实验,并将你所设计的原电池简图画在右面的方框内:所需物品及仪器:
水果(或果汁等电解质溶液)、铜片、锌片、导线、灵敏电流计(或小灯泡等)
水果(或果汁等电解质溶液)、铜片、锌片、导线、灵敏电流计(或小灯泡等)
.实验操作步骤及现象:
将铜片和锌片同时插入水果中,用导线连接铜片、灵敏电流计和锌片,可以看到电流表指针发生偏转(或小灯泡发光),即形成了原电池
将铜片和锌片同时插入水果中,用导线连接铜片、灵敏电流计和锌片,可以看到电流表指针发生偏转(或小灯泡发光),即形成了原电池
.
 Zn-MnO2干电池应用广泛,其示意图如下,电解质溶液是ZnCl2-NH4Cl混合溶液.
Zn-MnO2干电池应用广泛,其示意图如下,电解质溶液是ZnCl2-NH4Cl混合溶液.(1)该电池的负极材料是
Zn(或锌)
Zn(或锌)
.电池工作时,电子流向正极
正极
(填“正极”或“负极”).(2)如果该电池的工作原理为:Zn+2NH4Cl=ZnCl2+2NH3+H2,其正极反应式为:
2NH4++2e-=2NH3+H2
2NH4++2e-=2NH3+H2
(3)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀.其主要原因是
锌置换出铜,Zn+Cu2+=Cu+Zn2+,在溶液中,构成铜锌原电池,加快化学反应速率
锌置换出铜,Zn+Cu2+=Cu+Zn2+,在溶液中,构成铜锌原电池,加快化学反应速率
.欲除去Cu2+,最好选用下列试剂中的b
b
(填代号).a.NaOH b.Zn c.Fe d.NH3?H2O
(4)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液.阴极的电极反应式是:
2H++2e-→H2
2H++2e-→H2
;若电解电路中通过2mol电子,MnO2的理论产量为87g
87g
.