摘要:(3)F+IN的离子方程式: .
网址:http://m.1010jiajiao.com/timu_id_403929[举报]
一、1.B 2.BD 3.D 4.BD 5.CD 6.B?
7.解析:浓盐酸与足量的MnO2反应时,随着反应的进行,盐酸浓度变小,后者反应会停止,有一部分HCl不能转变成Cl2。
答案:B?
8.D 9.B?
二、10.(1)先变红,后褪色?
(2)2FeCl2+Cl2===2FeCl3 溶液由浅绿色变棕黄色?
(3)AgNO3+HCl===AgCl↓+HNO3 产生白色沉淀?
(4)Na2CO3+2HCl===2NaCl+H2O+CO2↑ 产生无色无味的气体?
(5)SO2+Cl2+2H2O===H2SO4+2HCl 氯水褪色?
(6)Mg+2HCl===MgCl2+H2↑ 产生无色无味气体?
11.(1)KCl Al Al(OH)3?
(2)2KCl+2H2O 2KOH+Cl2↑+H2↑
2KOH+Cl2↑+H2↑
(3)Al3++3ClO-+3H2O===Al(OH)3↓+3HClO?
12.(1)水 (2)无水CaCl2?
(3)白磷上残留的水溶解在酒精中,残留的酒精又溶解在醚中?
(4)用NaOH溶液吸收(装置图略)?
13.(1)2 4 ―― 2 2 1 2 H2O?
(2)② (3)0.2 (4)2.63?
14.9.18 kg?
15.m(KClO3)为61.25 g,m(MnO2)为6.09 g;c(Na2SO3)为0.14 mol?L-1。
甲、乙、丙、丁为四种常见单质,常温下,乙、丙、丁为气体.丙常用于自来水消毒,甲是生活中常见金属,A在通常情况下为无色液体,B、C在溶液中反应.
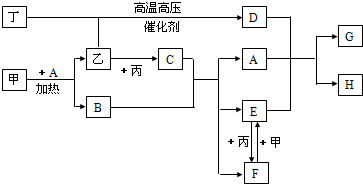
(1)D的化学式为
(2)甲+A反应的化学方程式为
(3)F+甲反应的离子方程式为
(4)A+D+E反应的离子方程式为
查看习题详情和答案>>

(1)D的化学式为
NH3
NH3
;闻气体丙的正确方法是扇闻
扇闻
;取少量长期放置的丙的水溶液,滴入几滴石蕊试液,可观察到的现象是溶液变红
溶液变红
.(2)甲+A反应的化学方程式为
3Fe+4H2O
Fe3O4+4H2
| ||
3Fe+4H2O
Fe3O4+4H2
.
| ||
(3)F+甲反应的离子方程式为
2Fe3++Fe=3Fe2+
2Fe3++Fe=3Fe2+
;该反应中,证明甲适量或过量的方法是取少量反应后的溶液于试管中,滴入几滴KSCN溶液,若溶液不变色,说明甲过量或适量
取少量反应后的溶液于试管中,滴入几滴KSCN溶液,若溶液不变色,说明甲过量或适量
.(4)A+D+E反应的离子方程式为
Fe2++2NH3?H2O=Fe(OH)2↓+2NH4+
Fe2++2NH3?H2O=Fe(OH)2↓+2NH4+
;该反应能顺利进行,是利用了D的极易溶于水且溶于水后显碱性
极易溶于水且溶于水后显碱性
的性质;若反应在试管中进行一,则其现象为先生成白色絮状沉淀,迅速变成灰绿色,最后变成红褐色
先生成白色絮状沉淀,迅速变成灰绿色,最后变成红褐色
.(2011?许昌模拟)已知物质M由属于同一周期的X.Y两种短周期元素组成,X原子的最外层电子数是最内层电子数的一半,Y元素最高正价与它的负价代数和为6.M与其他物质的转化关系如下(部分产物已略去):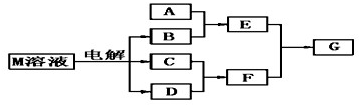
(1)已知元素Z与Y是最外层电子数相同的短周期元素,那么Z与Y分别与氢形成的氢化物中沸点较高的是
(2)若A是一种常见的酸性氧化物,且可用于制造玻璃,则E溶液与F溶液反应的离子方程式是:
(3)若A是与X、Y同周期元素的一种常见金属单质,且A与B溶液能够反应,则其化学方程式是:
 (4)若A是一种常见的化肥,式量为79,且E与F生成G时有白烟产生,则A的化学式
(4)若A是一种常见的化肥,式量为79,且E与F生成G时有白烟产生,则A的化学式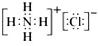
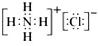 ;
;
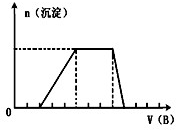
(5)若A是一种溶液,只可能含有H+.NH4+、Mg2+、Fe3+、Al3+、CO32-、SO42-中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积变化如图所示,由此可知,该溶液中肯定含有的离子是
查看习题详情和答案>>

(1)已知元素Z与Y是最外层电子数相同的短周期元素,那么Z与Y分别与氢形成的氢化物中沸点较高的是
HF
HF
(填化学式),原因是F元素电负性很强,HF分子之间可以形成氢键
F元素电负性很强,HF分子之间可以形成氢键
;(2)若A是一种常见的酸性氧化物,且可用于制造玻璃,则E溶液与F溶液反应的离子方程式是:
SiO32-+2H++2H2O=H4SiO4↓或SiO32-+2H+=H2SiO3↓
SiO32-+2H++2H2O=H4SiO4↓或SiO32-+2H+=H2SiO3↓
;(3)若A是与X、Y同周期元素的一种常见金属单质,且A与B溶液能够反应,则其化学方程式是:
2NaOH+2H2O+2Al=2NaAlO2+3H2↑
2NaOH+2H2O+2Al=2NaAlO2+3H2↑
; (4)若A是一种常见的化肥,式量为79,且E与F生成G时有白烟产生,则A的化学式
(4)若A是一种常见的化肥,式量为79,且E与F生成G时有白烟产生,则A的化学式NH4HCO3
NH4HCO3
,G的电子式是: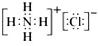
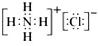
(5)若A是一种溶液,只可能含有H+.NH4+、Mg2+、Fe3+、Al3+、CO32-、SO42-中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积变化如图所示,由此可知,该溶液中肯定含有的离子是
H+、NH4+、Al3+、SO42-
H+、NH4+、Al3+、SO42-
(微粒次序按摩尔质量从小到大,下同),物质的量浓度之比为2:3:1:4
2:3:1:4
.A、B、C、D、E、F、G是中学里常遇到的一些物质,它们之间有如下转化关系,有些必要的信息已在框图中注明:

回答下列问题:
(1)D的空间构型为
 F溶液名称是
F溶液名称是
(2)在实验室中制取气体A的离子方程式是
(3)写出A+D→C的化学方程式
(4)写出:F+B→E的离子方程式
查看习题详情和答案>>

回答下列问题:
(1)D的空间构型为
三角锥形
三角锥形
,C的电子式为

银氨溶液
银氨溶液
(2)在实验室中制取气体A的离子方程式是
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
| ||
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
.
| ||
(3)写出A+D→C的化学方程式
3Cl2+8NH3═N2+6NH4Cl
3Cl2+8NH3═N2+6NH4Cl
,氧化剂与还原剂物质的量之比为3:2
3:2
(4)写出:F+B→E的离子方程式
Ag(NH3)2++2H++Cl-═2NH4++AgCl↓(或Ag(NH3)2++2OH-+4H++Cl-═2NH+4+AgCl↓+2H2O)
Ag(NH3)2++2H++Cl-═2NH4++AgCl↓(或Ag(NH3)2++2OH-+4H++Cl-═2NH+4+AgCl↓+2H2O)
. I.“阿波罗登月计划”总指挥韦伯在“阿波罗”登月成功后曾说:“阿波罗计划”中没有一项新发明的技术,都是现成的技术,关键在于综合.综合也是创新,例如可以用玻璃管制成的U形管、T形管、乳胶管、弹簧夹连接成如图所示的一种装置,在U型管中加入适量的红色溶液,即得简单U型气压计,我们可将它应用于多项实验,如:A.证明空气中的氧气参与氧化还原反应的实验(如铁生锈);B.溶解热效应实验(如硝酸铵溶于水);C.装置的气密性检验实验;D.检验某些气体性质的实验(如CO2,SO2、Cl2等与碱溶液的反应)等等.请从A或B中选择一项实验,画出该实验的装置图,写出实验名称.要求:①除U形气压计外,其他实验仪器或用品仅能从以下仪器中选取:广口瓶、小试管、胶头滴管、橡皮塞、乳胶管、导管;②实验药品或试剂自定,但需在图中注明.
I.“阿波罗登月计划”总指挥韦伯在“阿波罗”登月成功后曾说:“阿波罗计划”中没有一项新发明的技术,都是现成的技术,关键在于综合.综合也是创新,例如可以用玻璃管制成的U形管、T形管、乳胶管、弹簧夹连接成如图所示的一种装置,在U型管中加入适量的红色溶液,即得简单U型气压计,我们可将它应用于多项实验,如:A.证明空气中的氧气参与氧化还原反应的实验(如铁生锈);B.溶解热效应实验(如硝酸铵溶于水);C.装置的气密性检验实验;D.检验某些气体性质的实验(如CO2,SO2、Cl2等与碱溶液的反应)等等.请从A或B中选择一项实验,画出该实验的装置图,写出实验名称.要求:①除U形气压计外,其他实验仪器或用品仅能从以下仪器中选取:广口瓶、小试管、胶头滴管、橡皮塞、乳胶管、导管;②实验药品或试剂自定,但需在图中注明.


实验名称:
Ⅱ.广口瓶简单,但它的用途真不简单!实验室用Zn粒和盐酸反应制得的H2,其中含酸雾、水汽、硫化氢及少量氧气等杂质气体,某同学仅用四只广口瓶设计了以下几种装置,按一定顺序连接,便达到了当气体通过时,每一装置除去一种气体的目的.

(1)它们连接的顺序为
a→b→e→f→g→h→d→c
a→b→e→f→g→h→d→c
;(2)除去H2S的离子方程式为
Cu2++H2S=CuS↓+2H+
Cu2++H2S=CuS↓+2H+
;(3)除去O2的离子方程式为
4Fe2++O2+4H+=4Fe3++2H2O
4Fe2++O2+4H+=4Fe3++2H2O
,观察到的现象为装有FeSO4和H2SO4溶液的广口瓶中溶液的颜色由浅绿色变成棕黄色
装有FeSO4和H2SO4溶液的广口瓶中溶液的颜色由浅绿色变成棕黄色
.已知A、B、C为金属单质,甲、丙为无色气体,乙为黄绿色气体,D、E、F、G、H为中学常见的化合物,其中H为红褐色沉淀,它们之间能发生如下反应(图中的产物和条件未全部标出)
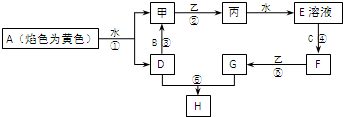
根据推断结果回答下列问题:
(1)写出下列物质的化学式:B
(2)写出③的化学方程式:
(3)写出⑤的离子方程式:
(4)F与D反应后的产物在空气中转化为H的化学方程式为:
查看习题详情和答案>>

根据推断结果回答下列问题:
(1)写出下列物质的化学式:B
Al
Al
,丙HCl
HCl
;(2)写出③的化学方程式:
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
;(3)写出⑤的离子方程式:
2Fe2++Cl2=2Fe3++2Cl-
2Fe2++Cl2=2Fe3++2Cl-
;(4)F与D反应后的产物在空气中转化为H的化学方程式为:
4Fe(OH)2+O2+2H2O=4Fe(OH)3
4Fe(OH)2+O2+2H2O=4Fe(OH)3
;现象为白色沉淀变成灰绿色,最后变成红褐色
白色沉淀变成灰绿色,最后变成红褐色
.