网址:http://m.1010jiajiao.com/timu_id_401941[举报]
物质在水溶液中存在的电离平衡、水解平衡和沉淀溶解平衡,都可看作化学平衡。请根据所学知识回答:
(1)在0.1mo1?L-1的NaHSO3溶液中存在的各种平衡体系为(用离子方程式表示)_______.
已知该溶液中有关微粒浓度由大到小的顺序为:c(Na+)>c(HSO![]() )>c(SO
)>c(SO![]() )>c(H2SO4)。则该溶液中c(H+) c(OH-) (填“大于”、“小于”或“等于”),简述理由:__________________________________________.
)>c(H2SO4)。则该溶液中c(H+) c(OH-) (填“大于”、“小于”或“等于”),简述理由:__________________________________________.
(2)常温下,某水溶液中存在的离子有:Na+、A―、H+、OH―,若该溶液由0.1mo1.L-1的HA溶液和0.1mol.L-1的NaOH溶液等体积混合而得,则溶液的pH _________(填“大于”、“小于”或“等于”)7,理由是____________。
(3)25℃时,Fe(OH)3的KSP=1.0×10-38mol4?L-4,Mg(OH)2的KSP=1.0×10-11mol3?L-3。某混合溶液中Fe3+和Mg2+的浓度均为1.0 ![]() 10-2mo1.L―1,现要除去溶液中的Fe3+,而Mg2+不沉淀,应将溶液的pH控制在________范围之内。(化学上通常认为残留在溶液中的离子浓度小于1.0×10-5mol.L-1时,沉淀就达到完全)
10-2mo1.L―1,现要除去溶液中的Fe3+,而Mg2+不沉淀,应将溶液的pH控制在________范围之内。(化学上通常认为残留在溶液中的离子浓度小于1.0×10-5mol.L-1时,沉淀就达到完全)

(1)在粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂为:
a.盐酸 b.氯化钡溶液 c.氢氧化钠溶液 d.碳酸钠溶液,则加入试剂的顺序是_______(填编号).
(2)Mg(OH)2中加入盐酸后,要获得MgCl2·6H2O晶体,需要进行的实验操作依次为______.
a.蒸馏 b.灼烧 .过滤 d.蒸发 e.冷却结晶
(3)利用MgCl2·6H2O可制得无水氯化镁,应采取的措施是__________________.
(4)目前工业上主要采用离子交换膜法电解饱和食盐水,下列关于离子交换膜电解槽的叙述错误的是____.
a.精制饱和食盐水进入阳极室
b.纯水(加少量NaOH)进入阴极室
c.阴极产物为氢氧化钠和氢气
d.阳极的电极反应为:Cl2+2e-===2Cl-
(5)母液中常含有MgCl2、NaCl、MgSO4、KCl等(其溶解度与温度的关系如图所示),可进一步加工制得一些重要的产品.若将母液加热升温到60℃以上,随着水分的蒸发,会逐渐析出晶体,此晶体的主要成分是________;过滤上述晶体后,将滤液降温到30℃以下,又逐渐析出晶体,用一定量的冷水洗涤该晶体,最后可得到比较纯净的________晶体.

蛇纹石可用于生产氢氧化镁,简要工程如下:
Ⅰ.制取粗硫酸镁:用酸液浸泡蛇纹石矿粉,过滤,并在常温常压下结晶,制得粗硫酸镁(其中常含有少量Fe3+、Al3+、Fe2+等杂质离子)
Ⅱ.提纯粗硫酸镁:将粗硫酸镁在酸性条件下溶解,加入适量的0.1mol?L-1H2O2溶液,再调节溶液pH至7~8,并分离提纯.
Ⅲ.制取氢氧化镁:向步骤Ⅱ所得溶液中加入过量氨水.
| Fe3+ | Al3+ | Fe2+ | Mg2+ | |
| 开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
| 沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
请回答:
(1)步骤Ⅱ中,可用于调节溶液pH至7~8的最佳试剂是______(填字母序号)
A.MgO B.Na2CO3 C.蒸馏水
(2)检验粗硫酸镁溶液中Fe2+的方法是:______ (注明试剂、现象).
(3)步骤Ⅲ中制备氢氧化镁反应的离子方程式为______.
(4)步骤Ⅱ沉淀后溶液中主要存在(NH4)2SO4,已知室温下0.1mol?L-1的(NH4)2SO4溶液pH是5,则溶液中离子浓度由大到小的排列为______,溶液中:2c(SO42-)-c(NH4+)=______mol?L-1(用精确数值表示)
(5)某生产科研小组经查阅资料得到以下溶度积Ksp数据(298K时):
Mg(OH)2(S)?Mg2+(aq)+2OH-(aq) Ksp=[Mg2+]?[OH-]2=5.6×10-12
Ca(OH)2(S)?Ca2+(aq)+2OH-(aq) Ksp=[Ca2+]?[OH-]2=4.7×10-6
该科研小组认为可以用熟石灰替代氨水制得氢氧化镁,他们的理由是______.
若沉淀转化反应为:Mg2+(aq)+Ca(OH)2(S)?Mg(OH)2(S)+Ca2+(aq),求此温度下该反应的化学平衡常数K=______ (写出算式和结果). 查看习题详情和答案>>
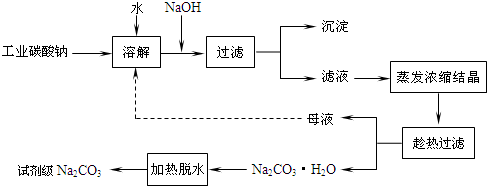
已知:碳酸钠的饱和溶液在不同温度下析出的溶质如图所示:
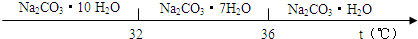
(1)加入NaOH溶液时发生的离子反应方程式为
(2)热的Na2CO3溶液有较强的去油污能力,其原因是(用离子方程式及必要的文字加以解释)
(3)“趁热过滤”时的温度应控制在
(4)已知:Na2CO3?10H2O(s)=Na2CO3(s)+10H2O(g)△H=+532.36kJ?mol-1
Na2CO3?10H2O(s)=Na2CO3?H2O(s)+9H2O(g)△H=+473.63kJ?mol-1
写出Na2CO3?H2O脱水反应的热化学方程式
(5)有人从“绿色化学”角度设想将“母液”沿流程图中虚线所示进行循环使用.请你分析实际生产中是否可行
以水氯镁石(主要成分为MgCl2·6H2O)为原料生产碱式碳酸镁的主要流程如下:
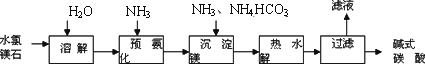
(1)预氨化过程中有Mg(OH)2沉淀生成,已知常温下Mg(OH)2的Ksp=1.8×10-11,若溶液中c(OH-)=3.0×10-6 mol·L-1,则溶液中c(Mg2+)=________.
(2)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为________.
(3)高温煅烧碱式碳酸镁得到MgO.取碱式碳酸镁4.66 g,高温煅烧至恒重,得到固体2.00 g和标准状况下CO2 0.896 L,通过计算确定碱式碳酸镁的化学式.
(4)若热水解不完全,所得碱式碳酸镁中将混有MgCO3,则产品中镁的质量分数________(填“升高”、“降低”或“不变”).