摘要:右侧留下的“笔记与反思 空档.是供老师.学生课堂记录及课后小结用的.可以写上重要的概念和规律.复习过程的心得体会.解题过程.变式习题.重难点.误中思.思中悟等.
网址:http://m.1010jiajiao.com/timu_id_398660[举报]
 现有A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大,D与E同主族,且D的氢化物常温时为液态.A、B的最外层电子数之和与C的最外层电子数相等,A分别与B、C、D形成电子总数相等的分子.
现有A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大,D与E同主族,且D的氢化物常温时为液态.A、B的最外层电子数之和与C的最外层电子数相等,A分别与B、C、D形成电子总数相等的分子.(1)C的元素符号是
N
N
;B的最高价氧化物的电子式为

第三周期第ⅦA族
第三周期第ⅦA族
.(2)B、C、D元素的氢化物的沸点由商到低的顺序为
H2O>NH3>CH4
H2O>NH3>CH4
(用化学式表示).(3)将足量D的单质通入到A2E的溶液中,反应的化学方程式为
2H2S+O2=2S↓+2H2O
2H2S+O2=2S↓+2H2O
(4)最近意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的C4气态分子.C4分子结构如图所示,已知断裂1molC-C吸收l67KJ的热量,生成1mol C≡C放出942KJ热量.试写出由C4气态分子变成C2气态分子的热化学方程式:
N4(g)=2N2(g)△H=-882kJ/mol
N4(g)=2N2(g)△H=-882kJ/mol
.(5)某盐x(C2A6F2)的性质与CA4F类似,是离子化合物,其水溶液因分步水解而呈弱酸性.
①盐x显酸性原因(用离子方程式表示)
N2H62++H2O?[N2H5?H2O]++H+
N2H62++H2O?[N2H5?H2O]++H+
.②写出足量金属镁加入盐x的溶液中产生H2的记学方程式为
Mg+N2H6Cl2=MgCl2+N2H4+H2↑
Mg+N2H6Cl2=MgCl2+N2H4+H2↑
.金刚烷是一种重要的化工原料,如合成的金刚烷胺就是一种抗病毒药剂,对帕金森症、老年痴呆有良好的疗效.由环戊二烯合成金刚烷的路线如下:
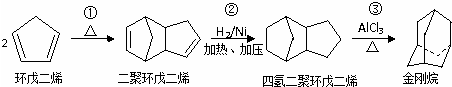
请回答下列问题:
(1)反应①的反应类型是
(2)写出环戊二烯与Br21:1在较高温度下的加成反应产物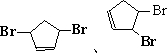
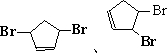 .
.
(3)金刚烷形成的二氯取代物有
(4)在有机分析中,常用臭氧氧化分解来确定有机物中碳碳双键的位置与数目.
A是金刚烷的一种同分异构体,经臭氧氧化后的产物仅为一种,其结构为 ,试写出A所有可能的结构简式
,试写出A所有可能的结构简式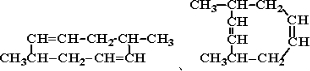
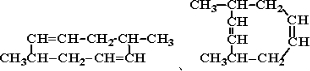 .
.
查看习题详情和答案>>

请回答下列问题:
(1)反应①的反应类型是
加成反应
加成反应
,金刚烷的分子式为C10H16
C10H16
.(2)写出环戊二烯与Br21:1在较高温度下的加成反应产物
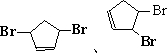
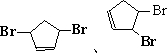
(3)金刚烷形成的二氯取代物有
2
2
种(4)在有机分析中,常用臭氧氧化分解来确定有机物中碳碳双键的位置与数目.

A是金刚烷的一种同分异构体,经臭氧氧化后的产物仅为一种,其结构为
 ,试写出A所有可能的结构简式
,试写出A所有可能的结构简式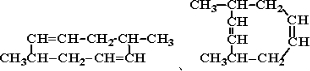
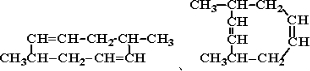
1、亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌.以下是过氧化氢法生产亚氯酸钠的工艺流程图:
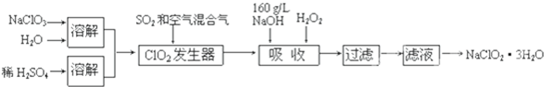
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2?3H2O.
②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全.
③160g/L NaOH溶液是指160g NaOH固体溶于水所得溶液的体积为1L.
(1)160g/L NaOH溶液的物质的量浓度为:
(2)发生器中鼓入空气的作用是:
(3)吸收装置内发生反应的化学方程式为:
吸收装置中的温度不能过高,其原因是:
(4)吸收塔中为防止NaClO2被还原成NaCl,所用还原剂的还原性应适中.除H2O2外,还可以选择的还原剂是
(选填序号)a.Na2O2 b.Na2S c.FeCl2
(5)从滤液中得到NaClO2?3H2O粗晶体的实验操作依次是
a.蒸发结晶 b.蒸发浓缩 c.灼烧 d.过滤 e.冷却结晶
2、在氯氧化法处理含CN一的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐再进一步被氧化为无毒物质.
(1)某厂废水中含KCN,其浓度为650mg?L-1.现用氯氧化法处理,发生如下反应:KCN+2KOH+Cl2=KOCN+2KCl+H2O,再投入过量液氯,可将氰酸盐进一步氯化为氮气.请配平下列化学方程式:
(配平后请在方框内填写每种物质的化学计量数,若为“1”也要写上)
(2)若处理上述废水20L,使KCN完全转化为无毒物质,至少需液氯
查看习题详情和答案>>

已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2?3H2O.
②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全.
③160g/L NaOH溶液是指160g NaOH固体溶于水所得溶液的体积为1L.
(1)160g/L NaOH溶液的物质的量浓度为:
4.00 mol/L
4.00 mol/L
(结果保留三位有效数字)(2)发生器中鼓入空气的作用是:
稀释ClO2,防止ClO2分解爆炸
稀释ClO2,防止ClO2分解爆炸
.(3)吸收装置内发生反应的化学方程式为:
2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2
2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2
;吸收装置中的温度不能过高,其原因是:
防止H2O2的分解
防止H2O2的分解
.(4)吸收塔中为防止NaClO2被还原成NaCl,所用还原剂的还原性应适中.除H2O2外,还可以选择的还原剂是
a
a
(选填序号)a.Na2O2 b.Na2S c.FeCl2
(5)从滤液中得到NaClO2?3H2O粗晶体的实验操作依次是
b e d
b e d
(选填序号)a.蒸发结晶 b.蒸发浓缩 c.灼烧 d.过滤 e.冷却结晶
2、在氯氧化法处理含CN一的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐再进一步被氧化为无毒物质.
(1)某厂废水中含KCN,其浓度为650mg?L-1.现用氯氧化法处理,发生如下反应:KCN+2KOH+Cl2=KOCN+2KCl+H2O,再投入过量液氯,可将氰酸盐进一步氯化为氮气.请配平下列化学方程式:
(配平后请在方框内填写每种物质的化学计量数,若为“1”也要写上)
2
2
KOCN+4
4
KOH+3
3
Cl2→2
2
CO2+1
1
N2+6
6
KCl+2
2
H2O(2)若处理上述废水20L,使KCN完全转化为无毒物质,至少需液氯
35.5
35.5
g.现有A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大,D与E的氢化物分子构型都是V型.A、B的最外层电子数之和与C的最外层电子数相等,A分别与B、C、D形成电子总数相等的分子甲、乙、丙.
(1)元素F在周期表中的位置是
(2)写出元素A、C形成分子C2A4的电子式:
 .
.
(3)甲、乙、丙三物质沸点由高到低的顺序为(用分子式):
(4)生活中的一种绿色氧化剂由A和D组成,一定条件下也可表现出还原性,试写出其和酸性KMnO4反应的离子方程式:
(5)某盐X(C2A6F2)的性质与CA4F类似,是离子化合物,其水溶液因分步水解而呈弱酸性.盐X显酸性原因(用离子方程式表示)
查看习题详情和答案>>
(1)元素F在周期表中的位置是
第三周期第ⅦA族
第三周期第ⅦA族
.(2)写出元素A、C形成分子C2A4的电子式:


(3)甲、乙、丙三物质沸点由高到低的顺序为(用分子式):
H2O>NH3>CH4
H2O>NH3>CH4
.(4)生活中的一种绿色氧化剂由A和D组成,一定条件下也可表现出还原性,试写出其和酸性KMnO4反应的离子方程式:
2MnO4-+5H2O2+16H+=2Mn2++5O2↑+8H2O
2MnO4-+5H2O2+16H+=2Mn2++5O2↑+8H2O
.(5)某盐X(C2A6F2)的性质与CA4F类似,是离子化合物,其水溶液因分步水解而呈弱酸性.盐X显酸性原因(用离子方程式表示)
N2H62++H2O?[N2H5?H2O]++H+
N2H62++H2O?[N2H5?H2O]++H+
.(2010?安徽模拟)某研究性学习小组为探究铜、锌与浓盐酸的反应,设计实验探究方案如下:
实验用品:纯锌片、铜片、37%的浓盐酸、蒸馏水、氯化钾溶液、稀硝酸溶液
实验记录:

背影资料:

请你参与以下探究:
(1)实验A反应速度明显比B小,原因是
(2)根据“铜位于金属活动顺序表氢之后,与稀盐酸不反应,而在实验中加热时又产生气体”的事实,作出如下推断:
①有同学认为“实验C中加热时产生的气体是溶解在溶液中的H2”,你认为是否有道理,理由是
②某同学作了如下猜想:是否成立?请你设计实验方案加入验证.
(3)某同学对实验D中的白色沉淀进行分析:“不可能是CuCl2,因为CuCl2能溶于水且溶液显蓝色;也不可能是ZnCl2,因为稀释后溶液更稀,不会析出ZnCl2晶体.若利用资源卡片资料大胆猜想,白色沉淀可能是CuCl.请你帮他设计验证方案(若有多处方案,只设计两个).
(4)指导老师肯定了实验D中的白色沉淀是CuCl;并措出生成沉淀的原因,实际上是[CuCl4]2等离子与CuCl(s)、Cl三者之间所形成的沉淀溶解平衡移动的结果.请写出这一平衡关系式(用离子方程式表示):
查看习题详情和答案>>
实验用品:纯锌片、铜片、37%的浓盐酸、蒸馏水、氯化钾溶液、稀硝酸溶液
实验记录:

背影资料:

请你参与以下探究:
(1)实验A反应速度明显比B小,原因是
铜锌及浓盐酸一起组成了原电池,加快了反应速率
铜锌及浓盐酸一起组成了原电池,加快了反应速率
.(2)根据“铜位于金属活动顺序表氢之后,与稀盐酸不反应,而在实验中加热时又产生气体”的事实,作出如下推断:
①有同学认为“实验C中加热时产生的气体是溶解在溶液中的H2”,你认为是否有道理,理由是
没道理,因为H2本身难溶于水
没道理,因为H2本身难溶于水
.②某同学作了如下猜想:是否成立?请你设计实验方案加入验证.
| 猜想 | 验证方法 | 预测现象及结论 |
| 认为铜片中可能含有锌等杂质 |
| 猜想 | 预计验证方法 | 猜想的现象与结论 |
| 白色沉淀是氯化亚铜 | ||
[CuCl4]3-(aq)?CuCl(s)+3Cl-(aq)
[CuCl4]3-(aq)?CuCl(s)+3Cl-(aq)
.