网址:http://m.1010jiajiao.com/timu_id_325560[举报]
无机化学反应式
1、2Na+2H2O=2NaOH+H2↑ ★ 2K+2H2O=2KOH+H2↑
2、2Na2O2+2H2O=4NaOH+O2↑ 3、2Na2O2+2CO2=2Na2CO3+O2
4、氢氧化钠和碳酸氢钠在溶液中反应的离子方程式为:
OH- +HCO3- =CO32- +H2O
氯气溶于水(新制氯水中含Cl2.HClO.H2O .H+ .Cl - .ClO - .OH-):
5、Cl2+H2O=HCl+HClO ★ Cl2+2NaOH=NaCl+NaClO+H2O
次氯酸见光分解(强氧化剂、杀菌消毒,漂白剂):
6、2HClO![]() 2HCl+O2↑
2HCl+O2↑
7、Ca(ClO)2+CO2+H2O=CaCO3+2HClO
8、MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
9、2F2+2H2O=4HF+O2 Cl2+H2O=HCl+HClO Br2+H2O=HBr+HBrO
10、2Al+2NaOH+2H2O=2NaAlO2+3H2↑ Al2O3+2NaOH=2NaAlO2+H2O
Al(OH)3+NaOH=NaAlO2+2H2O
11、H2O2的分解: 2H2O2![]() 2H2O+O2↑ *H2S与SO2的反应: 2H2S+SO2=3S+2H2O
2H2O+O2↑ *H2S与SO2的反应: 2H2S+SO2=3S+2H2O
12、2SO2+O2![]() 2SO3
2SO3
13、Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
14、C+2H2SO4(浓) CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
15、SiO2+2C![]() Si+2CO↑
Si+2CO↑
16、![]()
17、N2+O2 ![]() 2NO 2NO+O2=2NO2 3NO2+H2O=2HNO3+NO
2NO 2NO+O2=2NO2 3NO2+H2O=2HNO3+NO
18、4NH3 +5O2 4NO+6H2O
4NO+6H2O
19、用浓盐酸检验氨气(白烟生成): NH3+HCl=NH4Cl
20、(NH4)2SO4+2NaOH Na2SO4+2NH3↑+2H2O
Na2SO4+2NH3↑+2H2O
21、NH4NO3+NaOH=NaNO3+NH3↑+H2O
22、4HNO3![]() 4NO2↑+O2↑+2H2O
4NO2↑+O2↑+2H2O
23、Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
C+4HNO3(浓)=CO2↑+4NO2↑+2H2O
24、FeCl3+3KSCN![]() 3KCl+Fe(SCN)3
3KCl+Fe(SCN)3
25、盐类水解: CH3COO- +H2O![]() CH3COOH+OH- CO32- +H2O
CH3COOH+OH- CO32- +H2O![]() HCO3-+OH-
HCO3-+OH-
HCO3- +H2O![]() H2CO3+OH- NH4+ +H2O
H2CO3+OH- NH4+ +H2O![]() NH3?H2O+H+
NH3?H2O+H+
Fe3+ +3H2O![]() Fe(OH)3+3H+
Fe(OH)3+3H+
27、铝热反应: 2Al+Fe2O3![]() 2Fe+Al2O3
2Fe+Al2O3
4Al+3MnO2![]() 3Mn+2Al2O3
3Mn+2Al2O3
28、2Mg+CO2![]() C+2MgO
C+2MgO
29、Al2(SO4)3+6NH3·¤H2O=2Al(OH)3↓?+2(NH4)2SO4
30、NaAlO2+HCl+H2O=Al(OH)3↓? +NaCl ; NaAlO2+CO2+H2O=Al(OH)3↓? +NaHCO3
31、高温下铁与水反应 :3Fe+4H2O(g)![]() Fe3O4+4H2
Fe3O4+4H2
32、FeCl3+3NaOH=Fe(OH)3↓?+3NaCl
33、4Fe(OH)2+O2+2H2O=4Fe(OH)3
34、2FeCl2+Cl2=2FeCl3 2FeCl3+Fe=3FeCl2
35、氯化铁溶液中加入铜粉: 2FeCl3+Cu=2FeCl2+CuCl2
36、金属的冶炼:Fe2O3+3CO![]() 2Fe+3CO2
2Fe+3CO2
CuO+C![]() Cu+CO↑
Cu+CO↑
![]()
37、铜锌原电池:正极:2H++2e- =H2↑
负极:Zn-2e- =Zn2+
38、钢铁的吸氧腐蚀:正极:O2+4e- +2H2O=4OH-
负极:Fe-2e- =Fe2+
39、Fe(OH)3胶体的制取:FeCl3 +3H2O Fe(OH)3(胶体)+3HCl
Fe(OH)3(胶体)+3HCl
40、电解CuCl2溶液:阳极:2Cl- -2e- =Cl2↑
阴极:Cu2++2e- =Cu
总反应:CuCl2![]() Cu+Cl2↑
Cu+Cl2↑
41、铜的电解精炼:阳极:Cu-2e- =Cu2+
阴极:Cu2++2e- =Cu
42、电镀铜:阳极:Cu-2e- =Cu2+
阴极:Cu2++2e- =Cu
43、电解饱和食盐水:阳极:2Cl- +2e-=Cl2↑
阴极:2H+ +2e- =H2↑
总反应:2NaOH+2H2O![]() H2↑+2NaOH+Cl2↑
H2↑+2NaOH+Cl2↑
44、黄铁矿的燃烧: 4FeS2 +11O2![]() 2Fe2O3+8SO2
2Fe2O3+8SO2
45、氨水吸收少量SO2: SO2+2NH3 +H2O=(NH4)2SO3
46、C+H2O(g)![]() CO+H2
CO+H2
(1)生成氧化亚铜的反应很多,中学化学涉及的反应之一是乙醛与新制的氢氧化铜反应,该反应的化学方程为:
(2)目前常用微乳液-还原法:在100℃,将0.5g十二烷基苯磺酸钠溶解于100mL、0 1mol/L的Cu(NO3)2水溶液中,再快速加入一定体积5mol/L的NaOH水溶液,并搅拌使之混合均匀,再逐滴加入水合肼的水溶液,直至产生红色沉淀,经抽滤、洗涤和真空干燥,得到Cu2O粉末.
①已知:N2H4(l)+O2(g)═N2(g)+2H2O(l)△H=-akJ/mol
Cu(OH)2(s)═CuO(s)+H2O(l)△H=bkJ/mol
4CuO(s)═2Cu2O(s)+O2(g)△H=ckJ/mol
则4Cu(OH)2(s)+N2H4(l)═2Cu2O(s)+N2(g)+6H2O(l)△H=
②十二烷基苯磺酸钠是洗衣粉的主要成分,它在该法中可能的作用是
(3)用铜棒作阳极,钛作阴极,电解氯化钠和氢氧化钠的混合溶液,电解总方程为:2Cu+H2O
| ||
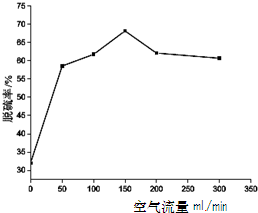
(4)在石化工业中常用纳米Cu2O光解脱硫时,在反应容器中加入一定量含硫混合物[噻吩(C4H4S)和正辛烷按物质的量1:1]并加入0.1g纳米Cu2O,光照同时通入空气1h,分别测定不同流速下最后剩余液中硫的质量分数确定脱硫率,所得结果如右图,下列说法正确的是
A.用正辛烷作溶剂进行实验,是为了模拟柴油的成分
B.用噻吩作含硫化合物是研究有机硫的去除率
C.该实验条件下,空气的流量以150mL/min左右为宜
D.当空气流量超过150mL/min脱硫率下降主要是因为氧化亚铜挥发.
(1)SO2、NOx是形成酸雨和光化学烟雾的环境污染性气体,研究发现,空气中少量的 NO2能参与硫酸型酸雨的形成,反应过程如下:
①SO2+NO2=SO3+NO ②SO3+H2O=H2SO4 ③2NO+O2=2NO2.
则NO2在上述过程中的作用与H2SO4在下述变化中的作用相似的是______.
?A.潮湿的氯气通过盛有浓H2SO4的洗气瓶 B.硫化氢通入浓H2SO4中
?C.亚硫酸钠固体中加入H2SO4 D.制备乙酸乙酯时加入浓H2SO4
(2)CO2可用NaOH溶液吸收得到Na2CO3或NaHCO3.
?①Na2CO3俗称纯碱,因CO32-水解而使其水溶液呈碱性,试写出CO32-水解的离子方程式(忽略第二步水解)______,其水解反应的平衡常数(即水解常数)的表达式为Kh=______.
?②已知25℃时,Kh=2×10-4mol/L,则当溶液中c(HCO3-):c(CO32-)=2:1时,试求溶液的pH=______.
?③0.1mol/L Na2CO3溶液中c(OH-)-c(H+)=______[用含c(HCO-3)、c(H2CO3)的关系式表示].
(3)汽车尾气的主要成分是一氧化碳和氮氧化物,治理尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2NO(g)+2CO(g)?N2(g)+2CO2(g);△H<0.
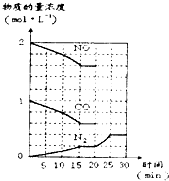
若在一定温度下,将2molNO、lmolCO充入固定容积的容器中,反应过程中各物质的浓度变化如图所示.则从开始到达到平衡状态的过程中,平均反应速率v(CO2)=______(结果保留两位有效数字).该温度下,反应的化学平衡常数为:K=______(用分数表示).20min时,若改变反应条件,导致N2浓度发生如图所示的变化,则改变的条件可能是______(填字母).
①加入催化剂 ②降低温度 ③缩小容器体积 ④增加CO2的物质的量
A.只有①B.只有②C.只有③D.只有④
(1)SO2、NOx是形成酸雨和光化学烟雾的环境污染性气体,研究发现,空气中少量的 NO2能参与硫酸型酸雨的形成,反应过程如下:
①SO2+NO2=SO3+NO ②SO3+H2O=H2SO4 ③2NO+O2=2NO2.
则NO2在上述过程中的作用与H2SO4在下述变化中的作用相似的是______.
?A.潮湿的氯气通过盛有浓H2SO4的洗气瓶 B.硫化氢通入浓H2SO4中
?C.亚硫酸钠固体中加入H2SO4 D.制备乙酸乙酯时加入浓H2SO4
(2)CO2可用NaOH溶液吸收得到Na2CO3或NaHCO3.
?①Na2CO3俗称纯碱,因CO32-水解而使其水溶液呈碱性,试写出CO32-水解的离子方程式(忽略第二步水解)______,其水解反应的平衡常数(即水解常数)的表达式为Kh=______.
?②已知25℃时,Kh=2×10-4mol/L,则当溶液中c(HCO3-):c(CO32-)=2:1时,试求溶液的pH=______.
?③0.1mol/L Na2CO3溶液中c(OH-)-c(H+)=______[用含c(HCO-3)、c(H2CO3)的关系式表示].
(3)汽车尾气的主要成分是一氧化碳和氮氧化物,治理尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2NO(g)+2CO(g)?N2(g)+2CO2(g);△H<0.
若在一定温度下,将2molNO、lmolCO充入固定容积的容器中,反应过程中各物质的浓度变化如图所示.则从开始到达到平衡状态的过程中,平均反应速率v(CO2)=______(结果保留两位有效数字).该温度下,反应的化学平衡常数为:K=______(用分数表示).20min时,若改变反应条件,导致N2浓度发生如图所示的变化,则改变的条件可能是______(填字母).
①加入催化剂 ②降低温度 ③缩小容器体积 ④增加CO2的物质的量
A.只有①B.只有②C.只有③D.只有④
 查看习题详情和答案>>
查看习题详情和答案>>
 CO2、SO2、NOx是重要的非金属氧化物,与我们的生存环境息息相关.
CO2、SO2、NOx是重要的非金属氧化物,与我们的生存环境息息相关.(1)SO2、NOx是形成酸雨和光化学烟雾的环境污染性气体,研究发现,空气中少量的 NO2能参与硫酸型酸雨的形成,反应过程如下:
①SO2+NO2=SO3+NO ②SO3+H2O=H2SO4 ③2NO+O2=2NO2.
则NO2在上述过程中的作用与H2SO4在下述变化中的作用相似的是
?A.潮湿的氯气通过盛有浓H2SO4的洗气瓶 B.硫化氢通入浓H2SO4中
?C.亚硫酸钠固体中加入H2SO4 D.制备乙酸乙酯时加入浓H2SO4
(2)CO2可用NaOH溶液吸收得到Na2CO3或NaHCO3.
?①Na2CO3俗称纯碱,因CO32-水解而使其水溶液呈碱性,试写出CO32-水解的离子方程式(忽略第二步水解)
| C(HCO3-)C(OH-) |
| C(CO32-) |
| C(HCO3-)C(OH-) |
| C(CO32-) |
?②已知25℃时,Kh=2×10-4mol/L,则当溶液中c(HCO3-):c(CO32-)=2:1时,试求溶液的pH=
?③0.1mol/L Na2CO3溶液中c(OH-)-c(H+)=
(3)汽车尾气的主要成分是一氧化碳和氮氧化物,治理尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2NO(g)+2CO(g)?N2(g)+2CO2(g);△H<0.
若在一定温度下,将2molNO、lmolCO充入固定容积的容器中,反应过程中各物质的浓度变化如图所示.则从开始到达到平衡状态的过程中,平均反应速率v(CO2)=
| 5 |
| 144 |
| 5 |
| 144 |
①加入催化剂 ②降低温度 ③缩小容器体积 ④增加CO2的物质的量
A.只有①B.只有②C.只有③D.只有④