网址:http://m.1010jiajiao.com/timu_id_3207960[举报]
A
、B、C、D四种溶液分别是NaOH溶液、氨水、CH3COOH溶液 、盐酸中的一种.常温下:①
浓度均为0.1 mol·L-1的A和C溶液,pH:A<C<7;②
将1 L pH=3的A溶液分别与0.001 mol·L-1 xL B溶液、0.001 mol·L-1 yL D溶液充分反应至中性,x、y大小关系为:y<x;回答下列问题:
(1)D是________(填化学式)溶液;
(2)②中1 L pH=3的A溶液与0
.001 mol·L-1 xL B溶液充分反应至中性,所得溶液中各种离子的物质的量浓度由大到小的顺序为________.(3)常温下,等体积且等物质的量浓度的C溶液和D溶液充分混合后所得溶液的pH________7(填“>”、“<”或“=”),用离子方程式解释其原因________.
(4)向pH相同且等体积的两份溶液A和C中,分别投入质量不同的锌粉反应,若放出氢气的质量相同,则下列说法正确的是________(填写序号).
①开始反应时的速率A>C
②反应所需要的时间C>A
③参加反应的锌粉物质的量A=C
④A溶液里有锌粉剩余
(10分)A、B、C、D四种溶液分别是NaOH溶液、氨水、 CH3COOH溶液 、盐酸中的一种。常温下:
①浓度均为0.1mol·L-1的A和C溶液,pH:A<C<7;
②将1L pH=3的A溶液分别与0.001mol·L-1 xL B溶液、0.001mol·L-1 yL D溶液充分反应至中性,x、y大小关系为: y<x;
回答下列问题:
(1)D是 (填化学式)溶液;
(2)②中1LpH=3的A溶液与0.001mol·L-1 xL B溶液充分反应至中性,所得溶液中各种离子的物质的量浓度由大到小的顺序为 。
(3)常温下,等体积且等物质的量浓度的C溶液和 D溶液充分混合后所得溶液的pH
7(填“>”、“<”或“=”),用离子方程式解释其原因 。
(4)向pH相同且等体积的两份溶液A和C中,分别投入质量不同的锌粉反应,若放出氢气的质量相同,则下列说法正确的是 (填写序号)。
①开始反应时的速率A>C ②反应所需要的时间C>A
③参加反应的锌粉物质的量A=C ④A溶液里有锌粉剩余
查看习题详情和答案>>
(10分)A、B、C、 D四种溶液分别是NaOH溶液、氨水、 CH3COOH溶液、盐酸中的一种。常温下:
①浓度均为0.1mol·L-1的A和C溶液,pH:A<C<7;
②将1 L pH=3的A溶液分别与0.001mol·L-1 xL B溶液、0.001mol·L-1 yL D溶液充分反应至中性,x、y大小关系为: y<x;
回答下列问题:
(1)D是 (填化学式)溶液;
(2)②中1LpH=3的A溶液与0.001mol·L-1 xL B溶液充分反应至中性,所 得溶液中各种离子的物质的量浓度由大到小的顺序为 。
得溶液中各种离子的物质的量浓度由大到小的顺序为 。
(3)常温下,等体积且等物质的量浓度的C溶液和D溶液充分混合后所得溶液的pH
7(填“>”、“<”或“=”),用离子方程式解释其原因 。
(4)向pH相同且等体积的两份溶液A和C中,分别投入质量不同的锌粉反应,若放出氢气的质量相同,则下列说法正确的是 (填写序号)。
①开始反应时的速率A>C ②反应所需要的时间C>A
③参加反应的锌粉物质的量A="C " ④A溶液里有锌粉剩余
(10分)A、B、C、 D四种溶液分别是NaOH溶液、氨水、 CH3COOH溶液 、盐酸中的一种。常温下:
①浓度均为0.1mol·L-1的A和C溶液,pH:A<C<7;
②将1 L pH=3的A溶液分别与0.001mol·L-1 xL B溶液、0.001mol·L-1 yL D溶液充分反应至中性,x、y大小关系为: y<x;
回答下列问题:
(1)D是 (填化学式)溶液;
(2)②中1LpH=3的A溶液与0.001mol·L-1 xL B溶液充分反应至中性,所得溶液中各种离子的物质的量浓度由大到小的顺序为 。
(3)常温下,等体积且等物质的量浓度的C溶液和 D溶液充分混合后所得溶液的pH
7(填“>”、“<”或“=”),用离子方程式解释其原因 。
(4)向pH相同且等体积的两份溶液A和C中,分别投入质量不同的锌粉反应,若放出氢气的质量相同,则下列说法正确的是 (填写序号)。
①开始反应时的速率A>C ②反应所需要的时间C>A
③参加反应的锌粉物质的量A=C ④A溶液里有锌粉剩余
查看习题详情和答案>>
(1)铁屑表面少量的铁锈(主要成分为Fe2O3?a H2O )对制取硫酸亚铁有无影响
(2)FeSO4在不同温度下溶解度如下表所示:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 溶解度/g/100g水 | 18.5 | 20.8 | 26.3 | 32.8 | 40.1 | 48.4 | 52.4 | 50.9 | 43.7 |
(A)冷却 (B)蒸发
(C)结晶 (D)洗涤 (E)过滤
(3)以下是测定FeSO4?xH2O中结晶水含量的实验流程.(称量仪器为电子天平)
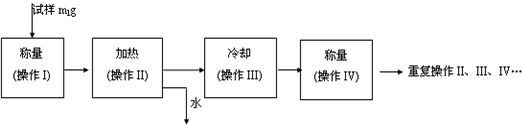
①其加热装置正确的是
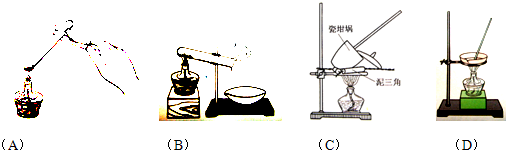
②重复操作II、III、IV,直到连续两次称量结果相差不超过
③操作III必须要在
(4)以下结晶水含量测定操作正确的是
A、加热时,晶体溅出坩埚,再加些FeSO4?xH2O
B、加热时,先用小火,后用大火加热至最后
C、加热时,不断用玻璃棒搅拌
D、恒重操作是指加热、冷却、称量这一过程重复两次
(5)实验中出现下列情况时,将对X值有何影响(填“偏大”、“偏小”或“无影响”):灼烧时有黑色固体出现