摘要:答案为A.D.[投影]例10已知一溶液中有四种离子:X+.Y-.H+.OH-.下列分析结果肯定错误的是 [ ]A.[Y-]>[X+]>[H+]>[OH-]B.[X+]>[Y-]>[OH-]>[H+]C.[H+]>[Y-]>[X+]>[OH-]D.[OH-]>[X+]>[H+]>[Y-]讨论分析:题目中四种离子在溶液中一定存在电荷守恒.即[X+]+[H+]=[Y-]+[OH-].根据此等式分析四个选项.对A选项[Y-]>[X+].必有[H+]>[OH-],对B选项[X+]>[Y-].必有[OH-]>[H+].才能使等式成立,对C选项[H+]>[Y-].必有[OH-]>[X+].所以C选项错误,对D选项[OH-]>[X+].必有[H+]>[Y-].这样等式成立.答案为C.[归纳]电解质溶液中离子浓度大小的比较尽管复杂.但解题关键是抓住平衡主线.认真分析并按照离子的电荷守恒.物料守恒理清关系.就可快速解答. 精选题
网址:http://m.1010jiajiao.com/timu_id_287881[举报]
已知一溶液中有四种离子:X+、Y-、H+、OH-,下列分析结果肯定错误的是( )
A.c(Y-)>c(X+)>c(H+)>c(OH-) B.c(X+)>c(Y-)>c(OH-)>c(H+)
C.c(H+)>c(Y-)>c(X+)>c(OH-) D.c(OH-)>c(X+)>c(H+)>c(Y-)
查看习题详情和答案>>已知一溶液中有四种离子:X+、Y-、H+、OH-,下列分析结果肯定错误的是( )
A.c(Y-)>c(X+)>c(H+)>c(OH-) B.c(X+)>c(Y-)>c(OH-)>c(H+)
C.c(H+)>c(Y-)>c(X+)>c(OH-) D.c(OH-)>c(X+)>c(H+)>c(Y-)
查看习题详情和答案>>已知一溶液中有四种离子:X+、Y-、H+、OH-,下列分析结果肯定错误的是
- A.c(Y-)>c(X+)>c(H+)>c(OH-)
- B.c(X+)>c(Y-)>c(OH-)>c(H+)
- C.c(H+)>c(Y-)>c(X+)>c(OH-)
- D.c(OH-)>c(X+)>c(H+)>c(Y-)
(2007?淄博三模)A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物.回答下列问题:
(1)常温下,X、Y的水溶液的pH均为5.则两种水溶液中由水电离出的H+浓度之比是
(2)A、B、D、E四种元素组成的某无机化合物,受热易分解.写出少量该化合物溶液与足量的Ba(OH)2溶液反应的离子方程式
(3)将铝片和镁片用导线相连,插入由A、D、E三种元素组成物质的稀溶液中构成原电池,则负极的电极反应式为
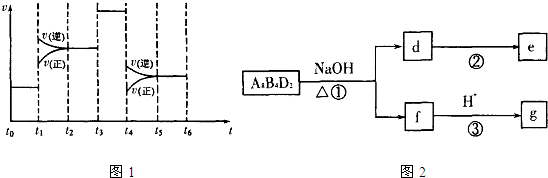
(4)化学反应3A2(g)+C2(g)?2CA3(g).当反应达到平衡时不断改变条件(不改变A2、C2和CA3的量),图1表示反应速率与反应过程的关系,其中表示平衡混合物中CA3的含量最高的一段时间是
(5)化合物A8B4D2有如图2转化关系.其中,g是常用调味品的主要成分.写出反应①的化学方程式
设计实验方案完成d→e的转化
查看习题详情和答案>>
(1)常温下,X、Y的水溶液的pH均为5.则两种水溶液中由水电离出的H+浓度之比是
10-4:1
10-4:1
.(2)A、B、D、E四种元素组成的某无机化合物,受热易分解.写出少量该化合物溶液与足量的Ba(OH)2溶液反应的离子方程式
Ba2++HCO3-+OH-═BaCO3↓+H2O
Ba2++HCO3-+OH-═BaCO3↓+H2O
.(3)将铝片和镁片用导线相连,插入由A、D、E三种元素组成物质的稀溶液中构成原电池,则负极的电极反应式为
Al+4OH-═AlO2-+2H2O+3e-
Al+4OH-═AlO2-+2H2O+3e-
.(4)化学反应3A2(g)+C2(g)?2CA3(g).当反应达到平衡时不断改变条件(不改变A2、C2和CA3的量),图1表示反应速率与反应过程的关系,其中表示平衡混合物中CA3的含量最高的一段时间是
t0~t1
t0~t1
.温度为T℃时,将4a mol A2和2a mol C2放入1L密闭容器中,充分反应后测得C2的转化率为50%,则反应的平衡常数| 4 |
| a2 |
| 4 |
| a2 |
(5)化合物A8B4D2有如图2转化关系.其中,g是常用调味品的主要成分.写出反应①的化学方程式
CH3COOC2H5+NaOH
CH3COONa+CH3CH2OH
| △ |
CH3COOC2H5+NaOH
CH3COONa+CH3CH2OH
| △ |
设计实验方案完成d→e的转化
取一根光洁铜丝绕成螺旋状,放在酒精灯外焰加热,然后伸入d中,反复几次,观察到铜丝由红→黑→红,并闻到液体有刺激性气味
取一根光洁铜丝绕成螺旋状,放在酒精灯外焰加热,然后伸入d中,反复几次,观察到铜丝由红→黑→红,并闻到液体有刺激性气味

科学家从化肥厂生产的(NH4)2SO4中检出组成为N4H4(SO4)2的物质.经测定,该物质易溶于水,在水中以SO42-和N4H44+两种离子形式存在,植物的根系极易吸收N4H44+,但它遇到碱时,会生成一种形似白磷的N4分子,N4分子不能被植物吸收.请回答下列问题:
(1)N4和N2的关系正确的是 (填序号)
(A)同种单质 (B)同位素
(C)同分异构体 (D)同素异形体
(2)N4H4(SO4)2 (填“能”或“不能”)和草木灰(主要成分为碳酸钾)混合施用.
(3)已知液氨中存在着下列平衡:2NH3?NH4++NH2-.科学家在液氨中加入氢氧化铯(CsOH)和特殊的吸水剂,使液氨中的NH4+生成N4分子,请写出液氨与氢氧化铯反应的化学方程式: .
查看习题详情和答案>>
(1)N4和N2的关系正确的是
(A)同种单质 (B)同位素
(C)同分异构体 (D)同素异形体
(2)N4H4(SO4)2
(3)已知液氨中存在着下列平衡:2NH3?NH4++NH2-.科学家在液氨中加入氢氧化铯(CsOH)和特殊的吸水剂,使液氨中的NH4+生成N4分子,请写出液氨与氢氧化铯反应的化学方程式: