网址:http://m.1010jiajiao.com/timu_id_28034[举报]
|
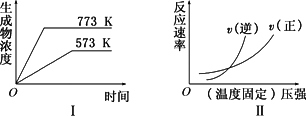
现有下列两个图象:
下列反应中符合上述图象的是 | |
| [ ] | |
A. |
N2(g)+3H2(g) |
B. |
2SO3(g) |
C. |
4NH3(g)+5O2(g) |
D. |
H2(g)+CO(g) |
|
现有下列四个图像
下列反应中全部符合上述图像的反应是 | |
| [ ] | |
A. |
N2(g)+3H2(g) |
B. |
2SO3(g) |
C. |
4NH3(g) +5O2(g) |
D. |
H2(g) +CO(g) |
|
下列可逆反应达平衡后,升高温度可使混合气的平均分子量增大的是 | |
| [ ] | |
A. |
N2(g)+3H2(g) |
B. |
H2(g)+I2(g) |
C. |
2SO3(g) |
D. |
4NH3(g)+5O2(g) |
下图为某化学反应速率—时间图。在t1时刻升高温度或增大压强,都符合下图所示变化的反应是 ( )

A.2SO2 (g)+O2 (g) ![]() 2SO3 (g) ;△H<0
2SO3 (g) ;△H<0
B.4NH3 (g)+5O2 (g) ![]() 4NO(g)+6H2O (g) ;△H<0
4NO(g)+6H2O (g) ;△H<0
C.H2 (g)+I2 (g) ![]() 2HI (g) ;△H>0
2HI (g) ;△H>0
D.C (s)+H2O (g) ![]() CO (g)+H2 (g) ;△H>0
CO (g)+H2 (g) ;△H>0
自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO.
(1)在不同温度下,反应N2(g)+O2(g)![]() 2NO(g) ΔH=a kJ·mol-1
2NO(g) ΔH=a kJ·mol-1
![]()
①该反应的ΔH________0
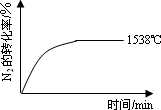
(填“>”、“=”或“<”).②其他条件相同时,在上述三个温度下分别发生该反应.1538℃时,N2的转化率随时间变化如图所示,请补充完成1760℃时N2的转化率随时间变化的示意图.
(2)
科学家一直致力于研究常温、常压下“人工固氮”的新方法.曾有实验报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3.相应的热化学方程式如下:2N2(g)+6H2O(1)=4NH3(g)+3O2(g) ΔH=+1530kJ·mol-1
则氨催化氧化反应4NH3(g)+5O2(g)=4NO(g)+6H2O(1)的反应热ΔH=________.(用含a的代数式表示)
(3)最近一些科学家研究采用高质子导电性的SCY陶瓷(能传递H+)实现氮的固定——氨的电解法合成,大大提高了氮气和氢气的转化率.总反应式为:N2+3H2 2NH3.则在电解法合成氨的过程中,
2NH3.则在电解法合成氨的过程中,
(4)合成氨的反应N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92、4 kJ·mol-1,一定条件下的密闭容器中,该反应达到平衡,要提高N2的转化率,可以采取的措施是________(填字母代号).
2NH3(g) ΔH=-92、4 kJ·mol-1,一定条件下的密闭容器中,该反应达到平衡,要提高N2的转化率,可以采取的措施是________(填字母代号).
a、升高温度
b、加入催化剂
c、增加H2的浓度
d、增加N2的浓度
e、分离出NH3
(5)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应后溶液中c(NH4+)=c(Cl-),则溶液显________性(填“酸”“碱”或“中”),可推断a________0.01(填大于、等于或小于).