摘要:§(2)硝酸盐(3)硝酸:4HNO3=====2H2O+4NO2↑+O2↑
网址:http://m.1010jiajiao.com/timu_id_233338[举报]
 2009年7月21日,山东省某金矿发生硝酸泄露事故.由于浓硝酸易挥发且不稳定,事故发生时,有大量黄色、刺激性气味的烟雾产生.消防官兵到达后,立即对泄露硝酸进行处理(大量抛洒某种固体粉末等),及时地消除了事故带来的危害.
2009年7月21日,山东省某金矿发生硝酸泄露事故.由于浓硝酸易挥发且不稳定,事故发生时,有大量黄色、刺激性气味的烟雾产生.消防官兵到达后,立即对泄露硝酸进行处理(大量抛洒某种固体粉末等),及时地消除了事故带来的危害.(1)请用化学方程式解释烟雾呈黄色的原因:
4HNO3
4NO2↑+O2↑+2H2O
| ||
4HNO3
4NO2↑+O2↑+2H2O
.
| ||
(2)消防官兵向泄露的硝酸抛洒的粉末可能是
A
A
.A.生石灰;B.铁粉;C.食盐;D.石膏
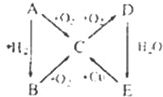
(3)若图中的E物质代表硝酸,请按要求表示下列转化:
B→C的化学方程式:
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
;
| ||
| △ |
D→E的化学方程式:
3NO2+H2O=2HNO3+NO
3NO2+H2O=2HNO3+NO
;E→C的离子方程式:
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
.已知KNO3、Cu(NO3)2、AgNO3三种硝酸盐热分解的反应方程式如下(条件都是加热):
①2KNO3=2KNO2+O2↑
②2Cu(NO3)2=2CuO+4NO2↑+O2↑
③2AgNO3=2Ag+2NO2↑+O2↑
今有某固体可能由上述三种硝酸盐中的一种或几种组成.取适量该固体充分加热,得到一定量的气体,将这些气体通入水中,结果全部被吸收,没有剩余,回答:
(1)该固体是否可能只由一种盐组成?若可能,指出是哪种盐,若不可能,说明原因.
(2)若固体是混合物,指出它的可能组成(即物质的量之比),若没有这种组成,也请说明
查看习题详情和答案>>
①2KNO3=2KNO2+O2↑
②2Cu(NO3)2=2CuO+4NO2↑+O2↑
③2AgNO3=2Ag+2NO2↑+O2↑
今有某固体可能由上述三种硝酸盐中的一种或几种组成.取适量该固体充分加热,得到一定量的气体,将这些气体通入水中,结果全部被吸收,没有剩余,回答:
(1)该固体是否可能只由一种盐组成?若可能,指出是哪种盐,若不可能,说明原因.
可能,Cu(NO3)2分解所得NO2、O2物质的量之比为4:1,通入水中发生反应:4NO2+O2+2H2O=4HNO3,全部吸收
可能,Cu(NO3)2分解所得NO2、O2物质的量之比为4:1,通入水中发生反应:4NO2+O2+2H2O=4HNO3,全部吸收
.(2)若固体是混合物,指出它的可能组成(即物质的量之比),若没有这种组成,也请说明
没有这种组成.由(1)可知,只有当NO2、O2物质的量之比为4:1时才可能被完全吸收,若为混合物,则不可能出现4:1的情况,因此不会有这种组成
没有这种组成.由(1)可知,只有当NO2、O2物质的量之比为4:1时才可能被完全吸收,若为混合物,则不可能出现4:1的情况,因此不会有这种组成
.雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生.根据题意完成下列填空:
(1)As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体.若As2S3和SnCl2正好完全反应,As2S3和SnCl2的物质的量之比为
(2)上述反应中的氧化剂是
(3)As2S3和HNO3有如下反应:As2S3+10H++10NO3-=2H3AsO4+3S+10NO2↑+2H2O,若生成2mol H3AsO4,则反应中转移电子的物质的量为
(4)若反应产物NO2与11.2L O2(标准状况)混合后用水吸收全部转化成浓HNO3,然后与过量的碳反应,所产生的CO2的量
A.小于0.5mol B.等于0.5mol C.大于0.5mol D.无法确定
(信息:碳粉与浓硝酸反应:C+4HNO3(浓)═CO2↑+4NO2↑+2H2O )
查看习题详情和答案>>
(1)As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体.若As2S3和SnCl2正好完全反应,As2S3和SnCl2的物质的量之比为
1:1
1:1
.(2)上述反应中的氧化剂是
As2S3
As2S3
,反应产生的气体可用NaOH溶液
NaOH溶液
吸收.(3)As2S3和HNO3有如下反应:As2S3+10H++10NO3-=2H3AsO4+3S+10NO2↑+2H2O,若生成2mol H3AsO4,则反应中转移电子的物质的量为
10mol
10mol
.(4)若反应产物NO2与11.2L O2(标准状况)混合后用水吸收全部转化成浓HNO3,然后与过量的碳反应,所产生的CO2的量
A
A
(选填编号).A.小于0.5mol B.等于0.5mol C.大于0.5mol D.无法确定
(信息:碳粉与浓硝酸反应:C+4HNO3(浓)═CO2↑+4NO2↑+2H2O )