网址:http://m.1010jiajiao.com/timu_id_21631[举报]
实验室制取O2,某同学按如下步骤设计:①连接仪器 ②装药品 ③将装有药品的试管固定在铁架台上 ④检查装置的气密性 ⑤加热 ⑥用排水法收集一瓶氧气 ⑦熄灭酒精灯 ⑧将导管移出水面.问该同学的操作是否有误?____若有错误,请你将正确操作顺序写出来(按序号排列)____,若最后两步操作顺序错了,会有什么后果?____.
查看习题详情和答案>>
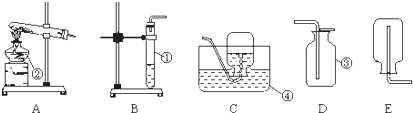
(1)写出仪器名称:①
(2)实验室采用装置A制取氧气时,其试管中应放的药品是
(3)采用装置B制取氧气时,其试管中应放的药品是
| ||
| ||
(4)收集氧气可以选择装置
(5)某同学收集完毕,先停止加热再将导管移出水面,你预测这种操作会引起什么后果
(6)以下是实验步骤,将步骤的序号按正确的先后次序排列为
A、点燃酒精灯加热 B、检查气密性 C、熄灭酒精灯 D、向试管中装入药品
E、收集气体 F、将试管固定在铁架台上 G、从水中撤离导管.
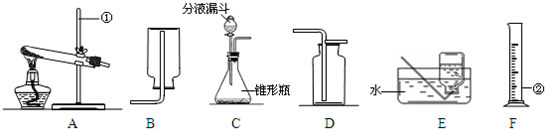
(1)写出标号仪器的名称 ①
(2)实验制取氧气常采用分解过氧化氢溶液的方法,选择的发生装置为
①产物无污染 ②不需加热 ③需加热 ④生成物只有氧气
(3)乙同学用大理石和稀盐酸反应来制取二氧化碳,其反应的文字表达式为
(4)某化学兴趣小组的同学,利用下列仪器进行实验(所有装置的气密性都已检查完毕)
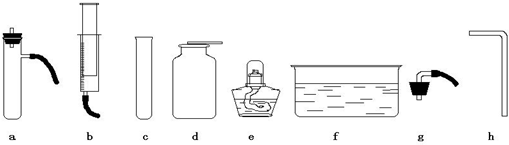
①把过氧化氢溶液缓缓加入盛有二氧化锰的容器中制取并用排气法收集氧气,完成该实验你所选用的仪器有
写出发生反应的化学符号表达式
| MnO2 |
| MnO2 |
②某同学继续探究“红砖粉末是否也可以作过氧化氢分解反应的催化剂?”实验步骤和现象如下:
a、他分别向两支试管中加入相同的过氧化氢溶液,向其中一支试管加入一药匙红砖粉末,然后将两支试管中的气体导出通入水中比较产生气泡的快慢,发现加入红砖粉末的试管中反应较快.
b、将反应较快的试管内固体过滤出来,洗涤、烘干、称量.
c、用称量后的固体重复步骤a的实验,现象与步骤a完全相同.
试回答:步骤a中他除了选用试管外还用到上面列出的仪器有
(5)在学习中我们了解到常用制取氧气的方法有如图所示的四种:
请回答问题:在实验室按绿色化学的要求你认为那种制取氧气的方法较好的是
| △ |
| △ |
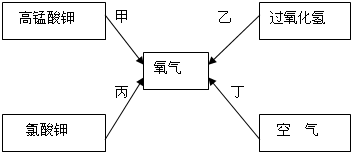
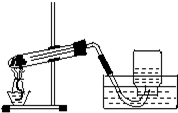 如图是某同学在实验室加热高锰酸钾制取氧气,用排水法收集的装置图,并试验O2的性质.
如图是某同学在实验室加热高锰酸钾制取氧气,用排水法收集的装置图,并试验O2的性质.(1)请改正图中的错误.
①
(2)高锰酸钾受热制取氧气的反应文字表达式是
| 加热 |
| 加热 |
(3)用排水法开始收集氧气的适宜时刻是
(4)以下是实验步骤,将步骤的序号按正确的先后次序排列为
①点燃酒精灯加热 ②检查气密性 ③熄灭酒精灯 ④向试管中装入药品
⑤收集气体 ⑥将试管固定在铁架台上 ⑦从水中撤离导管
(5)用排水法收集氧气完毕后,应先
(6)下图所示是木炭在氧气中燃烧的实验操作,试回答下列问题:
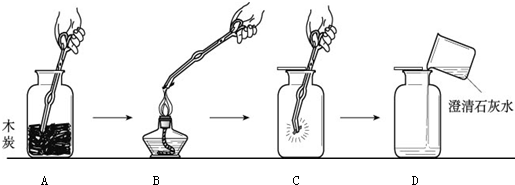
做木炭在氧气中燃烧的实验时,如果一开始就把红热的木炭很快地插入盛氧气的集气瓶下部,会出现的后果是
(7)做铁丝在氧气中燃烧的实验时,把铁丝绕成螺旋状,前端系一根火柴,其作用是
| 点燃 |
| 点燃 |
根据下图回答问题。
 |
(1)仪器a的名称是 。
(2)实验室制取二氧化碳所选用的发生装置是 (填装置序号,下同),不选择装置E收集二氧化碳的原因是______________________。
(3)实验室用高锰酸钾制取氧气反应的化学方程式是 _____________________ ,
所选用的收集装置是E或 。主要的实验步骤有:①加热 ②装药品并固定
试管 ③检查装置的气密性 ④用排水法收集氧气 ⑤停止加热 ⑥将导管从水
槽中取出。正确的操作顺序是 _____________ (用序号表示)。
(1)酒精灯(2)B 二氧化碳能溶于水且与水反应(只答一点给分)
|
32.(5分)32.(5分)某化学小组测定空气中氧气的体积分数。
 (1)根据右图回答问题。
(1)根据右图回答问题。
①红磷燃烧的化学方程式为__________________________________。
②若将红磷改为木炭,反应结束后降至室温,打开止水夹,烧杯
中的水不倒吸入集气瓶的原因是______________________________
 _______________________________________________。
_______________________________________________。
(2)用四硫化钠(Na2S4)固体可替代红磷测定空气中氧气的体积分数。
反应原理为:2Na2S4+O2+2H2O 8S↓+4NaOH(氢氧化钠)。
小资料:四硫化钠(Na2S4)与氧气、水反应生成难溶于水的固体硫(S)和易溶于水
的氢氧化钠。
【实验过程】
①取足量的四硫化钠固体加入试管中,再加入适量的水,迅速塞紧橡胶塞,充分振荡。测量液面至橡胶塞下沿的距离,记录数据h1(如图1所示)。

图1 图2
②将该试管插入水中(如图2所示),拔下橡胶塞,观察到__________,塞紧橡胶塞。将试管取出,倒转过来,测量液面至橡胶塞下沿的距离,记录数据h2。理论上h2∶h1= 。
③按照①和② 再重复实验2次。3次实验数据如下表所示。
再重复实验2次。3次实验数据如下表所示。
| 第1次 | 第2次 | 第3次 | |
| h1/cm | 11.0 | 11.4 | 11.6 |
| h2/cm | 8.7 | 9.1 | 9.2 |
根据第3次实验数据,计算空气中氧气的体积分数为 %(结果精确到 0.1%)。
(1)①4P + 5O 2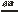 2P2O5
2P2O5
② 因为木炭燃烧生成二氧化碳气体,集气瓶内气体体积不变,瓶内气体压强没有明显变
因为木炭燃烧生成二氧化碳气体,集气瓶内气体体积不变,瓶内气体压强没有明显变
化,所以,当打开止水夹时水不会吸入到集气瓶中。
(2)②试管内液面上升至液面高度不再改变 79∶100(或4∶5)  ③ 20.7
③ 20.7
33.(8分)某兴趣小组同学阅读课外资料得知:很多因素都能影响过氧化氢分解速度。于是,
同学们探究影响过氧化氢分解速度的某种因素。
【实验过程】实验数据记录如下:
| 过氧化氢溶液的质量 | 过氧化氢溶液的浓度 | MnO2的质量 | 测量数据 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9 mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16 mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31 mL |
【实验分析】
(1)过氧化氢分解的化学方程式为______________________________________。
(2)表格中的“测量数据”的指的是:相同时间内_________________________________。
(3)本实验中,测量O2体积的装置是________(填编号)。
 |
【实验结论】
在相同条件下______________________________________________。
【交流评价】
(1)甲同学提出在上述实验中测量______________同样能得出相同的结论。
 (2)乙同学提出用右图装置进行实验,通过比较_____________
(2)乙同学提出用右图装置进行实验,通过比较_____________
___________________也能达到实验目的。
【实验反思】
除了上述因素会影响过氧化氢分解速度外, ___________(写
一种)也会影响过氧化氢分解速度,你的实验方案是______________________________________________________________________。
查看习题详情和答案>>