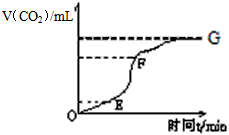
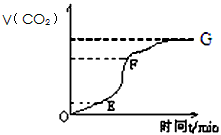摘要:实验过程如下图所示.分析判断: 段化学反应速率最快. 段收集的二氧化碳气体最多.为了减缓上述反应的速率.欲向溶液中加入下列物质.你认为可行的是 A.蒸馏水 B.氯化钠固体C.氯化钠溶液 D.浓盐酸
网址:http://m.1010jiajiao.com/timu_id_209760[举报]
一、二、选择题:
题号
1
2
3
4
5
6
7
8
9
10
11
12
答案
C
C
D
B
B
A
D
B
AB
BD
CD
C
三、13. 0.02mol?(L.s)-1
14.(1)EF、EF;(2)AC;(3)改用较大块的碳酸钙固体,或用与盐酸不反应的东西将碳酸钙部分包住,或加入醋酸钠溶液等。
15.(1)①镁片上有大量气泡产生 ②镁片逐渐溶解 ③烧杯中溶液变混浊
(2)镁与盐酸反应产生氢气,该反应为放热反应,Ca(OH)2在水中的溶解度随温度升高而减小,故析出Ca(OH)2晶体。
(3)Mg+2H+==Mg2++H2↑
(4)小于
16.(1)D;(2)加入硫酸铜溶液后,构成Fe-Ag原电池,Fe溶解,减轻,Cu2+在银圈上得到电子,沉积在其上,增重,所以银圈向下倾斜。
四、17.
18.(1)C6H12O6(s)+6O2(g)→6CO2(g)+6H2O(l);△H=-2560KJ/mol
(2)能量的利用率:45.4%
\
用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,请回答:
(1)实验过程如下图所示,分析判断:________段化学反应速率最快, _________段收集的二氧化碳最多。
(1)实验过程如下图所示,分析判断:________段化学反应速率最快, _________段收集的二氧化碳最多。
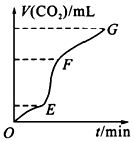
(2)为了减缓上述反应的化学反应速率,欲向溶液中加入下列物质,你认为可行的是___________。
A.蒸馏水 B.NaCl固体 C.NaCl溶液 D.浓盐酸
(3)除了上述方法外,你认为还可以采取哪些措施来减缓化学反应速率?
_________________________________
查看习题详情和答案>>
A.蒸馏水 B.NaCl固体 C.NaCl溶液 D.浓盐酸
(3)除了上述方法外,你认为还可以采取哪些措施来减缓化学反应速率?
_________________________________
 用纯净的锌粒与稀盐酸反应制取氢气气体,请回答:
用纯净的锌粒与稀盐酸反应制取氢气气体,请回答:(1)实验过程如下图所示,分析判断
EF
EF
段化学反应速率最快,EF
EF
段收集的氢气最多.(2)将锌粒投入盛有稀盐酸的烧杯中,刚开始时产生H2的速率逐渐加快,其影响因素是
该反应是放热反应,温度升高,反应速率加快
该反应是放热反应,温度升高,反应速率加快
,一定时间后反应速率逐渐减慢,其原因是随着反应的进行,盐酸的浓度逐渐减小,反应速率逐渐减小
随着反应的进行,盐酸的浓度逐渐减小,反应速率逐渐减小
.(3)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是
ACE
ACE
A.蒸馏水 B.氯化钠固体 C.氯化钠溶液 D.浓盐酸 E.降低温度
(4)EF段产生H2的反应速率为
7.0
7.0
mL?min-1.用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,请回答
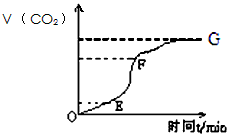
(1)实验过程如下图所示,分析判断:________段化学反应速率最快,_______段收集的二氧化碳气体最多。
(2)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是____________
A.蒸馏水 B.氯化钠固体 C.氯化钠溶液 D.浓盐酸
(3)除了上述方法外,你认为还可以采取哪些措施来减缓化学反应速率?(至少回答两种)
________________________________。
查看习题详情和答案>>
(2)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是____________
A.蒸馏水 B.氯化钠固体 C.氯化钠溶液 D.浓盐酸
(3)除了上述方法外,你认为还可以采取哪些措施来减缓化学反应速率?(至少回答两种)
________________________________。