网址:http://m.1010jiajiao.com/timu_id_193977[举报]
1
2
3
4
5
6
7
8
9
C
C
B
D
B
D
B
C
D
10
11
12
13
14
15
16
17
18
D
C
D
B
B
D
B
B
A
19
20
21
22
23
24
25
――
――
A
B
D
B
C
C
A
26、(14分)
⑴电解池 ,原电池 (2分,各1分)
2H2O+2CuSO4 = 2Cu+O2↑+2H2SO4 (5分,第一空1分,其它各2分)
(3)0.02 ,增加 ,0.63 , 1 。(7分,第二空1分,其它各2分)
27、(10分)
(1)Fe3++3H2O Fe(OH)3+3H+ ,将FeCl3先溶于盐酸,然后再加水稀释 。
Fe(OH)3+3H+ ,将FeCl3先溶于盐酸,然后再加水稀释 。
碳酸钙消耗了H+,使Fe3+水解程度增大,形成Fe(OH)3沉淀。(6分,各2分)
(2)白色悬浊液逐渐转变为黑色悬浊液。2AgCl(s)+S2―=Ag2S(s)+2Cl―。(4分,各2分)
28.(9分)
(1)增大 (2分)(2) 15―20min、25―30min 。(2分)
(3) 增大氧气的浓度,a、b。(3分,第二空2分,多选不给分)
(4)不 、向左。(2分,各1分)
29.(11分)
(1)①转移,定容 ②烧杯(或表面皿)、药匙。(4分,各1分)
(2)①溶液从无色恰好变为红色,且半分钟内不褪去。
②0.11mol?L-1 ③ 丙 ④ D (7分,第三空1分,其它各2分)
30.(6分)(1)0.04 mol?L-1?min-1、80% (2)16%
(算出反应速率且过程正确的给4分,转化率和体积分数各给1分)
NO很容易与许多分子迅速发生反应,科学家发现在生物体中不断地产生NO,用于在细胞和细胞间传递信息;NO还参与心血管系统、免疫系统以及中枢和外围神经系统的调控.
(1)实验室用金属铜和稀硝酸制取NO的离子方程式为________.
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示.
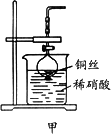
①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝状材料包裹铜粒以代替铜丝进行实验,这种丝状材料的成分可以是________(填选项编号)
A.铁
B.铝
C.铂
D.玻璃
②打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是________(写化学方程式).
(3)为证明铜丝与稀硝酸反应生成的确实是NO,某学生另设计了一套如图乙所示的装置制取NO.反应开始时,可以在U形管右端观察到无色的NO气体.
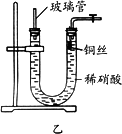
长玻璃管的作用是________.
(4)假设实验中12.8 g Cu全部溶解,需要通入标准状况下________mL O2才能使NO全部溶于水.
(5)用金属铜制取硝酸铜,从节约原料和防止环境污染的角度考虑,下列4种方法中最好的是________(填“甲”“乙”“丙”或“丁”),理由是________.
甲:铜![]() 硝酸铜
硝酸铜
乙:铜![]() 硝酸铜
硝酸铜
丙:铜![]() 氯化铜
氯化铜![]() 硝酸铜
硝酸铜
丁:铜![]() 氧化铜
氧化铜![]() 硝酸铜
硝酸铜
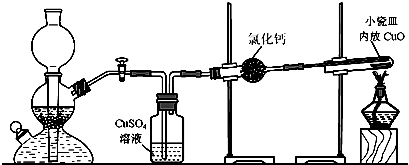
(1)在启普发生器中纯锌与稀硫酸反应过于缓慢,可采取的加快速率的措施是①适当增大硫酸的浓度,②
(2)用纯度不高的锌(粗锌)制取氢气,反应速率快,但制得的氢气因含H2S等还原性杂质而有难闻的气味,CuSO4洗气瓶中观察到的现象是
(3)有同学发现粗锌与稀硫酸反应一段时间后,锌粒表面变黑,于是收集了少量该黑色固体,验证黑色固体含铁元素的简单化学方法
(4)实验中得到的数据有:小瓷皿的质量mg,小瓷皿加样品的质量n g,反应后小瓷皿加固体的质量w g,已知氧的相对原子质量为16,则铜的相对原子质量是
| 16(w-m) |
| n-w |
| 16(w-m) |
| n-w |
(5)某次实验中测定结果明显偏大,可能的原因是
a.未充分冷却即停止通氢气 b.氧化铜样品中含有氯化铵杂质
c.反应后固体中有少量Cu2O d.氢气不干燥有少量水分
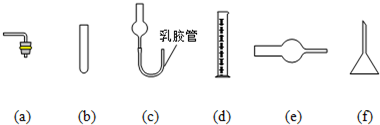
(6)由于启普发生器药品用量较多,利用下列仪器装配一套有启普发生器功能的简易装置,你选择
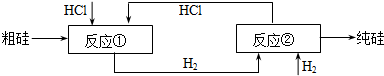
反应①:Si(粗)+3HCl(g)
| ||
反应②:SiHCl3+H2
| ||
(1)制备三氯氢硅的反应为:Si(s)+3HCl(g)═SiHCl3(g)+H2(g);△H=-210kJ?mol-1.伴随的副反应有:Si(s)+4HCl(g)═SiCl4(g)+2H2(g);△H=-241kJ?mol-1.SiCl4在一定条件下与H2反应可转化为SiHCl3,反应的热化学方程式为:SiCl4(g)+H2(g)═SiHCl3(g)+HCl(g);△H=
(2)假设在每一轮次的投料生产中,硅元素没有损失,反应①HCl中的利用率为75%,反应②中和H2的利用率为80%.则在下一轮次的生产中,需补充投入HCl和H2的体积比是
(3)由于SiH4具有易提纯的特点,因此硅烷热分解法是制备高纯硅很有发展潜力的方法.工业上广泛采用的合成硅烷方法是让硅化镁和固体氯化铵在液氨介质中反应得到硅烷,化学方程式是
整个制备过程必须严格控制无水,否则反应将不能生成硅烷,而是生成硅酸和氢气等,其化学方程式为
整个系统还必须与氧隔绝,其原因是
(4)若将硅棒与铁棒用导线相连浸在氢氧化钠溶液中构成原电池,则负极的电极反应式为:
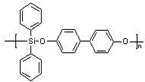
(5)硅能用于合成硅橡胶,右图是硅橡胶中的一种,其主要优点是玻璃化温度低,耐辐射性能好,则该硅橡胶的化学式为
有机物A的分子式为C9H10O2,A在光照条件下生成的一溴代物B,可发生如下转化关系(无机产物略):
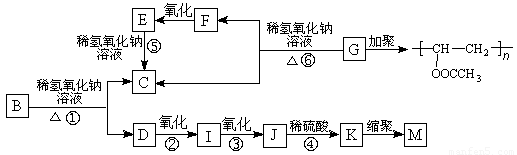
其中K物质与氯化铁溶液发生显色反应,且环上的一元取代物只有两种结构。
已知:①当羟基与双键碳原子相连时,易发生如下转化:RCH=CHOH→RCH2CHO;
②-ONa连在烃基上不会被氧化。
请回答下列问题:
(1)F与I中具有相同的官能团,该官能团的名称是??????????????? 。
(2)上述变化中属于水解反应的是???????????????????? (填反应编号)。
(3)写出结构简式,G:??????????????????? ,M:????????????????????????? 。
(4)写出反应①的化学方程式:???????????????????????????????????????????????????????? 。
(5)任写一种符合下列要求的A的同分异构体?????????????????????????????? 。
I.含有苯环???? II.能发生银镜反应,且能使氯化铁溶液显紫色
III.苯环上的一元取代物只有一种
查看习题详情和答案>>
有机物A的分子式为C9H10O2,A在光照条件下生成的一溴代物B,可发生如下转化关系(无机产物略):
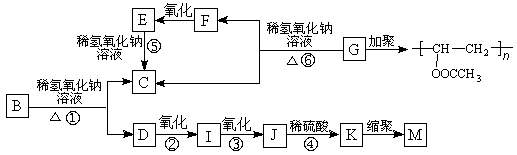
其中K物质与氯化铁溶液发生显色反应,且环上的一元取代物只有两种结构。
已知:①当羟基与双键碳原子相连时,易发生如下转化:RCH=CHOH→RCH2CHO;
②-ONa连在烃基上不会被氧化。
请回答下列问题:
(1)F与I中具有相同的官能团,该官能团的名称是 。
(2)上述变化中属于水解反应的是 (填反应编号)。
(3)写出结构简式,G: ,M: 。
(4)写出下列反应的化学方程式:
F E
:
E
:
反应①: ,
(5)写出所有符合下列要求的A的同分异构体 。
I.含有苯环 II.能发生银镜反应,且能使氯化铁溶液显紫色
III. 苯环上的一元取代物只有一种
查看习题详情和答案>>
