摘要:答案:(1)一定要将浓H2SO4沿内壁缓缓注入盛有浓HNO3的烧杯中.并不断搅拌.冷却(2)50℃-60℃水浴加热(3)分液漏斗(4)洗去粗产品中的酸性杂质(5)C 解析:(1)硝基苯的制备中.加入药品必须将浓硫酸加入浓硝酸中.这相当于是浓硫酸的稀释,(2)水浴加热有助于控制温度.且受热均匀,(3)两种不相溶的液体可用分液的方法,(4)粗产品用NaOH溶液洗涤主要是为了洗去溶于溴苯中的Br2.
网址:http://m.1010jiajiao.com/timu_id_186270[举报]
 (1)下列关于实验操作的叙述中正确的为
(1)下列关于实验操作的叙述中正确的为②⑤⑥⑦
②⑤⑥⑦
.(填序号)①从试剂瓶中取出的任何药品,若有剩余,不能再放回原试剂瓶
②可燃性气体点燃之前必须先验纯
③用胶头滴管向试管中滴加液体时,一定要将滴管伸入试管中
④在中和滴定的实验过程中,目光应注视滴定管中液面的变化
⑤蒸馏时,应使温度计水银球与蒸馏烧瓶支管口在同一水平线上
⑥分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
⑦配制浓硫酸和浓硝酸的混酸时,应将浓硫酸慢慢加到浓硝酸中,并及时搅拌和冷却
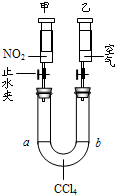
(2)在常温、常压下,注射器甲中装有NO2气体,注射器乙中装有同体积的空气(如图所示,夹持仪器均已略去).
①常温下,打开两个止水夹后,同时向外拉动两注射器的活塞,且拉动的距离相同,将会看到U型管中液面a
下降
下降
(升高、下降、不变);②如将注射器甲中的气体换成NH3,U型管中的CCl4换成水,仍在常温下,打开两个止水夹后,同时向里推动两注射器的活塞,且推动的距离相同,将会看到U型管中液面a
上升
上升
(升高、下降、不变).(3)下列仪器和装置,经过简单连接,可制备中学化学常见的多种不同的气体(暂不考虑尾气的吸收).
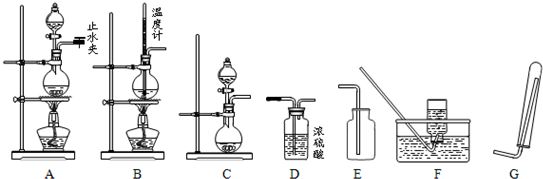
请回答下列问题:
(1)检验A装置气密性的操作为
关闭A装置的止水夹和分液漏斗的旋塞,向分液漏斗中加水.然后打开分液漏斗的旋塞,当少许水进入烧瓶后滴水停止,说明装置A不漏气
关闭A装置的止水夹和分液漏斗的旋塞,向分液漏斗中加水.然后打开分液漏斗的旋塞,当少许水进入烧瓶后滴水停止,说明装置A不漏气
.(2)若用橡胶管连接了装置“B→F”,可制备的气体为
CH2=CH2
CH2=CH2
.(3)若用橡胶管连接了装置“C→D→G”,可制备的气体为
H2
H2
.(4)若用橡胶管连接了装置“C→D→E”,则实验室制备该气体时发生反应的离子方程式为
CaCO3+2H+=Ca2++CO2↑+H2O
CaCO3+2H+=Ca2++CO2↑+H2O
.下列关于实验操作的叙述中正确的是( )
①从试剂瓶中取出的任何药品,若有剩余都不能再放回原试剂瓶
②可燃性气体点燃之前必须验纯
③用胶头滴管向试管中滴加液体,一定要将滴管伸入试管中
④用托盘天平称量固体药品时,应左物右码
⑤配制浓硫酸与蒸馏水的混合液时,应将浓硫酸慢慢加到蒸馏水中并及时搅拌和冷却
⑥选用100mL量筒量取4.0mL的稀硫酸.
①从试剂瓶中取出的任何药品,若有剩余都不能再放回原试剂瓶
②可燃性气体点燃之前必须验纯
③用胶头滴管向试管中滴加液体,一定要将滴管伸入试管中
④用托盘天平称量固体药品时,应左物右码
⑤配制浓硫酸与蒸馏水的混合液时,应将浓硫酸慢慢加到蒸馏水中并及时搅拌和冷却
⑥选用100mL量筒量取4.0mL的稀硫酸.
查看习题详情和答案>>
下列关于实验操作的叙述中正确的是……( )
①从试剂瓶中取出的任何药品,若有剩余不能再放回原试剂瓶;
②可燃性气体点燃之前必须检验纯度;
③用胶头滴管向试管中的加液体,一定要将滴管伸入试管中;
④在中和滴定的实验过程中,目光应注视滴定管中的液面;
⑤蒸馏时应使温度计水银球靠近蒸馏烧瓶支管处;
⑥分液时,分液漏斗中,下层液体从下口放出,上层液体从上口倒出;
⑦配制浓硫酸与浓硝酸的混酸时,应将浓硫酸慢慢加到浓硝酸中并及时搅拌和冷却;
⑧欲测某溶液的pH,需先用蒸馏水湿润pH试纸,再用洁净干燥的玻璃棒蘸取该溶液滴在试纸上,并与标准比色卡对比。
- A.①③④⑤⑥⑦
- B.①③④⑧
- C.②⑤⑥⑦
- D.以上答案均不正确。