摘要:25.(1)3Fe+4H2O Fe3O4+4H2 (2)防止暴沸(3)Fe+2Fe3+ㄔ3Fe2+ (4)验纯 关闭K3.打开K2在X处点燃氢气.挤压矿泉水瓶 (或 打开K3在X处点燃氢气 )
网址:http://m.1010jiajiao.com/timu_id_182236[举报]
 常温下,在没有氧气存在时,铁粉与水几乎不反应,但在高温下,铁粉能与水蒸气反应.
常温下,在没有氧气存在时,铁粉与水几乎不反应,但在高温下,铁粉能与水蒸气反应.(1)铁粉与水蒸气反应的化学方程式是
Fe3O4+4H2O
3Fe+4H2
| ||
Fe3O4+4H2O
3Fe+4H2
.
| ||
(2)停止反应,待装置冷却后,取出反应后的混合物,加入过量的稀硫酸充分反应,过滤.简述检验所得滤液中含有Fe3+的操作方法:
取少量滤液与试管中,滴入几滴KSCN溶液,若溶液变血红色,证明含有铁离子,否则无铁离子
取少量滤液与试管中,滴入几滴KSCN溶液,若溶液变血红色,证明含有铁离子,否则无铁离子
.(3)经检验上述滤液中不含Fe3+,这不能说明铁粉与水蒸气反应所得的产物中不含+3价的铁.原因是(结合化学方程式说明)
如果反应后的混合物中含有过量的铁粉,会发生反应2Fe3++Fe=3Fe2+,铁粉把铁离子全部还原为亚铁离子后滴入KSCN溶液不变红色
如果反应后的混合物中含有过量的铁粉,会发生反应2Fe3++Fe=3Fe2+,铁粉把铁离子全部还原为亚铁离子后滴入KSCN溶液不变红色
.(4)某同学利用上述滤液制取白色的Fe(OH)2沉淀,向滤液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色.
①沉淀由白色变为红褐色的化学反应方程式是
4Fe(OH)2+O2+2H2O=4Fe(OH)3
4Fe(OH)2+O2+2H2O=4Fe(OH)3
.②为了得到白色的Fe(OH)2沉淀,并尽可能较长时间保持白色沉淀,该同学设计了如图所示的装置:
请简述实验操作:
实验时先打开活塞K,再将分液漏斗的活塞打开,使稀硫酸与铁粉反应,用生成的氢气排出装置中的空气,然后关闭K,利用生成的氢气将试管中的硫酸亚铁溶液压入氢氧化钠溶液中,则可在盛氢氧化钠溶液的试剂瓶中较长时间保存白色氢氧化亚铁沉淀;
实验时先打开活塞K,再将分液漏斗的活塞打开,使稀硫酸与铁粉反应,用生成的氢气排出装置中的空气,然后关闭K,利用生成的氢气将试管中的硫酸亚铁溶液压入氢氧化钠溶液中,则可在盛氢氧化钠溶液的试剂瓶中较长时间保存白色氢氧化亚铁沉淀;
.
指出下列反应的氧化剂和还原剂,氧化产物和还原产物,写出被氧化和被还原的元素名称。
(1)3Fe+2O2![]() Fe3O4______________________________________________
Fe3O4______________________________________________
(2)H2S+3H2SO4(浓)![]() 4SO2↑+4H2O_____________________________________
4SO2↑+4H2O_____________________________________
(3)2KMnO4+16HCl(浓)![]() 2KCl+2MnCl2+5Cl2↑+8H2O
2KCl+2MnCl2+5Cl2↑+8H2O
______________________________________________
(4)2Na2O2+2CO2══2Na2CO3+O2_______________________________________
查看习题详情和答案>>我国是个钢铁大国,钢铁产量为世界第一,高炉炼铁是最为普遍的炼铁方法。高炉内可能发生如下反应:
C(s)+O2(g)=CO2(g) △H1=-393.5 kJ/mol ①
C(s)+CO2(g)=2CO(g) △H2=+172.5 kJ/mol ②
4CO(g)+Fe3O4(s)=4CO2(g)+3Fe(s) △H3=-13.7 kJ/mol ③
请回答下列问题:
(1)反应3Fe(s)+2O2(g)=Fe3O4(s)的△H=_____________。
(2)800℃时,C(s)+CO2(g) 2CO(g)的平衡常数K=1.64,测得高炉内c(CO)= 0. 20 mol/L、c(CO2)=
2CO(g)的平衡常数K=1.64,测得高炉内c(CO)= 0. 20 mol/L、c(CO2)=
0.05mol/L,此时反应向____(填“正”或“逆”)方向进行。
(3)某种矿石中铁元素以氧化物FemOn形式存在(矿石中杂质不与酸反应),现进行如下实验:将少量铁矿石样品粉碎,称取25.0 g样品于烧杯中,加入稀H2SO4充分溶解,并不断加热、搅拌,滤去不溶物。向所得滤液中加入10.0 g铜粉充分反应后过滤、洗涤、干燥得剩余固体36 g。剩下滤液用浓度为2
mol/L的酸性KMnO4滴定,至终点时消耗KMnO4溶液体积25.0 mL。提示:2Fe3++Cu=2Fe2++Cu2+
8H++MnO4-+5Fe2+=Mn2++5Fe3++4H2O
①计算该铁矿石中铁元素的质量分数。
②计算氧化物FemOn的化学式(m、n为正整数)(请写出计算过程)。
查看习题详情和答案>>
C(s)+O2(g)=CO2(g) △H1=-393.5 kJ/mol ①
C(s)+CO2(g)=2CO(g) △H2=+172.5 kJ/mol ②
4CO(g)+Fe3O4(s)=4CO2(g)+3Fe(s) △H3=-13.7 kJ/mol ③
请回答下列问题:
(1)反应3Fe(s)+2O2(g)=Fe3O4(s)的△H=_____________。
(2)800℃时,C(s)+CO2(g)
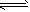 2CO(g)的平衡常数K=1.64,测得高炉内c(CO)= 0. 20 mol/L、c(CO2)=
2CO(g)的平衡常数K=1.64,测得高炉内c(CO)= 0. 20 mol/L、c(CO2)=0.05mol/L,此时反应向____(填“正”或“逆”)方向进行。
(3)某种矿石中铁元素以氧化物FemOn形式存在(矿石中杂质不与酸反应),现进行如下实验:将少量铁矿石样品粉碎,称取25.0 g样品于烧杯中,加入稀H2SO4充分溶解,并不断加热、搅拌,滤去不溶物。向所得滤液中加入10.0 g铜粉充分反应后过滤、洗涤、干燥得剩余固体36 g。剩下滤液用浓度为2
mol/L的酸性KMnO4滴定,至终点时消耗KMnO4溶液体积25.0 mL。提示:2Fe3++Cu=2Fe2++Cu2+
8H++MnO4-+5Fe2+=Mn2++5Fe3++4H2O
①计算该铁矿石中铁元素的质量分数。
②计算氧化物FemOn的化学式(m、n为正整数)(请写出计算过程)。
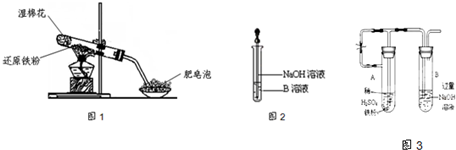
某同学利用如图1所示的实验装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质.
已知:①FeO+2H+=Fe2++H2O②Fe2O3+6H+=2Fe3++3H2O ③Fe3O4+8H+=Fe2++2Fe3++4H2O
请回答下列问题:
(1)硬质试管中发生反应的化学方程式为
(2)该同学欲确定反应一段时间后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的成分是(只有一个选项符合题意)
A.一定有Fe3O4,可能有Fe B.只有Fe(OH)3C.一定有Fe3O4和Fe
D.一定有Fe(OH)3,可能有FeE.只有Fe3O4
(3)该同学按上述实验方案进行了实验,结果溶液未变红色,原因是
(4)该同学马上另取少量溶液B,使其跟NaOH溶液反应.若按图2所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述现象相关的反应的化学方程式
(5)一段时间后,该同学发现(3)中未变红的溶液变成红色,说明Fe2+具有
(6)乙同学为了获得持久白色的Fe(OH)2沉淀,准备用图3所示装置,用不含O2的蒸馏水配制的NaOH溶液与新制的FeSO4溶液反应.获得不含O2的蒸馏水的方法是
一段时间后,关闭止水夹,在试管
查看习题详情和答案>>

已知:①FeO+2H+=Fe2++H2O②Fe2O3+6H+=2Fe3++3H2O ③Fe3O4+8H+=Fe2++2Fe3++4H2O
请回答下列问题:
(1)硬质试管中发生反应的化学方程式为
3Fe+4H2O(g)
Fe3O4+4H2
| ||
3Fe+4H2O(g)
Fe3O4+4H2
.
| ||
(2)该同学欲确定反应一段时间后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的成分是(只有一个选项符合题意)
A
A
,若溶液未变红色则说明硬质试管中固体物质的成分是(只有一个选项符合题意)C
C
.A.一定有Fe3O4,可能有Fe B.只有Fe(OH)3C.一定有Fe3O4和Fe
D.一定有Fe(OH)3,可能有FeE.只有Fe3O4
(3)该同学按上述实验方案进行了实验,结果溶液未变红色,原因是
Fe+2Fe3+=3Fe2+
Fe+2Fe3+=3Fe2+
(用离子方程式表示).(4)该同学马上另取少量溶液B,使其跟NaOH溶液反应.若按图2所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述现象相关的反应的化学方程式
FeSO4+2NaOH=Fe(OH)2↓+Na2SO4、4Fe(OH)2+O2+2H2O=4Fe(OH)3
FeSO4+2NaOH=Fe(OH)2↓+Na2SO4、4Fe(OH)2+O2+2H2O=4Fe(OH)3
.(5)一段时间后,该同学发现(3)中未变红的溶液变成红色,说明Fe2+具有
还原
还原
性.由此可知,实验室中含Fe2+的盐溶液需现用现配制的原因是Fe2+易被空气中的氧气氧化而变质
Fe2+易被空气中的氧气氧化而变质
,并且配制含Fe2+的盐溶液时应加入少量铁粉
铁粉
.(6)乙同学为了获得持久白色的Fe(OH)2沉淀,准备用图3所示装置,用不含O2的蒸馏水配制的NaOH溶液与新制的FeSO4溶液反应.获得不含O2的蒸馏水的方法是
把蒸馏水煮沸
把蒸馏水煮沸
.反应开始时,打开止水夹的目的是利用铁粉和稀硫酸反应产生的氢气排出试管A、B中的空气,防止Fe(OH)2被空气中氧气氧化
利用铁粉和稀硫酸反应产生的氢气排出试管A、B中的空气,防止Fe(OH)2被空气中氧气氧化
;一段时间后,关闭止水夹,在试管
B
B
(填“A”或“B”)中观察到白色的Fe(OH)2.