网址:http://m.1010jiajiao.com/timu_id_179169[举报]
一、二(63分)
题序
1
2
3
4
5
6
7
8
9
答案
D
B
B
C
B
D
A
C
D
题序
10
11
12
13
14
15
16
17
18
答案
C
D
AD
B
CD
B
A
AC
BD
三、(本题包括2小题,共27分)
19、(11分)(1)搅拌、加热(2分)(2)坩埚钳(1分),用玻璃棒不断搅拌滤液(1分)(3)NaCl(2分)
 (4)稀释溶液,防止降温过程中NaCl析出,提高产品纯度(3分)(5)重结晶(2分)。
(4)稀释溶液,防止降温过程中NaCl析出,提高产品纯度(3分)(5)重结晶(2分)。
20(16分)(1)引流作用(1分) (2) 2H2O2 == 2H2O + O2↑(3分) (3) 炭(或碳、或C) (2分)
(4)(一)[判断猜想]:猜想I不成立 (1分)
(二)[验证(操作)过程]:取少量滤液逐滴滴入稀氨水 (3分)
[实验现象]:先有白色沉淀、滴入过量稀氨水后白色沉淀溶解(3分);
[判断猜想]:结论:主要为氯化锌,其中含少量的氯化铵(3分)。
[若说成氯化铵和氯化锌的混合物给1分;若说成只有氯化锌没有氯化铵0分]
四、(本题包括3小题,共40分)
(3)B、C; (3分,若只选一个对的得1分,全对得3分)
(4)设3min―4min达到平衡时CO、H2 O的平衡浓度为c3, 则CO2 、H2的平衡浓度分别为0.200-c3和0.300- c3
根据: K= (2分)
(2分)
c3=0.120 mol/L (2分,写0.12的不给分) ;
22(12分)(1)Fe(OH)3(2分) (2)氨水 (2分) 不会引入新的杂质(1分)
(3)2Fe3++3Mg(OH)2 == 3 Mg2+ +2Fe(OH)3 (3分)
(4)A C D E (4分)(选对1个给1分,选错1个倒扣1分,但不出现负分。)
23(15分)(1)113~
(5)H2S(g) = H2(g) + S(s) △H = +112.2KJ/mol (3分) (6) 硒 (2分) 氧气 (2分)
五、(本题包括1小题,共10分)
24.(10分)(1)小(1分)(2)CH2=CH2 + H2O → CH3CH2OH (1分)100%(1分)
(3)D E(共2分)(4)①3(2分)
③BCD(2分,漏1个扣1分,漏2个和错选均为0分)
六、(本题包括2小题,每小题10分。考生只能选做一题。26题为“有机化学基础”内容试题,27小题为“物质结构”内容试题)
25 (10分)(1)[根据答到的要点或关键词给分]
①在此条件下,卤代烃的消去反应和取代反应同时进行(1分),有利于消去反应(1分)。
②在此条件下,有利于生成对称烯烃(1分),且卤原子半径越大(1分)越有利于生成对称烯烃(1分)。
若回答只是数据翻译,如:消去(取代)产物比例较大(小),或消去反应谁的比例大、谁的比例小,说出一点给1分,说出几点都如此最多给2分。
 |
⑵① (1分) CH3C≡CH (1分)
 |
|||
 |
|||
26.(10分)
(1) 3d84s2 (2分) ,分子晶体(1分), CO(1分)。
(2) B C (2分) (3)20 (2分) (4)Cu2++4H2O=[Cu(H2O)4]2+ (2分)
在一固定容积的密闭容器中进行着如下反应:
CO2(g) + H2(g)  CO(g) + H2O(g),其平衡常数K和温度t的关系如下:
CO(g) + H2O(g),其平衡常数K和温度t的关系如下:
| t℃ | 700 | 800 | 850 | 1000 | 1200 |
| K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
(2) 能判断该反应是否已经达到化学平衡状态的是:
A.容器中压强不变 B.混合气体中CO浓度不变
C.v(H2)正= v(H2O)逆 D.c(CO2) = c(CO)
(3)某研究小组利用反应:CO(g)+H2O(g)
 H2(g)+CO2(g) △H=-41.2kJ/mol,制备CO2与H2的混合气体。用碱液吸收一定量CO2的方法来提高混合气中H2与CO2的体积比。若以1L1.5mol/L的NaOH溶液充分吸收了22.4L(已折算为标准状况下体积)CO2,则吸收后溶液中各离子浓度从大到小的顺序是 。
H2(g)+CO2(g) △H=-41.2kJ/mol,制备CO2与H2的混合气体。用碱液吸收一定量CO2的方法来提高混合气中H2与CO2的体积比。若以1L1.5mol/L的NaOH溶液充分吸收了22.4L(已折算为标准状况下体积)CO2,则吸收后溶液中各离子浓度从大到小的顺序是 。(4)如将H2与CO2以4:1的体积比混合,在适当的条件下可制得CH4。已知:
CH4 (g) + 2O2(g)
 CO2(g)+ 2H2O(1) ΔH1=-890.3 kJ/mol
CO2(g)+ 2H2O(1) ΔH1=-890.3 kJ/mol H2(g) + 1/2O2(g)
 H2O(1) ΔH2=-285.8 kJ/mol
H2O(1) ΔH2=-285.8 kJ/mol 则CO2(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式是 。
(5)熔融盐燃料电池如下图:

该图是以熔融碳酸盐为电解质,以CH4为燃料,空气为氧化剂,稀土金属材料为电极。已知负极的电极反应是CH4 +4CO32--8e-=5CO2+2H2O。正极的电极反应是_______ 。为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此电池工作时必须有部分A物质参加循环,则A物质的化学式是_________。实验过程中,若通入了标准状况下空气448L(假设空气中O2体积分数为20%),则熔融盐燃料电池消耗标准状况下CH4____________L。 查看习题详情和答案>>
CO2(g) + H2(g)
 CO(g) + H2O(g),其平衡常数K和温度t的关系如下:
CO(g) + H2O(g),其平衡常数K和温度t的关系如下:| t℃ | 700 | 800 | 850 | 1000 | 1200 |
| K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
(2) 能判断该反应是否已经达到化学平衡状态的是:
A.容器中压强不变 B.混合气体中CO浓度不变
C.v(H2)正= v(H2O)逆 D.c(CO2) = c(CO)
(3)某研究小组利用反应:CO(g)+H2O(g)
 H2(g)+CO2(g) △H=-41.2kJ/mol,制备CO2与H2的混合气体。用碱液吸收一定量CO2的方法来提高混合气中H2与CO2的体积比。若以1L1.5mol/L的NaOH溶液充分吸收了22.4L(已折算为标准状况下体积)CO2,则吸收后溶液中各离子浓度从大到小的顺序是 。
H2(g)+CO2(g) △H=-41.2kJ/mol,制备CO2与H2的混合气体。用碱液吸收一定量CO2的方法来提高混合气中H2与CO2的体积比。若以1L1.5mol/L的NaOH溶液充分吸收了22.4L(已折算为标准状况下体积)CO2,则吸收后溶液中各离子浓度从大到小的顺序是 。(4)如将H2与CO2以4:1的体积比混合,在适当的条件下可制得CH4。已知:
CH4 (g) + 2O2(g)
 CO2(g)+ 2H2O(1) ΔH1=-890.3 kJ/mol
CO2(g)+ 2H2O(1) ΔH1=-890.3 kJ/mol H2(g) + 1/2O2(g)
 H2O(1) ΔH2=-285.8 kJ/mol
H2O(1) ΔH2=-285.8 kJ/mol 则CO2(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式是 。
(5)熔融盐燃料电池如下图:

该图是以熔融碳酸盐为电解质,以CH4为燃料,空气为氧化剂,稀土金属材料为电极。已知负极的电极反应是CH4 +4CO32--8e-=5CO2+2H2O。正极的电极反应是_______ 。为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此电池工作时必须有部分A物质参加循环,则A物质的化学式是_________。实验过程中,若通入了标准状况下空气448L(假设空气中O2体积分数为20%),则熔融盐燃料电池消耗标准状况下CH4____________L。
在一固定容积的密闭容器中进行着如下反应: CO2(g) + H2(g) CO(g)+ H2O(g) ;其平衡常数K和温度t的关系如下:
| t℃ | 700 | 800 | 850 | 1000 | 1200 |
| K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
(1) K的表达式为: ;
(2) 该反应的正反应为 反应(“吸热”或“放热”);
(3) 能判断该反应是否已经达到化学平衡状态的是:
A.容器中压强不变 B.混合气体中CO浓度不变
C.v(H2)正 = v(H2O)逆 D.c(CO2)= c(CO)
(4) 在850℃时,可逆反应:CO2(g)+ H2(g) CO(g)+ H2O(g),在该容器内各物质的浓度变化如下:
| 时间/min | CO2 (mol/L) | H2 (mol/L) | CO (mol/L) | H2 O ( mol/L) |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
计算:3min—4min达到平衡时CO的平衡浓度c3和CO2 (g)的转化率,要求写出简单的计算过程(c3精确到小数点后面三位数)。
查看习题详情和答案>>
在一固定容积的密闭容器中进行着如下反应: CO2(g) + H2(g) 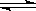 CO(g) + H2O(g) ;其平衡常数K和温度t的关系如下:
CO(g) + H2O(g) ;其平衡常数K和温度t的关系如下:
| t℃ | 700 | 800 | 850 | 1000 | 1200 |
| K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
(2) 该反应的正反应为 反应(“吸热”或“放热”);
(3) 能判断该反应是否已经达到化学平衡状态的是:
A.容器中压强不变 B.混合气体中CO浓度不变
C.v(H2)正 = v(H2O)逆 D.c(CO2) = c(CO)
(4) 在850℃时,可逆反应:CO2(g) + H2(g)
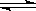 CO(g) + H2O(g),在该容器内各物质的浓度变化如下:
CO(g) + H2O(g),在该容器内各物质的浓度变化如下:| 时间/min | CO2 (mol/L) | H2 (mol/L) | CO (mol/L) | H2O ( mol/L) |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
在一固定容积的密闭容器中进行着如下反应:
CO2(g) + H2(g) 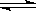 CO(g) + H2O(g) 其平衡常数K和温度t的关系如下:
CO(g) + H2O(g) 其平衡常数K和温度t的关系如下:
| t℃ | 700 | 800 | 850 | 1000 | 1200 |
| K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
(2) 该反应的正反应为 反应(“吸热”或“放热”);
(3)下列选项中可作为该反应在850℃时已经达到化学平衡状态的标志的是:
A.容器中压强不再变化 B.混合气体中CO浓度不再变化
C.混合气体的密度不再变化 D.c(CO2) =" c(CO)=" c(H2) = c(H2O)
(4)当温度为850℃,某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
| CO | H2O | CO2 | H2 |
| 0.5 mol | 8.5 mol | 2.0 mol | 2.0 mol |
 此时上述的反应中正、逆反应速率的关系式是 (填代号)。
此时上述的反应中正、逆反应速率的关系式是 (填代号)。a.v(正)>v(逆) b.v(正)<v(逆) c.v(正)=v(逆) d.无法判断 查看习题详情和答案>>



