网址:http://m.1010jiajiao.com/timu_id_174519[举报]
【小题1】 醋酸是一种常见的弱酸,为了证明醋酸是弱电解质,某校研究性学习小组开展了题为“醋酸是弱电解质的实验研究”的探究活动。该校研究性学习小组设计了如下方案:
| A.先配制一定量的0.10 mol/L CH3COOH溶液,然后测溶液的pH,若pH大于1,则可证明醋酸为弱电解质 |
| B.先测0.10 mol/L CH3COOH溶液的pH,然后将其加热至40℃,再测pH,如果pH变小,则可证明醋酸为弱电解质 |
| C.先配制一定量0.01 mol/L和0.10 mol/L的CH3COOH溶液,分别测它们的pH,若两者的pH相差小于1个单位,则可证明醋酸为弱电解质 |
| D.在常温下,配制一定量的CH3COONa溶液,测其pH,若pH大于7,则可证明醋酸为弱电解质。 |
【小题2】 一定温度下,有a、盐酸;b、硫酸;c、醋酸三种酸的稀溶液。(用a、b、c、<、=、>号填写)
①当其物质的量浓度相同时,c(H+)由大到小的顺序是_____ ____,②同体积同物质的量浓度的三种酸,中和同物质的量浓度的NaOH消耗的体积由大到小的顺序是_________ ③当c(H+)相同、体积相同时,分别加入足量锌,相同状况产生的气体体积由大到小的顺序___________ ④将c(H+)相同的三种酸均稀释10倍,pH由大到小的顺序为_____________
【小题3】某温度(t ℃)时, KW=10-13,将此温度下pH=1的硫酸溶液aL与pH=12的氢氧化钡溶液bL混合。
①若所得混合液为中性,则a:b= 。
②若所得混合液的pH=2,则a:b= 。 查看习题详情和答案>>
某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验。请填写下列空白:
【实验一】用如图所示装置,排水法收集一试管甲烷和氯气的混合气体,光照后观察到量筒内形成一段水柱,认为有氯化氢生成。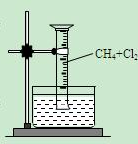
【小题1】该反应的化学方程式为 ;(只写第二步)
【小题2】水槽中盛放的液体最好为 ;(填标号)
| A.水 | B.饱和石灰水 | C.饱和食盐水 | D.饱和NaHCO3溶液 |
滴加AgNO3溶液,看到有白色沉淀生成,认为有氯化氢生成。
【小题3】该实验设计的错误之处 ;
【实验三】
步骤一:收集半试管氯气,加入10 mL 蒸馏水,充分振荡,采用DIS系统的pH传感器测溶
液的pH(下同)。测得pH = 3.26。
步骤二:收集一试管甲烷和氯气的混合气体(各占50%),在40 W的日光灯下光照6 min后,
加入10 mL 蒸馏水,充分振荡,测得pH = 1.00。
【小题4】判断该反应中有氯化氢生成的依据是 ;
【小题5】假设氯气完全参与反应,且不考虑氯气溶解于水。往反应后的溶液中加水稀释到100.00
mL,取20.00 mL稀释液,加入10.00 mL浓度为0.01 mol·L-1的AgNO3溶液恰好完全反应,则试管中原有氯气在标准状况下的体积为 mL 查看习题详情和答案>>
(12分)恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应 :N2 (g) + 3 H2(g)  2NH3(g)
2NH3(g)
【小题1】若反应某时刻t时,n t (N2) =" 13" mol,n t (NH3) =" 6" mol,则a =__________mol;
【小题2】反应达平衡时,混合气体的体积为716.8 L(标况下),其中NH3的含量(体积分数)为25%,平衡时NH3的物质的量__________;[
【小题3】原混合气体与平衡混合气体的总物质的量之比(写出最简整数比、下同),n(始)∶n(平) =________;
【小题4】原混合气体中,a∶b =__________;
【小题5】达到平衡时,N2和H2的转化率之比,α(N2)∶α(H2)= __________;
【小题6】平衡混合气体中,n(N2)∶n(H2)∶n(NH3) =__________________。
(13分)元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了①~⑨九种元素在周期表中的位置。
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | | | | ⑤ | | ⑥ | | |
| 3 | ① | ③ | ④ | | | | ⑦ | ⑨ |
| 4 | ② | | | | | | ⑧ | |
【小题1】这九种元素分别是① (填元素符号,下同)、② 、④ 、⑤ 、⑥ 、⑧ 、其中化学性质最不活泼的是 。
【小题2】在①、②、③三种元素的氧化物对应的水化物中,碱性最强的是 (填化学式)。
【小题3】⑥元素的氢化物是 (填化学式),该氢化物在常温下与②发生反应的化学方程式为 。
【小题4】⑧元素与①元素形成的化合物是 (填化学式),高温下灼烧该化合物时,火焰呈 色。 查看习题详情和答案>>
(本题共15分)空气中CO2浓度的持续走高引起人们的高度重视。一些科学家认为,人类不仅要努力减少CO2的排放,还要尽快想办法清除空气中过多的CO2。为此,他们设想了一系列“捕捉”和“封存” CO2的方法。
【小题1】方法Ⅰ:一些科学家利用太阳能加热的反应器“捕捉”空气中的CO2,如下图所示。
(1)步骤一中的CaO俗称 。
(2)步骤二中发生反应的化学方程式是 ,该反应 (填“是”或“不是”)步骤一中反应的逆反应。
【小题2】方法Ⅱ:另一些科学家利用NaOH溶液的喷淋“捕捉”空气中的CO2,如右图所示。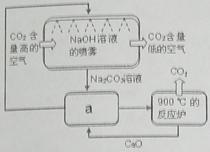
(1)NaOH溶液喷成雾状是为了 。
(2)右图a环节中,物质分离的基本操作是 。
(3)为了尽量减少成本,在整个流程中,循环利用的物质有CaO和 。
【小题3】下列溶液中,同样能用于“捕捉”二氧化碳的是( )。
| A.KNO3溶液 | B.CaCl2溶液 | C.CuSO4溶液 | D.Na2CO3溶液 |
①方法Ⅰ将受到地域的限制
②方法Ⅱ的能耗太大
③方法Ⅰ中使用的是氧化钙颗粒而不是氧化钙粉末
④方法Ⅱ中的物质可以循环利用,但方法Ⅰ中的却不能
| A.①③ | B.①② | C.②④ | D.③④ |
可见,要真正实现“碳捕捉”和“碳封存”的设想,科学家任重而道远。 查看习题详情和答案>>