摘要:(2) 817.6 .(3) 产物不会造成环境污染 .
网址:http://m.1010jiajiao.com/timu_id_174316[举报]
(1)常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol?L-1.若忽略水的电离及H2CO3的第二级电离.则H2CO3?HCO3-+H+的平衡常数K1=
(2)已知常温下Ksp(BaCO3)=5.1×10-9,Ksp(BaSO4)=1.1×10-10.
①把BaCO3和BaSO4的混合物投入水中,搅拌,制成悬浊液,再静止.上层清液中c(CO32-)与c(SO42-)之比是
②在BaSO4的悬浊液加入Na2CO3溶液,可使BaSO4转化为BaCO3.要生成BaCO3,Na2CO3溶液的浓度应大于
≈1)
查看习题详情和答案>>
4.2×10-7
4.2×10-7
.(已知10-5.60=2.5×10-6)(2)已知常温下Ksp(BaCO3)=5.1×10-9,Ksp(BaSO4)=1.1×10-10.
①把BaCO3和BaSO4的混合物投入水中,搅拌,制成悬浊液,再静止.上层清液中c(CO32-)与c(SO42-)之比是
46:1
46:1
.②在BaSO4的悬浊液加入Na2CO3溶液,可使BaSO4转化为BaCO3.要生成BaCO3,Na2CO3溶液的浓度应大于
5.1×10-4
5.1×10-4
mol/L.(设定:| 1.1 |
(2011?静安区模拟)某化工厂联合生产纯碱、镁、阻燃剂.以白云石(CaCO3?MgCO3)为原料冶炼镁:经高温煅烧生成的氧化物在还原炉中经1200℃用硅铁还原生成镁蒸汽(铁化合价不变),镁蒸汽经冷凝为粗镁;同时以海水为原料制碱和制阻燃剂.具体流程如下:
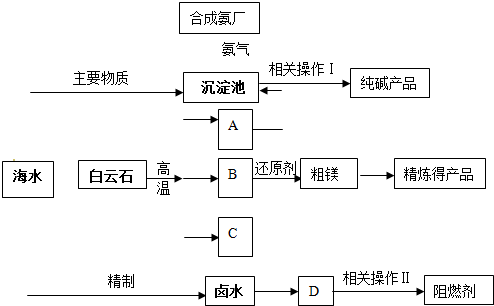
(1)分别写出A、B、C的化学式
(2)硅铁还原生成镁蒸汽时选择低压和1200℃,试分析选择这种反应条件的原因
(3)精制卤水中的MgCl2与适量石灰乳反应生成碱式氯化镁[Mg(OH)Cl]沉淀,此时溶液中主要溶质是(写化学式)
(4)描述流程中相关操作Ⅰ包括过滤、
(5)已知:Mg(OH)2(s)→MgO(s)+H2O(g)-81.5kJ;
Al(OH)3(s)→0.5Al2O3(s)+1.5H2O(g)-87.7kJ
①Mg(OH)2能起阻燃作用,其原因是
②等质量Mg(OH)2和Al(OH)3相比,阻燃效果较好的是
(6)某化工厂利用上图所示流程联合生产纯碱、镁、阻燃剂,试分析该生产的优点
查看习题详情和答案>>

(1)分别写出A、B、C的化学式
CO2
CO2
、MgO
MgO
、CaO
CaO
;沉淀池中反应的化学方程式是CO2+NH3+NaCl+H2O→NaHCO3↓+NH4Cl
CO2+NH3+NaCl+H2O→NaHCO3↓+NH4Cl
.(2)硅铁还原生成镁蒸汽时选择低压和1200℃,试分析选择这种反应条件的原因
低压有利于镁蒸气的生成及分离;1200℃只有镁为气体,从速率和平衡2个角度都有利于镁的生成
低压有利于镁蒸气的生成及分离;1200℃只有镁为气体,从速率和平衡2个角度都有利于镁的生成
.(3)精制卤水中的MgCl2与适量石灰乳反应生成碱式氯化镁[Mg(OH)Cl]沉淀,此时溶液中主要溶质是(写化学式)
CaCl2
CaCl2
.(4)描述流程中相关操作Ⅰ包括过滤、
洗涤
洗涤
、煅烧(或加热)
煅烧(或加热)
.(5)已知:Mg(OH)2(s)→MgO(s)+H2O(g)-81.5kJ;
Al(OH)3(s)→0.5Al2O3(s)+1.5H2O(g)-87.7kJ
①Mg(OH)2能起阻燃作用,其原因是
Mg(OH)2受热分解时吸收大量的热使环境温度下降;同时生成的耐高温、稳定性好的MgO、覆盖在可燃物表面,产生阻燃作用
Mg(OH)2受热分解时吸收大量的热使环境温度下降;同时生成的耐高温、稳定性好的MgO、覆盖在可燃物表面,产生阻燃作用
.②等质量Mg(OH)2和Al(OH)3相比,阻燃效果较好的是
Mg(OH)2
Mg(OH)2
.(6)某化工厂利用上图所示流程联合生产纯碱、镁、阻燃剂,试分析该生产的优点
原料易得价廉、原料利用率高、中间产物能有效地循环利用、产品结构的多样化
原料易得价廉、原料利用率高、中间产物能有效地循环利用、产品结构的多样化
.(2009?江门一模)氯化亚铜是一种重要的化工产品,常用作有机合成催化剂,还可用于颜料,防腐等工业.该物质是微溶于水的白色固体,露置于空气中易被氧化为绿色的碱式氯化铜(Cu2(0H)3Cl),在热水中易水解生成氧化铜水合物而呈红色.以下是一种采用亚硫酸盐还原法,从含铜电镀废水中制备氯化亚铜的工艺流程如图1.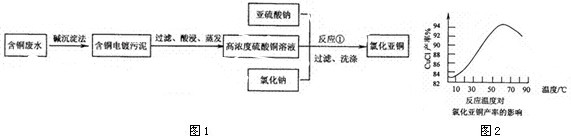
已知Ksp:CuCl:1.2×10-4 CuOH:1.4×10-15 Cu (OH) 2:1.6×10-10
请回答以下问题:
(1)写出反应①制备氯化亚铜的离子反应方程式:
(2)为提高CuCl的产率,常在反应①的体系中加入稀碱溶液,调节pH至3.5.这样做的目的是
(3)图2是各反应物在最佳配比条件下,反应温度对CuCl产率影响.由图2可知,溶液温度控制在
(4)若要提高Cucl的产率你认为还可采取的措施有
(5)写出氯化亚铜在空气中被氧化的化学方程式
(6)反应①也可用铁代替亚硫酸钠,写出该反应的化学方程式
查看习题详情和答案>>

已知Ksp:CuCl:1.2×10-4 CuOH:1.4×10-15 Cu (OH) 2:1.6×10-10
请回答以下问题:
(1)写出反应①制备氯化亚铜的离子反应方程式:
2Cu2++SO32-+2Cl-+H2O=2CuCl↓+SO42-+2H+
2Cu2++SO32-+2Cl-+H2O=2CuCl↓+SO42-+2H+
.(2)为提高CuCl的产率,常在反应①的体系中加入稀碱溶液,调节pH至3.5.这样做的目的是
OH-中和了反应中的H+,有利于平衡向右进行,提高CuCl的产率.但当OH-浓度过大时,Cu+能与OH-结合,生成氢氧化亚铜,从而降减了CuCl的产率
OH-中和了反应中的H+,有利于平衡向右进行,提高CuCl的产率.但当OH-浓度过大时,Cu+能与OH-结合,生成氢氧化亚铜,从而降减了CuCl的产率
.(3)图2是各反应物在最佳配比条件下,反应温度对CuCl产率影响.由图2可知,溶液温度控制在
60℃
60℃
时,CuCl产率能达到94%,随后随温度升高CuCl产率会下降,其原因是温度过高,一是促进了CuCl的水解,二是促进了CuCl与空气中氧气发生反应
温度过高,一是促进了CuCl的水解,二是促进了CuCl与空气中氧气发生反应
.(4)若要提高Cucl的产率你认为还可采取的措施有
反应①在隔绝空气条件下进行
反应①在隔绝空气条件下进行
.(5)写出氯化亚铜在空气中被氧化的化学方程式
4CuCl+O2+4H2O=2Cu2(OH)3Cl+2HCl
4CuCl+O2+4H2O=2Cu2(OH)3Cl+2HCl
.(6)反应①也可用铁代替亚硫酸钠,写出该反应的化学方程式
2CuSO4+2NaCl+Fe=2CuCl+FeSO4+Na2SO4
2CuSO4+2NaCl+Fe=2CuCl+FeSO4+Na2SO4
.(2011?山东)实验室以含有Ca2+、Mg2+、Cl-、SO42-、Br-等离子的卤水为主要原料制备无水CaCl2和Br2,流程如下:

(1)操作Ⅰ使用的试剂是
(2)加入溶液W的目的是
(3)实验室用贝壳与稀盐酸反应制备并收集气体,下列装置中合理的是

(4)常温下,H2SO3的电离常数Ka1=1.2×10-2,Ka2=6.3×10-8;H2CO3的电离常数Ka1=4.5×10-7,Ka2=4.7×10-11.某同学设计实验验证H2SO3酸性强于H2CO3:将SO2和CO2气体分别通入水中至饱和,立即用酸度计测量溶液的pH,若前者的pH小于后者,则H2SO3酸性强于H2CO3.该实验设计不正确,错误在于
设计合理实验验证H2SO3酸性强于H2CO3(简要说明实验步骤、现象和结论).
仪器自选.
供选择的试剂:CO2、SO2、Na2CO3、NaHCO3、Na2SO3、NaHSO3、蒸馏水、饱和石灰水、酸性KMnO4溶液、品红溶液、pH试纸.
查看习题详情和答案>>

(1)操作Ⅰ使用的试剂是
四氯化碳
四氯化碳
,所用的主要仪器名称是分液漏斗
分液漏斗
.(2)加入溶液W的目的是
除去溶液中SO42-
除去溶液中SO42-
.用CaO调节溶液Y的pH,可以除去Mg2+.由表中数据可知,理论上可选择的pH最大范围是11.0≤pH≤12.2
11.0≤pH≤12.2
.酸化溶液Z时,使用的试剂为盐酸
盐酸
.| 开始沉淀时的pH | 沉淀完全时的pH | |
| Mg2+ | 9.6 | 11.0 |
| Ca2+ | 12.2 | c(OH-)=1.8mol?L-1 |
b、d
b、d
.
(4)常温下,H2SO3的电离常数Ka1=1.2×10-2,Ka2=6.3×10-8;H2CO3的电离常数Ka1=4.5×10-7,Ka2=4.7×10-11.某同学设计实验验证H2SO3酸性强于H2CO3:将SO2和CO2气体分别通入水中至饱和,立即用酸度计测量溶液的pH,若前者的pH小于后者,则H2SO3酸性强于H2CO3.该实验设计不正确,错误在于
用于比较pH的两种酸的物质的量浓度不相等
用于比较pH的两种酸的物质的量浓度不相等
.设计合理实验验证H2SO3酸性强于H2CO3(简要说明实验步骤、现象和结论).
三种参考方案如下:
方案一:配制相同物质的量浓度的NaHSO3和NaHCO3溶液.用酸度计(或pH试纸)测两溶液的pH.前者的pH小于后者,证明H2SO3酸性强于H2CO3.
方案二:将SO2气体依次通过NaHCO3(或Na2CO3)溶液、酸性KMnO4溶液、品红溶液、澄清石灰水.品红溶液不褪色,且澄清石灰水变浑浊,证明H2SO3酸性强于H2CO3.
方案三:将CO2气体依次通过NaHSO3(或Na2SO3)溶液、品红溶液.品红溶液不褪色,证明H2SO3酸性强于H2CO3
方案一:配制相同物质的量浓度的NaHSO3和NaHCO3溶液.用酸度计(或pH试纸)测两溶液的pH.前者的pH小于后者,证明H2SO3酸性强于H2CO3.
方案二:将SO2气体依次通过NaHCO3(或Na2CO3)溶液、酸性KMnO4溶液、品红溶液、澄清石灰水.品红溶液不褪色,且澄清石灰水变浑浊,证明H2SO3酸性强于H2CO3.
方案三:将CO2气体依次通过NaHSO3(或Na2SO3)溶液、品红溶液.品红溶液不褪色,证明H2SO3酸性强于H2CO3
三种参考方案如下:
方案一:配制相同物质的量浓度的NaHSO3和NaHCO3溶液.用酸度计(或pH试纸)测两溶液的pH.前者的pH小于后者,证明H2SO3酸性强于H2CO3.
方案二:将SO2气体依次通过NaHCO3(或Na2CO3)溶液、酸性KMnO4溶液、品红溶液、澄清石灰水.品红溶液不褪色,且澄清石灰水变浑浊,证明H2SO3酸性强于H2CO3.
方案三:将CO2气体依次通过NaHSO3(或Na2SO3)溶液、品红溶液.品红溶液不褪色,证明H2SO3酸性强于H2CO3
.方案一:配制相同物质的量浓度的NaHSO3和NaHCO3溶液.用酸度计(或pH试纸)测两溶液的pH.前者的pH小于后者,证明H2SO3酸性强于H2CO3.
方案二:将SO2气体依次通过NaHCO3(或Na2CO3)溶液、酸性KMnO4溶液、品红溶液、澄清石灰水.品红溶液不褪色,且澄清石灰水变浑浊,证明H2SO3酸性强于H2CO3.
方案三:将CO2气体依次通过NaHSO3(或Na2SO3)溶液、品红溶液.品红溶液不褪色,证明H2SO3酸性强于H2CO3
仪器自选.
供选择的试剂:CO2、SO2、Na2CO3、NaHCO3、Na2SO3、NaHSO3、蒸馏水、饱和石灰水、酸性KMnO4溶液、品红溶液、pH试纸.
粗CuO是将工业废铜、废铜合金等高温焙烧而成的,杂质主要是铁的氧化物及泥沙.
以粗CuO为原料制备胆矾的主要流程如下: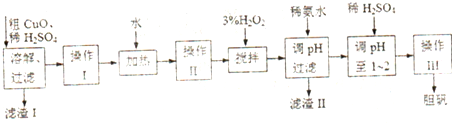
已知Fe3+,Fe2+,Cu2+转化为相应氢氧化物时,开始沉淀的沉淀完全时的pH如下表:
(1)为使粗CuO充分溶解,可采取的措施除适当延长溶解时间、充分搅拌、将粗CuO粉碎外,还有 (答一条即可)
(2)加入3% H2O2之前必须进行操作Ⅱ,操作Ⅱ的目的是 .H2O2参加反应的离子方程式为 .
(3)加入稀氨水后,溶液的pH应在 范围内.
(4)经操作Ⅰ得到粗胆矾,操作Ⅲ得到精制胆矾.两步操作相同,都包括燕发浓缩、冷却结晶、吸滤、洗涤、干燥等步骤示和普通过滤相比,吸滤的优点是 .(至少答两条).
(5)吸滤操作中,除烧杯、玻璃棒、安全瓶外,还必须使用的属于硅酸盐材料的仪器有 .
查看习题详情和答案>>
以粗CuO为原料制备胆矾的主要流程如下:

已知Fe3+,Fe2+,Cu2+转化为相应氢氧化物时,开始沉淀的沉淀完全时的pH如下表:
| Fe3+ | Fe2+ | Cu2+ | |
| 开始沉淀的pH | 2.7 | 7.6 | 5.2 |
| 沉淀完全的pH | 3.7 | 9.6 | 6.4 |
(2)加入3% H2O2之前必须进行操作Ⅱ,操作Ⅱ的目的是
(3)加入稀氨水后,溶液的pH应在
(4)经操作Ⅰ得到粗胆矾,操作Ⅲ得到精制胆矾.两步操作相同,都包括燕发浓缩、冷却结晶、吸滤、洗涤、干燥等步骤示和普通过滤相比,吸滤的优点是
(5)吸滤操作中,除烧杯、玻璃棒、安全瓶外,还必须使用的属于硅酸盐材料的仪器有