网址:http://m.1010jiajiao.com/timu_id_169064[举报]
说明:1. 文字简答题以关键词到位为准,按点给分;
2. 化学用语书写:(1)方程式未配平不得分、无条件扣一半分值;
(2)化学式书写错误得0分;
3. 写名称或化学式正确的正常给分; 4. 其他合理解法正常给分。
第Ⅰ卷(选择题,共48分)
一、选择题(本题包括8小题,每小题3分,共24分。每小题只有一个选项符合题意。)
二、选择题(本题包括6小题,每小题4分,共24分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给满分,但只要选错一个该小题就为0分。)
题号
1
2
3
4
5
6
7
8
9
10
11
12
13
14
答案
A
C
D
B
D
D
A
C
A
AD
A
C
BD
D
第Ⅱ卷(非选择题 共72分)
三、(本题包括2小题,共18分)
15.(12分)(1)过滤(2分) 蒸发、结晶(2分) (2)从漏斗向量气筒内注入一定量的水,连接好装置,移动漏斗形成液面高度差,静置后,液面高度不再变化,即表明气密性良好。(其他合理方法均给分)(2分)
(3)移动漏斗保持液面与量气筒液面相平,防止试管和量气筒内气体压强过大 (4分,各2分)
(4) %(2分)
%(2分)
16.(6分,各2分)(2)向上述刚好褪色的溶液中再滴入一些NaOH溶液,若红色复出,则是因为HCl和HClO的酸性所致,甲正确;若红色不再复出,则是因为HClO的强氧化性所致,乙正确。
(3)在试管中注入滴有酚酞的氨水,加热试管,观察溶液颜色变化,如果颜色变浅,则加热使氨水中的c(OH一)减小,乙正确;如颜色变深,则加热使氨水中的c(OH一)增大,甲正确。
(4)向Mg(OH)2沉淀中加入中性的醋酸铵浓溶液,加入后若Mg(OH)2不溶解,甲正确;加入后若Mg(OH)2溶解,则乙正确。
四、(本题包括2小题,共22分)
17.(12分,每空2分)(1)
(2)减小 , OH―中和了反应中的H+,有利于平衡向右进行,提高CuCl的产率。但当OH―浓度过大时,Cu+能与OH-结合,生成氢氧化亚铜,从而降减了CuCl的产率。
注此答案同题目不一致
(3)
(4)反应①在隔绝空气条件下进行。
18.(10分,每空2分)
(1)6(NH2)2CO → C3H6N6 + 6NH3 + 3CO2、4NO2 + O2+2H2O = 4HNO3、 CO2+4H2→CH4 +2H2O
(2)66.7% (3)做耐磨材料等。
五、(本题包括1小题,共12分)
19.(12分)
(1)Fe-6e-+8OH-ㄔFeO42-+4H2O(2分)
(2)铁丝网的接触面积更大。(2分)因为铁电极上发生析氧反应4OH--4e-ㄔO2↑+2H2O,氧气将铁氧化而得到氧化铁膜。(也可以直接写电极反应式或综合式:6OH--6e-+2FeㄔFe2O3+3H2O)(2分)
(3)ACD(2分,对1―2个给1分,全对得2分,错1个扣1分)
(4)升温电解一方面加快了高铁酸盐的生成速率,另一方面又加速FeO42-的分解,10~
(5)BCD(2分,对1―2个给1分,全对得2分,错1个扣1分)
六、(本题包括1小题,共10分)
20.(10分)(1)BD (2分,对1个得1分,多选1个扣1分,扣完为止) (2)小于,减小 (2分)
(3)不,1.0(4分,各2分) (4)56(2分)
七、(本题包括1小题,共10分)
21.(10分)(1)2Cl―+2H2O=2OH―+Cl2↑+H2↑(2分)
(2)A(2分)
(3)n(H2)= n(已电解NaCl)=500
mol´2=1000
mol(1分)
n(已电解NaCl)=500
mol´2=1000
mol(1分)
n(总NaCl)=1000
/0.9 mol m(总NaCl)=
1000 /0.9 mol´
m(NaCl溶液)=
(4)由n(H2)=500 mol得:n(CH4)= 500 mol´2/8=125 mol(2分)
V(CH4)= 125 mol ´

(1)加入的A是
(2)反应②的离子方程式是
但当OH-浓度偏大时,Cu2+能与OH结合,生成沉淀,反而降低了Cu2Cl2的产率造成产物不纯
但当OH-浓度偏大时,Cu2+能与OH结合,生成沉淀,反而降低了Cu2Cl2的产率造成产物不纯
(3)保持各反应物的最佳配比,改变温度,测得Cu2Cl2产率的变化如图二所示.则溶液温度控制在
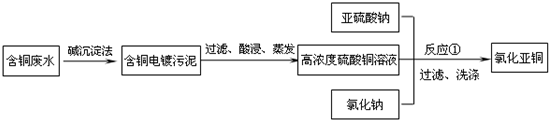
氯化亚铜是一种重要的化工产品,常用作有机合成催化剂,还可用于颜料,防腐等工业.该物质是微溶于水的白色固体,露置于空气中易被氧化为绿色的碱式氯化铜(Cu2(0H) 3CI),在热水中易水解生成氧化铜水合物而呈红色.以下是一种采用亚硫酸盐还原法,从含铜电镀废水中制备氯化亚铜的工艺流程如图1.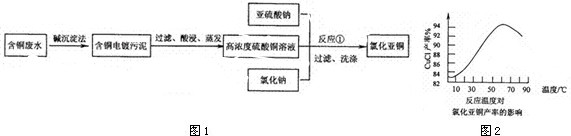
已知Ksp:Cucl:1.2×10-4 CuOH:1.4×10-15 Cu (OH) 2:1.6×10-10
请回答以下问题:
(1)写出反应①制备氯化亚铜的离子反应方程式:______.
(2)为提高CuCl的产率,常在反应①的体系中加入稀碱溶液,调节pH至3.5.这样做的目的是______.
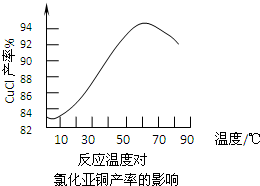
(3)图2是各反应物在最佳配比条件下,反应温度对CuCl产率影响.由图2可知,溶液温度控制在______时,CuCl产率能达到94%,随后随温度升高CuCl产率会下降,其原因是______.
(4)若要提高Cucl的产率你认为还可采取的措施有______.
(5)写出氯化亚铜在空气中被氧化的化学方程式______.
(6)反应①也可用铁代替亚硫酸钠,写出该反应的化学方程式______.
查看习题详情和答案>>
 氯化亚铜是一种重要的化工产品,常用作有机合成催化剂,还可用于颜料,防腐等工业.该物质露置于空气中易被氧化为绿色的高价铜盐,在热水中易水解生成氧化铜水合物而呈红色.以下是一种采用亚硫酸盐还原法,从含铜电镀废水中制备氯化亚铜的工艺流程图.请回答以下问题:
氯化亚铜是一种重要的化工产品,常用作有机合成催化剂,还可用于颜料,防腐等工业.该物质露置于空气中易被氧化为绿色的高价铜盐,在热水中易水解生成氧化铜水合物而呈红色.以下是一种采用亚硫酸盐还原法,从含铜电镀废水中制备氯化亚铜的工艺流程图.请回答以下问题:
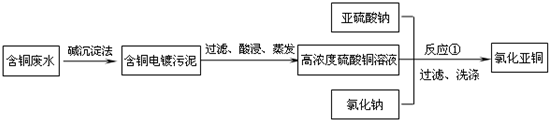
(1)写出反应①制备氯化亚铜的离子反应方程式:______.
(2)为提高CuCl的产率,常在反应①的体系中加入稀碱溶液,调节pH至3.5.这样做的目的是______.
(3)右图是各反应物在最佳配比条件下,反应温度对CuCl产率影响.由图可知,溶液温度控制在______
时,CuCl产率能达到94%.随后随温度升高CuCl产率会下降,其原因是______.
(4)若要提高CuCl的产率你认为还可采取的措施有______.
查看习题详情和答案>>
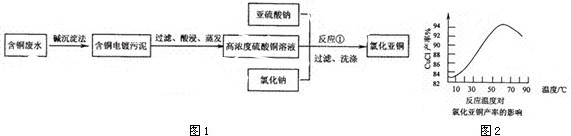
已知Ksp:CuCl:1.2×10-4 CuOH:1.4×10-15 Cu (OH) 2:1.6×10-10
请回答以下问题:
(1)写出反应①制备氯化亚铜的离子反应方程式:______.
(2)为提高CuCl的产率,常在反应①的体系中加入稀碱溶液,调节pH至3.5.这样做的目的是______.
(3)图2是各反应物在最佳配比条件下,反应温度对CuCl产率影响.由图2可知,溶液温度控制在______时,CuCl产率能达到94%,随后随温度升高CuCl产率会下降,其原因是______.
(4)若要提高Cucl的产率你认为还可采取的措施有______.
(5)写出氯化亚铜在空气中被氧化的化学方程式______.
(6)反应①也可用铁代替亚硫酸钠,写出该反应的化学方程式______.
(1)写出反应①制备氯化亚铜的离子反应方程式:______.
(2)为提高CuCl的产率,常在反应①的体系中加入稀碱溶液,调节pH至3.5.这样做的目的是______.
(3)右图是各反应物在最佳配比条件下,反应温度对CuCl产率影响.由图可知,溶液温度控制在______
时,CuCl产率能达到94%.随后随温度升高CuCl产率会下降,其原因是______.
(4)若要提高CuCl的产率你认为还可采取的措施有______.