网址:http://m.1010jiajiao.com/timu_id_169051[举报]
说明:1. 文字简答题以关键词到位为准,按点给分;
2. 化学用语书写:(1)方程式未配平不得分、无条件扣一半分值;
(2)化学式书写错误得0分;
3. 写名称或化学式正确的正常给分; 4. 其他合理解法正常给分。
第Ⅰ卷(选择题,共48分)
一、选择题(本题包括8小题,每小题3分,共24分。每小题只有一个选项符合题意。)
二、选择题(本题包括6小题,每小题4分,共24分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该小题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给满分,但只要选错一个该小题就为0分。)
题号
1
2
3
4
5
6
7
8
9
10
11
12
13
14
答案
A
C
D
B
D
D
A
C
A
AD
A
C
BD
D
第Ⅱ卷(非选择题 共72分)
三、(本题包括2小题,共18分)
15.(12分)(1)过滤(2分) 蒸发、结晶(2分) (2)从漏斗向量气筒内注入一定量的水,连接好装置,移动漏斗形成液面高度差,静置后,液面高度不再变化,即表明气密性良好。(其他合理方法均给分)(2分)
(3)移动漏斗保持液面与量气筒液面相平,防止试管和量气筒内气体压强过大 (4分,各2分)
(4) %(2分)
%(2分)
16.(6分,各2分)(2)向上述刚好褪色的溶液中再滴入一些NaOH溶液,若红色复出,则是因为HCl和HClO的酸性所致,甲正确;若红色不再复出,则是因为HClO的强氧化性所致,乙正确。
(3)在试管中注入滴有酚酞的氨水,加热试管,观察溶液颜色变化,如果颜色变浅,则加热使氨水中的c(OH一)减小,乙正确;如颜色变深,则加热使氨水中的c(OH一)增大,甲正确。
(4)向Mg(OH)2沉淀中加入中性的醋酸铵浓溶液,加入后若Mg(OH)2不溶解,甲正确;加入后若Mg(OH)2溶解,则乙正确。
四、(本题包括2小题,共22分)
17.(12分,每空2分)(1)
(2)减小 , OH―中和了反应中的H+,有利于平衡向右进行,提高CuCl的产率。但当OH―浓度过大时,Cu+能与OH-结合,生成氢氧化亚铜,从而降减了CuCl的产率。
注此答案同题目不一致
(3)
(4)反应①在隔绝空气条件下进行。
18.(10分,每空2分)
(1)6(NH2)2CO → C3H6N6 + 6NH3 + 3CO2、4NO2 + O2+2H2O = 4HNO3、 CO2+4H2→CH4 +2H2O
(2)66.7% (3)做耐磨材料等。
五、(本题包括1小题,共12分)
19.(12分)
(1)Fe-6e-+8OH-ㄔFeO42-+4H2O(2分)
(2)铁丝网的接触面积更大。(2分)因为铁电极上发生析氧反应4OH--4e-ㄔO2↑+2H2O,氧气将铁氧化而得到氧化铁膜。(也可以直接写电极反应式或综合式:6OH--6e-+2FeㄔFe2O3+3H2O)(2分)
(3)ACD(2分,对1―2个给1分,全对得2分,错1个扣1分)
(4)升温电解一方面加快了高铁酸盐的生成速率,另一方面又加速FeO42-的分解,10~
(5)BCD(2分,对1―2个给1分,全对得2分,错1个扣1分)
六、(本题包括1小题,共10分)
20.(10分)(1)BD (2分,对1个得1分,多选1个扣1分,扣完为止) (2)小于,减小 (2分)
(3)不,1.0(4分,各2分) (4)56(2分)
七、(本题包括1小题,共10分)
21.(10分)(1)2Cl―+2H2O=2OH―+Cl2↑+H2↑(2分)
(2)A(2分)
(3)n(H2)= n(已电解NaCl)=500
mol´2=1000
mol(1分)
n(已电解NaCl)=500
mol´2=1000
mol(1分)
n(总NaCl)=1000
/0.9 mol m(总NaCl)=
1000 /0.9 mol´
m(NaCl溶液)=
(4)由n(H2)=500 mol得:n(CH4)= 500 mol´2/8=125 mol(2分)
V(CH4)= 125 mol ´
一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
2CO(g)+SO2(g)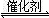 2CO2(g)+S(l)
△H
2CO2(g)+S(l)
△H
(1)已知2CO(g)+O2(g)= 2CO2(g) △H1=—566kJ•mol—1
S(l) +O2(g)= SO2(g) △H2=—296kJ•mol—1
则反应热ΔH= kJ•mol-1。
(2)其他条件相同、催化剂不同时,SO2的转化率随反应温度的变化如图a。260℃时 (填Fe2O3、NiO或Cr2O3)作催化剂反应速率最快。Fe2O3和NiO作催化剂均能使SO2的转化率达到最高,不考虑价格因素,选择Fe2O3的主要优点是 。

(3)科研小组在380℃、Fe2O3作催化剂时,研究了不同投料比[n(CO)∶n(SO2)]对 SO2转化率的影响,结果如图b。请在答题卡坐标图中画出n(CO)∶n(SO2)=2∶1 时,SO2转化率的预期变化曲线。
(4)工业上还可用Na2SO3溶液吸收烟气中的SO2:Na2SO3+SO2+H2O=2NaHSO3。某温度下用1.0mol•L-1 Na2SO3溶液吸收纯净的SO2,当溶液中c(SO32-)降至 0.2mol•L-1时,吸收能力显著下降,应更换吸收剂。
①此时溶液中c(HSO3-)约为______mol•L-1;
②此时溶液pH=______。(已知该温度下SO32—+H+ HSO3—的平衡常数K=8.0 × 106 L•mol-1,计算时SO2、H2SO3的浓度忽略不计)
HSO3—的平衡常数K=8.0 × 106 L•mol-1,计算时SO2、H2SO3的浓度忽略不计)
查看习题详情和答案>>
提出假设:
假设1:沉淀为Cu (OH)2
假设2:沉淀为
假设3:沉淀为碱式碳酸铜[化学式可表示为nCuCO3?mCu (OH)2]
查阅资料:
无论是哪一种沉淀受热均易分解(假设均不含结晶水).
定性探究:
步骤1:将所得悬浊液过滤,用蒸馏水洗涤,再用无水乙醇洗涤,风干;
步骤2:甲同学取一定量固体,用气密性良好的如下装置(夹持仪器未画出)进行定性实验;
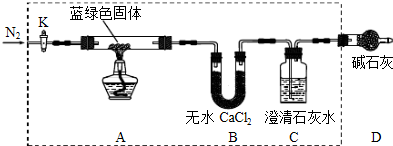
(1)若反应后A中蓝绿色固体变黑,C中无明显现象,证明假设
(2)乙同学认为只要将上图中B装置的试剂改用下列某试剂后,便可验证上述所有假设,该试剂是
a.浓硫酸 b.无水CuSO4 c.碱石灰 d.P2O5
(3)乙同学更换B试剂后验证假设3成立的实验现象是
定量探究
(4)乙同学进一步探究假设3中固体的组成:
①乙同学查得一些物质在20℃的数据(如下表)后,将C中的澄清石灰水改为Ba(OH)2溶液,其原因是
| 溶解度(S)/g | 溶度积(Ksp) | 摩尔质量(M)/g?mol-1 | |||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9×10-9 | 2.6×10-9 | 100 | 197 |
b.Ba(OH)2为强碱,Ca(OH)2为弱碱
c.吸收等量CO2生成的BaCO3的质量大于CaCO3,测量误差小
d.相同条件下,CaCO3的溶解度明显大于BaCO3
②若所取蓝绿色固体质量为54.2g,实验结束后装置B的质量增加5.4g,C中的产生沉淀的质量为39.4g.则该蓝绿色固体的化学式为
(1)常温下,0.1 mol/L的醋酸和0.1 mol/L的盐酸各100 mL,分别与足量的锌粒反应,产生的气体体积前者 后者(填“<”、“>”或“=”).
(2)在25℃条件下将pH=5的氯化铵溶液稀释100倍,稀释后溶液的pH为(填选项字母,下同) .
A.5 B.7 C.3~5之间 D.5~7之间
(3)将体积和物质的量浓度都相同的醋酸和氢氧化钠溶液混合后,溶液呈 性(填“酸”,“中”或“碱”,下同),溶液中c(Na+) c(CH3COO-)(填“ >” 或“=”或“<”,下同 )。
(4)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈 性,溶液中c(Na+) c(CH3COO-)
(5)将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后溶液的pH=7,则醋酸溶液中c(H+) 氢氧化钠溶液中c(OH-),m与n的大小关系是m n。
(6)用标准的NaOH滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏高的原因可能是 。(多选、错选不得分)
A.配制标准溶液的氢氧化钠中混有Na2CO3杂质;
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确;
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗;
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液;
E.未用标准液润洗碱式滴定管。
查看习题详情和答案>>