网址:http://m.1010jiajiao.com/timu_id_159104[举报]
1.D 2.D 3.B 4.D 5.D 6.B 7.A 8.C
9.C 10.AB 11.D 12.C 13.C 14.C
15.(1)检验反应中生成的H2 (2分)
(2)Fe Fe3O4溶于盐酸生成的Fe3+ 与Fe反应生成了Fe2+ (2分)
(3)① 2Fe2++2H++H2O2=2Fe3++2H2O (2分)
②取少量最后一次洗涤液,滴加AgNO3溶液,若无沉淀生成,表明沉淀已洗涤干净 (2分)
③固体样品质量和红褐色固体的质量 (2分)
(本题共10分,其它合理答案参照给分)
 (3)相同温度下,K2SO4 的溶解度小于KCl、(NH4)2SO4
及NH4Cl
(3)相同温度下,K2SO4 的溶解度小于KCl、(NH4)2SO4
及NH4Cl
(4)CaO、H2O 或Ca(OH)2
(5) 原子利用率高,没有有害物质排放到环境中 (每空2分,共10分)
19.(1)  (2)酸性KMnO4溶液 (3) 3
(2)酸性KMnO4溶液 (3) 3
(4) 
 |
(5)
(6) 
 (每空2分,共12分)
(每空2分,共12分)
20.(1) (C6H10O5)n+nH2O 3nCH4↑+3nCO2↑ (2分)
(2)9.20 (
(3) 设反应③中消耗O2的物质的量为x,则N2的物质的量为4x
2CH4+O2→4H2+2CO CH4 + H2O → 3H2 + CO
2x x 4x 2x 1×103-2x (1×103-2x)×3 (1×103-2x)
合成二甲醚反应中CO和H2为1∶2,合成氨反应中,N2与H2体积比为1∶3,则
4x+(1×103-2x)×3-[2x+(1×103-2x)]×2=4x×3 (3分,关系式)
x=1000/14 mol
NH3
:4x×2×17=
答略。(本题共10分,其它合理答案参照给分)
21.(1) 1s22s22p63s23p63d54s2 (2分)
Mn2+的3d轨道电子排布为半满状态较稳定 (2分)
(2) 直线型 (2分) CO2 (2分)
(3) 1:2 (1分)  (1分) 30 (2分)
(1分) 30 (2分)
本资料由《七彩教育网》www.7caiedu.cn 提供!
氢氧燃料电池能量转化率高,具有广阔的发展前景。现用氢氧燃料电池进行下图所示实验:①氢氧燃料电池中,正极的电极反应式为
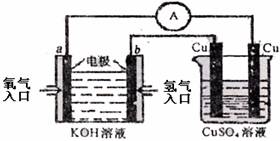
②上图装置中,某一铜电极的质量减轻3.2g,则a极上消耗的O2在标准状况下的体积为
L
查看习题详情和答案>>(1)氮化铝具有耐高温,抗冲击等优良性能,可以通过氧化铝、氮气和碳在高温下反应制得,缺点是会生成一种有毒气体,写出反应方程式:
(2)C3N4晶体的硬度可以和金刚石相媲美,且原子间均以单键结合,C3N4属于晶体,晶体中C-N键键长
(3)氮化硅是一种高温陶瓷材料,用来制作汽轮机叶子或永久性模具,现利用四氯化硅和氮气在氢气的作用下加强热,可得较高纯度的氮化硅,反应的化学方程式为:
(4)氮的另外一种化合物肼(N2H4)是一种火箭发射原料,已知0.4mol液态肼与足量液态双氧水发生反应生成N2和水蒸气,放出256.65kJ的热量.请写出该反应的热化学方程式:
Ⅱ用地壳中某主要元素生产的多种产品在现代高科技中占重要位置,足见化学对现代物质文明的重要作用.例如:
(1)目前应用最多的太阳能电池的光电转化材料是
(2)光导纤维的主要成分是:
(3)用作吸附剂、干燥剂、催化剂或催化剂载体的人造分子筛大多是一类称为
化学在能源开发与利用中起着十分关键的作用。氢气是一种新型的绿色能源,又是一种重要的化工原料。
Ⅰ.氢氧燃料电池能量转化率高,具有广阔的发展前景。现用氢氧燃料电池进行如图所示的实验(图中所用电极均为惰性电极):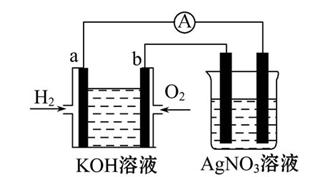
(1)对于氢氧燃料电池,下列表达不正确的是 。
| A.a电极是负极,OH-移向负极 |
| B.b电极的电极反应为:O2+2H2O+4e-=4OH- |
C.电池总反应式为:2H2+O2 2H2O 2H2O |
| D.电解质溶液的pH保持不变 |
(2)上图装置中盛有100 mL 0.1 mol·L-1 AgNO3溶液,当氢氧燃料电池中消耗氢气112 mL(标准状况下)时,此时图中装置中溶液的pH= (溶液体积变化忽略不计)。
Ⅱ.已知甲醇的燃烧热ΔH为-726.5 kJ·mol-1,在直接以甲醇为燃料的电池中,电解质溶液为酸性,负极的反应式为 ,正极的反应式为 。
理想状态下,该燃料电池消耗1 mol甲醇所能产生的最大电能为702.1 kJ,则该燃料电池的理论效率为 (燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比)。 查看习题详情和答案>>
Ⅰ.氢氧燃料电池能量转化率高,具有广阔的发展前景。现用氢氧燃料电池进行如图所示的实验(图中所用电极均为惰性电极):

(1)对于氢氧燃料电池,下列表达不正确的是 。
| A.a电极是负极,OH-移向负极 |
| B.b电极的电极反应为:O2+2H2O+4e-=4OH- |
C.电池总反应式为:2H2+O2 2H2O 2H2O |
| D.电解质溶液的pH保持不变 |
(2)上图装置中盛有100 mL 0.1 mol·L-1 AgNO3溶液,当氢氧燃料电池中消耗氢气112 mL(标准状况下)时,此时图中装置中溶液的pH= (溶液体积变化忽略不计)。
Ⅱ.已知甲醇的燃烧热ΔH为-726.5 kJ·mol-1,在直接以甲醇为燃料的电池中,电解质溶液为酸性,负极的反应式为 ,正极的反应式为 。
理想状态下,该燃料电池消耗1 mol甲醇所能产生的最大电能为702.1 kJ,则该燃料电池的理论效率为 (燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比)。
Ⅰ、氢氧燃料电池能量转化率高,具有广阔的发展前景.现用氢氧燃料电池进行如图实验(图中所用电极均为惰性电极)
(1)对于氢氧燃料电池中,下列表达不正确的是______.
A、a电极是负极,OH-移向负极
B、b电极的电极反应为:O2+2H2O+4e-→4OH-
C、电极总反应式为:2H2+O2
| ||
D、电池中电解质溶液的pH保持不变
E、氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
(2)如图装置中盛有100mL 0.1mol?L-1 AgNO3溶液,当氢氧燃料电池中消耗氢气112mL(标准状况下)时,则此时右图装置中溶液的pH=______.(溶液体积变化忽略不计)
Ⅱ、氢气是合成氨的重要原料.工业上合成氨的反应是:N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ?mol-1
(1)下列事实中,不能说明上述可逆反应已经达到平衡的是______.
①N2、H2、NH3的体积分数不再改变
②单位时间内生成2n mol NH3的同时生成3n mol H2
③单位时间内生成3n mol N-H键的同时生成n mol N≡N
④用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1:3:2
⑤混合气体的平均摩尔质量不再改变
⑥混合气体的总物质的量不再改变
(2)已知合成氨反应在某温度下2.00L的密闭容器中进行,测得如下数据:
| 时间(h) 物质的量(mol) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0.00 | 0.20 | n2 | 1.00 | 1.00 |
①反应进行到2小时时放出的热量为______kJ.
②0~1小时内N2的平均反应速率______mol?L-1?h-1
③此条件下该反应的化学平衡常数K=______(保留两位小数).
④反应达到平衡后,若往平衡体系中再加入N2、H2和NH3各1mol,化学平衡向______方向移动(填“正反应”或“逆反应”或“不移动”)
