网址:http://m.1010jiajiao.com/timu_id_144185[举报]
一、选择题(126分)
1、D 2、D 3、D 4、A 5、C
6、D 7、B 8、D 9、D 10、D
11、C 12、C 13、D
14、A 15、B 16、D 17、AC 18、B 19、CD 20、C 21、D
二、非选择题
22、I、(1)3.8 (2分) (2) 0.3(2分) (3)512.5(2分)
理科综合.files/image246.gif) Ⅱ、(1)电路图如图所示(4分)
Ⅱ、(1)电路图如图所示(4分)
(2)理科综合.files/image118.gif) (2分)
(2分) 理科综合.files/image126.gif) (2分)
(2分)
(3)1.47(1分) (1.46~1.48)
0.8(2分)(0.78~0.83)
23、(1)设A物体的质量为m,B物体的质量为M。A、B两物体下滑过程机械能守恒:
理科综合.files/image250.gif) ,
, 理科综合.files/image252.gif) (2分)
(2分)
解得:理科综合.files/image254.gif) m/s(2分)
m/s(2分)
理科综合.files/image256.gif) m/s(2分)
m/s(2分)
(2)设A、B两物体下滑的时间分别为理科综合.files/image258.gif) 、
、理科综合.files/image260.gif) 。由牛顿第二定律求得A、B两物体下滑的加速度均为:
。由牛顿第二定律求得A、B两物体下滑的加速度均为:理科综合.files/image262.gif) (2分)
(2分)
由运动学公式:理科综合.files/image264.gif)
理科综合.files/image266.gif) (2分)
(2分)
解得:理科综合.files/image268.gif) s
s 理科综合.files/image270.gif) s (2分)
s (2分)
在水平面上两物体均做匀速运动,所以当B物体追上A物体时,
有 理科综合.files/image272.gif) (2分) 解得:
(2分) 解得:理科综合.files/image274.gif) s(2分)
s(2分)
24、(1)设小铁块的加速度大小为a,对小铁块进行受力分析有理科综合.files/image276.gif) 得
得
理科综合.files/image278.gif) (3分)因为
(3分)因为理科综合.files/image280.gif) ,所以小铁块有相对滑动时的加速度沿斜面向上。(1分)
,所以小铁块有相对滑动时的加速度沿斜面向上。(1分)
(2)小铁块先沿斜面向下匀减速运动至速度为零再沿斜面向上匀加速运动,最终获得稳定速度理科综合.files/image105.gif) ,设经时间t后小铁块达到稳定速度,则
,设经时间t后小铁块达到稳定速度,则理科综合.files/image283.gif) (2分)
(2分)
理科综合.files/image285.gif) (1分)
(1分)
设此段时间内小铁块的位移为理科综合.files/image287.gif) ,木板的位移为
,木板的位移为理科综合.files/image289.gif) 有:
有:
理科综合.files/image291.gif) 方向沿斜面向下(
方向沿斜面向下(理科综合.files/image293.gif) ) (1分)
) (1分)
理科综合.files/image295.gif) 方向沿斜面向上(1分)
方向沿斜面向上(1分)
理科综合.files/image297.gif) (1分)
(1分) 理科综合.files/image299.gif) (3分)
(3分)
(3)对木板M进行受力分析,可知拉力
理科综合.files/image301.gif) (3分)
(3分)
则由理科综合.files/image303.gif) 得:
得:
理科综合.files/image305.jpg)
理科综合.files/image307.gif)
理科综合.files/image309.gif) (3分)
(3分)
25、(1)带电微粒从O点射入磁场,运动轨迹如右图。第一次
经过磁场边界上的A点。由于带电粒子做圆周运动的圆心一定
在速度的垂线上,可确定圆心的坐标为理科综合.files/image311.gif) ,又由几何关系可
,又由几何关系可
判断出A点的位置坐标为理科综合.files/image313.gif) 。
。
由理科综合.files/image315.gif) 可知:
可知:理科综合.files/image317.gif) ,所以A点坐标为
,所以A点坐标为理科综合.files/image319.gif) ……(5分)
……(5分)
(2)设带电微粒在磁场中做圆周运动的周期为T,则理科综合.files/image321.gif) ,又由几何关系得,
,又由几何关系得,
OA、AC所对应的圆心角分别为理科综合.files/image323.gif) 和
和理科综合.files/image325.gif) ,故
,故理科综合.files/image327.gif) ……(5分)
……(5分)
(3)微粒从C点沿y轴正方向进入电场,做类平抛运动。
沿y轴方向做匀速运动:理科综合.files/image329.gif) ……(2分)
……(2分)
沿x轴方向做匀加速运动:理科综合.files/image331.gif) ,
, 理科综合.files/image333.gif) (2分)
(2分)
解得:理科综合.files/image335.gif) ,
,理科综合.files/image337.gif) ……(2分)
……(2分)
离开电、磁场区域的位置坐标理科综合.files/image339.gif) (2分)
(2分)
离开电、磁场时的位置坐标是理科综合.files/image341.gif) (2分)
(2分)
理科综合.files/image343.gif) 26、(1)①
26、(1)①
理科综合.files/image345.gif)
理科综合.files/image191.gif) ;酸
;酸
②变小;
V=10时,生成物为K2C2O4
,理科综合.files/image347.gif) 发生水解反应,
发生水解反应,理科综合.files/image349.gif) ,加入NaOH溶液使水解平衡向左移动,
,加入NaOH溶液使水解平衡向左移动,理科综合.files/image347.gif) 的浓度增大,故
的浓度增大,故理科综合.files/image351.gif) 变小
变小
(2)①当滴入最后一滴KMnO4溶液时,溶液由无色变紫色且半分钟内不褪色
②理科综合.files/image353.gif)
③0.0025mol?L-1(或2.5×10-3mol?L-1)(每空2分)
27、(1)理科综合.files/image355.gif) ;
; 理科综合.files/image357.gif) (3分)
(3分)
(2)理科综合.files/image359.gif) (2分)
(2分)
(3)①理科综合.files/image036.gif) (2分) ②
(2分) ②理科综合.files/image362.gif) (2分 )
(2分 )
(4)①理科综合.files/image364.gif) (1分);>(1分)
(1分);>(1分)
②理科综合.files/image366.gif) (2分);
(2分);
理科综合.files/image368.gif) (3分)
(3分)
28、(1)平衡气压,使分液漏斗中液体能顺利加入大试管内(2分)
(2)理科综合.files/image370.gif) (2分)
(2分)
(3)溶液变蓝(2分) 理科综合.files/image372.gif) (3分);
(3分);
理科综合.files/image374.gif) (3分)
(3分)
(4)理科综合.files/image376.gif) (2分)
(2分)
(5)理科综合.files/image378.gif) 与水反应放热,使生成的
与水反应放热,使生成的理科综合.files/image380.gif) 分解产生
分解产生理科综合.files/image085.gif) (2分)
(2分)
理科综合.files/image191.gif)
30、(每空2分)
(1)淀粉; 作为能源物质; 合成代谢产物
(2)酶活性; 酶合成; 既保证了代谢的需要,又避免了物质和能量的浪费; 初
(3)经诱变处理培育出不能合成乙酶的真菌
(4)①天然
②鲜牛奶应煮沸冷却后使用;再设置一对照实验,把新鲜花园土换成高温加热过的花园土
31、I、(每空3分)
(1)左 ; 右
(2)均为右
Ⅱ、(每空2分)
(1)接种相应的病原体;全部感病 (或高茎感病);抗病和感病(或高茎抗病和高茎感病)
(2)高茎抗病,矮茎感病
理科综合.files/image383.gif) (3)如下图
(3)如下图
(1)化学式为Pt(NH3)2Cl2的化合物有两种异构体,其中一种异构体易溶于水,则此种化合物是________(填“极性”、“非极性”)分子.
(2)今有A、B、C、D四种元素,它们的原子序数依次增大,且均小于18,A和B在同一周期,A原子p能级有一个空轨道,B原子的p能级有两个未成对电子,0.1 mol C单质能从酸中置换出2.24 L氢气(标准状态),此时它就变成与B离子电子层排布完全相同的离子.D离子的半径在B、C、D中为最小.则:
①A是________,B是________,C是________,D是________.(填名称)
②A单质和B单质充分反应生成的化合物的电子式是________.
③我国科学工作者于20世纪90年代在兰州制备出过去一直依赖进口,价格十分昂贵的B的一种同位素形成的单质,1 mol这种单质中含中子的物质的量是20 mol,则这种同位素原子的符号为________.
(3)NH3·H2O的电离方程式为NH3·H2O![]() NH4++OH-,试判断溶于水后,形成的合理结构是________.(填下图中的字母)
NH4++OH-,试判断溶于水后,形成的合理结构是________.(填下图中的字母)

(4)把CoCl2溶于水后加氨水直到先生成的Co(OH)2沉淀又溶解后,再加氨水,使生成[Co(NH3)6]2+,此时向溶液中通入空气,得到的产物中有一种其组成可用CoCl3·5NH3表示,Co的配位数是6.把分离出的CoCl3·5NH3溶于水后立即加硝酸银溶液,则析出AgCl沉淀.经测定,每1 mol CoCl3·5NH3只生成2 mol AgCl.CoCl3·5NH3中Co化合价为________,请写出表示此配合物结构的化学式:________.
(5)核内中子数为N的R2+,质量数为A,则ng它的氧化物中所含质子的物质的量是________.
(6)Mg晶体的熔点比Na晶体________(填“高”或“低”),原因是________.
化学学科中的化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理。
请回答下列问题: (1)工业上采取CO和H2为原料合成乙醇,其化学反应方程式为:2CO(g)+4H2(g)??
(1)工业上采取CO和H2为原料合成乙醇,其化学反应方程式为:2CO(g)+4H2(g)??
CH3CH2OH(g)+H2O(g)。请写出该反应的化学平衡常数表达式K=________。
(2)常温下,浓度均为0.1 mol·L-1的六种溶液的pH如下表:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | Na2SO4 |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 7.0 |
①上述盐溶液中的阴离子,结合质子能力最强的是________。
②根据表中数据,浓度均为0.01 mol·L-1的下列五种物质的溶液中,酸性最强的是________(填字母);将各溶液分别稀释100倍,pH变化最小的是________(填字母)。
A.HCN B.HClO C.H2SO4 D.CH3COOH E.H2CO3
③把CO2气体通入饱和碳酸钠溶液中,可以观察到的现象为________,原因为________(用离子方程式表示)。
④要增大氯水中HClO的浓度,可向氯水中加入少量的碳酸钠溶液,反应的离子方程式为____________。
(3)某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是_______。

A.加入适量BaCl2(固体)可以使溶液由d点变到c点
B.通过加水稀释可以使溶液由b点变到a点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp等于c点对应的Ksp 查看习题详情和答案>>
化学学科中的化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理。
请回答下列问题:
 (1)工业上采取CO和H2为原料合成乙醇,其化学反应方程式为:2CO(g)+4H2(g)??
(1)工业上采取CO和H2为原料合成乙醇,其化学反应方程式为:2CO(g)+4H2(g)??
CH3CH2OH(g)+H2O(g)。请写出该反应的化学平衡常数表达式K=________。
(2)常温下,浓度均为0.1 mol·L-1的六种溶液的pH如下表:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | Na2SO4 |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 7.0 |
①上述盐溶液中的阴离子,结合质子能力最强的是________。
②根据表中数据,浓度均为0.01 mol·L-1的下列五种物质的溶液中,酸性最强的是________(填字母);将各溶液分别稀释100倍,pH变化最小的是________(填字母)。
A.HCN B.HClO C.H2SO4 D.CH3COOH E.H2CO3
③把CO2气体通入饱和碳酸钠溶液中,可以观察到的现象为________,原因为________(用离子方程式表示)。
④要增大氯水中HClO的浓度,可向氯水中加入少量的碳酸钠溶液,反应的离子方程式为____________。
(3)某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是_______。

A.加入适量BaCl2(固体)可以使溶液由d点变到c点
B.通过加水稀释可以使溶液由b点变到a点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp等于c点对应的Ksp
查看习题详情和答案>>
请回答下列问题:
 (1)工业上采取CO和H2为原料合成乙醇,其化学反应方程式为:2CO(g)+4H2(g)??
(1)工业上采取CO和H2为原料合成乙醇,其化学反应方程式为:2CO(g)+4H2(g)??CH3CH2OH(g)+H2O(g)。请写出该反应的化学平衡常数表达式K=________。
(2)常温下,浓度均为0.1 mol·L-1的六种溶液的pH如下表:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | Na2SO4 |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 7.0 |
①上述盐溶液中的阴离子,结合质子能力最强的是________。
②根据表中数据,浓度均为0.01 mol·L-1的下列五种物质的溶液中,酸性最强的是________(填字母);将各溶液分别稀释100倍,pH变化最小的是________(填字母)。
A.HCN B.HClO C.H2SO4 D.CH3COOH E.H2CO3
③把CO2气体通入饱和碳酸钠溶液中,可以观察到的现象为________,原因为________(用离子方程式表示)。
④要增大氯水中HClO的浓度,可向氯水中加入少量的碳酸钠溶液,反应的离子方程式为____________。
(3)某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是_______。

A.加入适量BaCl2(固体)可以使溶液由d点变到c点
B.通过加水稀释可以使溶液由b点变到a点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp等于c点对应的Ksp
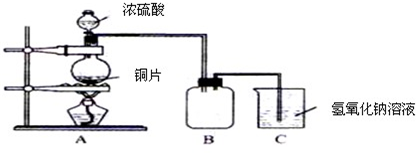
(1)B是用来收集实验中产生的气体的装置,但未将导管画全,请在图上把导管补充完整.
(2)实验中他们取6.4g 铜片和12mL 18mol?L-1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余.
①写出铜跟浓硫酸反应的化学方程式:
| ||
| ||
②为什么有一定量的余酸但未能使铜片完全溶解,你认为原因是
③下列药品中能够用来证明反应结束后的烧瓶中确有余酸的是:
A.铁粉 B.氯化钡溶液 C.银粉 D.碳酸氢钠溶液
(3)为定量测定余酸的物质的量浓度,甲学生进行了如下设计学生设计的方案是:在反应后的溶液中加蒸馏水稀释至1000mL,取20mL与锥形瓶中,滴入2~3滴甲基橙指示剂,用标准氢氧化钠溶液进行滴定(已知氢氧化铜开始沉淀的pH约为5),通过测出消耗氢氧化钠溶液的体积来求余酸的物质的量浓度.假定反应前后烧瓶中溶液的体积不变,你认为他设计的实验方案能否求得余酸的物质的量浓度
(4)现已确认,SO2和NOx的排放是造成酸沉降的两大罪魁祸首.汽车排放的尾气中含有未燃烧充分的CH、以及N2、CO2、NO、CO等.有人设计利用反应2NO+2CO
 N2+2CO2 将有害的污染物转化为可参与大气循环的N2和CO2.
N2+2CO2 将有害的污染物转化为可参与大气循环的N2和CO2.在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
| 时间/h | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol?L-1 | 1.00×10-3 | 4.5×10-4 | 2.5×10-4 | 1.5×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol?L-1 | 3.6×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |