网址:http://m.1010jiajiao.com/timu_id_144017[举报]
9.C 10.B 11.A 12.A 13.D 14.D 15.C
28 (13分)
(1) HNO3 NH3 .files/image024.gif) H2O NH4NO3 (3分)
H2O NH4NO3 (3分)
(2)2Al+2OH- +6H2O=====2[Al(OH)4]- +3H2 Ó 或2Al+2OH- +2H2O====2AlO2- +3H2Ó(2分);
(3)I.<(2分) II K1/K2;66.67%(4分)
(4)N2+8H+ +6e- =======2NH4+(2分)
29.(15分)
(1)①NaNO2(2分);0.8(2分 ) ②b、c(2分 )
(2)①Fe3+>Cu2++>Fe2+(2分)
②方案:将铜棒与碳棒用导线连接,再插入氯化铁溶液,发现有电流产生(3分)
(3)①Cu2+、Fe2+(2分)
②1.0.files/image026.gif) 10-17(mol
10-17(mol.files/image024.gif) L-1)3(2分)
L-1)3(2分)
30(14分)
(1) C(2分)
(2) 避免 Na2SO3==== Na2S+ 2 Na2SO4(2分)
(3)
4 Na2SO3.files/image029.gif) 3
Na2SO4(2分)
3
Na2SO4(2分)
(4)
实验③的溶液中可能有Na2S,相同条件下,S2-水解程度大于SO2-3,的溶液的碱性强,pH增大(2分);S2-+H2O.files/image009.gif) HS-+HO-(2分)
HS-+HO-(2分)
(5)
取 ③溶液适量于试管中,向其中加稀H2SO4,如有腐蛋气味气体生成,则证明有S2-(或向其中加新制氯水,如有浑浊出现,则证明有S2-)(2分),另取③中溶液适量于试管中,加入HCL酸化的BaCL2溶液,如有白色沉淀 证明SO2-4.files/image031.gif) 38(8分)
38(8分)
31.(8分)
(1) 苯环,醛基(1分);
(2) D(1分)
(3)
.files/image032.gif)
(4)4分(2分)
PCl5(气)
 PCl3(气)+Cl2(气);△H>0 K=1 ①
PCl3(气)+Cl2(气);△H>0 K=1 ①CO(气)+Cl2(气)
 COCl2(气);△H<0 K=5×104 ②
COCl2(气);△H<0 K=5×104 ②COCl2(气)
 CO(气)+Cl2(气);△H>0③
CO(气)+Cl2(气);△H>0③(1)反应②和反应③的K值表达式
(2)降低Cl2浓度,反应③的K值
(3)要使反应①和反应②的K值相等,应采取的措施是
(a)反应①、反应②同时升高温度
(b)反应①、反应②同时降低温度
(c)反应①降低温度,反应②维持210℃
(Ⅱ)(10分)现将水蒸汽和CO气体分别通入到体积为1L的恒容密闭容器中进行反应.H2O(g)+CO(g)
 CO2(g)+H2(g);△H.得到以下三组数据,据此回答下列问题:
CO2(g)+H2(g);△H.得到以下三组数据,据此回答下列问题:| 实验组 | 温度 | 起始量 | 平衡量 | 达到平衡所需时间 | ||
| H2O | CO | H2 | CO2 | |||
| 1 | 650℃ | 1mol | 2mol | 0.8mol | 0.8mol | 5min |
| 2 | 900℃ | 0.5mol | 1mol | 0.2mol | 0.2mol | 3min |
| 3 | 900℃ | a mol | b mol | c mol | d mol | t |
(2)比较该反应实验1和实验2中CO的转化率:a1
(3)若实验3要达到与实验2等效的平衡状态,且t<3min,则a、b应满足的关系是
(4)900℃时,若要重新达到平衡,使c(CO2)/c(CO)比值变小,在其他条件不变时,可采取的措施有(填字母)
A.使用高效催化剂 B.增大H2浓度 C.升高温度 D.缩小容器体积.
PCl5(气)
CO(气)+Cl2(气)
COCl2(气)
(1)反应②和反应③的K值表达式______;(填“相同”或“不同”)
(2)降低Cl2浓度,反应③的K值______;(填“增大”、“减少”或“不变”)
(3)要使反应①和反应②的K值相等,应采取的措施是______
(a)反应①、反应②同时升高温度
(b)反应①、反应②同时降低温度
(c)反应①降低温度,反应②维持210℃
(Ⅱ)(10分)现将水蒸汽和CO气体分别通入到体积为1L的恒容密闭容器中进行反应.H2O(g)+CO(g)
 CO2(g)+H2(g);△H.得到以下三组数据,据此回答下列问题:
CO2(g)+H2(g);△H.得到以下三组数据,据此回答下列问题:| 实验组 | 温度 | 起始量 | 平衡量 | 达到平衡所需时间 | ||
| H2O | CO | H2 | CO2 | |||
| 1 | 650℃ | 1mol | 2mol | 0.8mol | 0.8mol | 5min |
| 2 | 900℃ | 0.5mol | 1mol | 0.2mol | 0.2mol | 3min |
| 3 | 900℃ | a mol | b mol | c mol | d mol | t |
(2)比较该反应实验1和实验2中CO的转化率:a1______ a2;该反应的反应热△H______0;(两空填“>”、“=”或“<”)
(3)若实验3要达到与实验2等效的平衡状态,且t<3min,则a、b应满足的关系是______,实验3条件时反应的平衡常数为______;
(4)900℃时,若要重新达到平衡,使c(CO2)/c(CO)比值变小,在其他条件不变时,可采取的措施有(填字母)______.
A.使用高效催化剂 B.增大H2浓度 C.升高温度 D.缩小容器体积.
查看习题详情和答案>>
(1)以N2和H2为原料合成氨气.反应N2(g)+3H2(g)?2NH3(g)△H<0
①下列措施可以提高H2的转化率是(填选项序号)
a.选择适当的催化剂 b.增大压强 c.及时分离生成的NH3 d.升高温度
②一定温度下,在密闭容器中充入1molN2和3molH2发生反应.若容器容积恒定,达到平衡状态时,容器内的压强是原来的
| 15 | 16 |
若容器压强恒定,达到平衡状态时,N2的转化率为a2,则a2
(2)以氨气、空气为主要原料制硝酸.
①NH3被氧气催化氧化生成NO的反应的化学方程式是
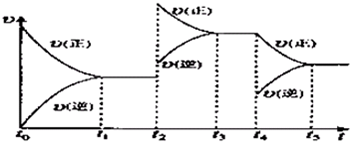
②在容积恒定的密闭容器中进行反应2NO(g)+O2(g)?2NO2(g)△H>0
该反应的反应速率(v)随时间(t)变化的关系如图所示.若t2、t4时刻只改变一个条件,下列说法正确的是(填选项序号)
a.在t1~t2时,可依据容器内气体的压强保持不变判断反应已达到平衡状态
b.在t2时,采取的措施一定是升高温度
c.在t3~t4时,可依据容器内气体的密度保持不变判断反应已达到平衡状态
d.在t0~t5时,容器内NO2的体积分数在t3时值的最大
③向容积相同、温度分别为T1和T2的两个密闭容器中分别充入等量NO2发生反应:
2NO2 (g)?N2O4(g)△H<0.恒温恒容下反应相同时间后,分别测定体系中NO2的百分含量分别为a1,a2.已知T1<T2,则a1
A.大于 B.小于 C.等于 D.以上都有可能
(3)硝酸厂常用如下2种方法处理尾气.
①催化还原法:催化剂存在时用H2将NO2还原为N2.
已知:2H2(g)+O2(g)=2H2O(g)△H=-483.5kJ/mol
N2(g)+2O2(g)=2NO2(g)△H=+133kJ/mol
则H2还原NO2生成水蒸气反应的热化学方程式是
②碱液吸收法:用Na2CO3溶液吸收NO2生成CO2.
若每9.2gNO2和Na2CO3溶液反应时转移电子数为0.1mol,则反应的离子方程式是
 2AB3(g)化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量)。据图可得出的判断正确的是
2AB3(g)化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量)。据图可得出的判断正确的是 