网址:http://m.1010jiajiao.com/timu_id_14205[举报]
一、选择题
题号
1
2
3
4
5
6
7
8
9
10
答案
C
D
A
B
A
B
D
B
D
B
二、选择题
题号
11
12
13
14
15
答案
D
C
BD
C
B
三、填空、简答和计算
16.(1)酒精或氢氧化钠溶液 (2)稀盐酸或稀硝酸 (3)浓盐酸
17.(1)生成淡黄色沉淀 (2)分层,下层橙红色 (3)生成白色沉淀
18. Cl2、Br2、I2、HClO; KCl、I2; KCl
19.(1)
MnO2+ 4HCN  Mn(CN)2+(CN)2↑+2H2O(2)(CN)2+2KOH==KCN+ KCNO+ H2O
Mn(CN)2+(CN)2↑+2H2O(2)(CN)2+2KOH==KCN+ KCNO+ H2O
20.(1)NH4I>NH4Br>NH4Cl>NH
21. HCl MnO2 Cl2 KBr KCl Br2 KI I2 AgBr
22.(1)2I-+Cl ====2Cl-+I
====2Cl-+I (2)BD;四氯化碳不溶于水、碘在其中有较好的溶解度、且四氯化碳易挥发;分层,下层为紫红色,上层近于无色。(3) 使漏斗内外空气相通,以保证漏斗里液体能流出;使漏斗下端管口紧靠烧杯内壁,及时关闭活塞,不要让上层液体流出;(4)蒸馏
(2)BD;四氯化碳不溶于水、碘在其中有较好的溶解度、且四氯化碳易挥发;分层,下层为紫红色,上层近于无色。(3) 使漏斗内外空气相通,以保证漏斗里液体能流出;使漏斗下端管口紧靠烧杯内壁,及时关闭活塞,不要让上层液体流出;(4)蒸馏
23.设参加反应的Cl2的质量为x,
2NaI+Cl2==2NaCl+I
300 71 117 300-117
x
 x=
x=
答:有
24.解:Cl2+2KBr=2KCl+Br2 ∵K+:Cl-=2:1
∴KBr过量有剩余且生成的KCl物质的量等于KBr剩余的物质的量。
又∵Br元素
则:KBr剩余0.125mol,生成KCl0.125mol
(1)V(Cl)2 = (2)
(2)
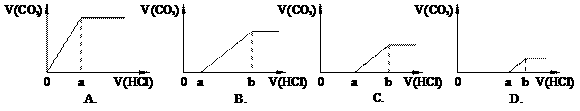
向等量的NaOH溶液中分别通入CO2气体。因CO2的通入量不同,得到组分不同的溶液M。若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)关系如下,(注:①假设CO2全部逸出;②C图中oa=ab)。其中M中只有1种溶质的是

查看习题详情和答案>>
现有A、B、C、D、E、F六种中学常见的元素,其原子序数依次增大。①D的一种含氧酸根离子与H+结合生成D的单质、D的氧化物和水;该D的氧化物通入品红溶液,溶液褪色,加热溶液又变红色;②在短周期元素中,只有C的氧化物和烧碱反应生成的溶液与过量盐酸混合产生白色沉淀;③A与D的原子最外层电子数相同;④B的单质既能与盐酸反应,又能与氢氧化钠溶液反应;⑤E有多种含氧酸,其氧化性与“同元素价态越高,其氧化性越强”一般规律相悖,它是生活调味品和农药的组成元素 ⑥E单质+F单质![]() 红棕色烟,D单质+F单质
红棕色烟,D单质+F单质![]() 黑色固体,A单质+F单质
黑色固体,A单质+F单质![]() 黑色固体。F的最高价钾盐是一种绿色环保型净水剂。
黑色固体。F的最高价钾盐是一种绿色环保型净水剂。
根据上述信息,回答下列问题:
(1)A的简单离子结构示意图为 ;具有强氧化性的E的含氧酸结构式为 ;
(2)向一定量的烧碱溶液中缓慢通入DA2,得到中性溶液,其溶质的化学式为 ;
(3)下列“根据”能证明B、F单质活泼性强弱的是 ;
a.根据它们分别与D单质反应产物的价态
b.根据它们最高价氧化物的水化物在氢氧化钠溶液中溶解情况
c.根据它们分别与盐酸反应产生气泡快慢
d.根据它们在空气中稳定性
(4)工业上冶炼C单质的化学方程式为 。
(5)CE4在湿空气中产生大量白雾,可以用于海战。写出发生的化学方程式: 。
(6)C、D、E最高价氧化物对应的水化物酸性强弱顺序为(用化学式表示): 。
查看习题详情和答案>>下列反应对自然界中碳酸钙的搬运、喀斯特地貌的形成具有重要意义:CaCO3+H2O+CO2=Ca2+ +2HCO3-。富含二氧化碳的地下水流经大理石岩层时,通过该反应腐蚀岩层,久而久之,就形成了溶洞,溶洞还可能塌垮而形成天坑。地下河把Ca2+和HCO3-带到其他地方,渗出、滴下的水蒸发后,碳酸氢钙[Ca(HCO3)2]分解Ca(HCO3)2=CaCO3↓+H2O+CO2↑,产生的碳酸钙不断累积,就形成了钟乳石、石笋、石柱等自然景观。
(1)写出Na2CO3溶液中通入二氧化碳时反应的离子方程式:_______________ 据此,为什么除去二氧化碳气体中混有的少量氯化氢等酸性气体时,用饱和NaHCO3溶液而不用Na2CO3溶液_____________
(2)用NaOH溶液吸收二氧化碳气体,每摩尔氢氧化钠最多可吸收标准状况下__________升CO2。
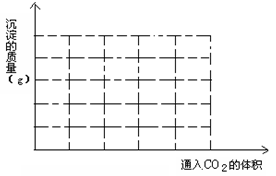
(3)向一定量的氢氧化钙溶液中慢慢通入二氧化碳气体,请在图中画出反应体系中沉淀的质量与通入二氧化碳体积之间的关系图