网址:http://m.1010jiajiao.com/timu_id_135504[举报]
| ||
(1)化学小组所制得的气体中混有的主要杂质气体可能是
(2)为证实相关分析,化学小组的同学设计了如下实验,对退回气体(X)取样进行认真探究(遇有气体吸收过程,视为全吸收).

①组装好仪器后,盛放药品前,必要的一个操作是
②A中加入的试剂可能是:
③可证实气体X中混有较多量某杂质气体的实验现象是
(3)对上述装置略加改进,可粗略测定X气体中SO2的体积分数.改进时可选用的下列仪器为
A 导管 B 水槽 C 广口瓶 D 容量瓶 E 量筒 F 单孔塞 G 双孔塞.

试回答下列问题:
(1)将铜粉分散在石棉绒中的原因是
(2)在铜和浓硝酸反应前,挤压打气球,经A、B、C反应后,进入D中的气体主要成分是
(3)关闭K1、K2,打开K3,由分液漏斗向D中滴加浓硝酸.待Cu和浓硝酸反应结束后,再通过分液漏斗向D中加入CCl4至满.则D中一定发生反应的离子方程式为:
(4)若E中出现倒吸,可采取的应急操作是
(5)I.从E装置所得溶液中取出25.00mL,加两滴酚酞,用0.1000mol?L-1的NaOH溶液滴定,当滴定完成后消耗NaOH溶液18.00mL,则E容器中所得硝酸的物质的量浓度为
Ⅱ.若实验测得F装置所收集到的气体体积为139.00mL,则铜和一定量的浓硝酸反应
某化学兴趣小组欲验证:“铜和一定量的浓硝酸反应有一氧化氮产生”.设计使用了如下装置进行实验.(假设气体体积均为标准状况,导气管中气体体积忽略不计,且忽略反应中的溶液体积变化)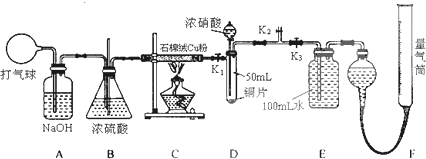
试回答下列问题:
(1)将铜粉分散在石棉绒中的原因是______.
(2)在铜和浓硝酸反应前,挤压打气球,经A、B、C反应后,进入D中的气体主要成分是______(填化学式),通入该气体的目的是______;进行此步操作时应关闭______,打开______ (填K1、K2或K3).
(3)关闭K1、K2,打开K3,由分液漏斗向D中滴加浓硝酸.待Cu和浓硝酸反应结束后,再通过分液漏斗向D中加入CCl4至满.则D中一定发生反应的离子方程式为:______.
(4)若E中出现倒吸,可采取的应急操作是______.
(5)I.从E装置所得溶液中取出25.00mL,加两滴酚酞,用0.1000mol?L-1的NaOH溶液滴定,当滴定完成后消耗NaOH溶液18.00mL,则E容器中所得硝酸的物质的量浓度为______ mol?L-1.
Ⅱ.若实验测得F装置所收集到的气体体积为139.00mL,则铜和一定量的浓硝酸反应______(填“有”或“无”)NO生成,其依据是(请用数据和文字说明)______.
查看习题详情和答案>>
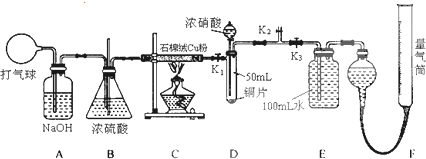
试回答下列问题:
(1)将铜粉分散在石棉绒中的原因是______.
(2)在铜和浓硝酸反应前,挤压打气球,经A、B、C反应后,进入D中的气体主要成分是______(填化学式),通入该气体的目的是______;进行此步操作时应关闭______,打开______ (填K1、K2或K3).
(3)关闭K1、K2,打开K3,由分液漏斗向D中滴加浓硝酸.待Cu和浓硝酸反应结束后,再通过分液漏斗向D中加入CCl4至满.则D中一定发生反应的离子方程式为:______.
(4)若E中出现倒吸,可采取的应急操作是______.
(5)I.从E装置所得溶液中取出25.00mL,加两滴酚酞,用0.1000mol?L-1的NaOH溶液滴定,当滴定完成后消耗NaOH溶液18.00mL,则E容器中所得硝酸的物质的量浓度为______ mol?L-1.
Ⅱ.若实验测得F装置所收集到的气体体积为139.00mL,则铜和一定量的浓硝酸反应______(填“有”或“无”)NO生成,其依据是(请用数据和文字说明)______.
某化学兴趣小组欲验证:“铜和一定量的浓硝酸反应有一氧化氮产生”。设计使用了如下装置进行实验。(假设气体体积均为标准状况,导气管中气体体积忽略不计,且忽略反应中的溶液体积变化)

试回答下列问题:
(1)将铜粉分散在石棉绒中的原因是___________________________________。
(2)在铜和浓硝酸反应前,挤压打气球,经A、B、C反应后,进入D中的气体主要成分是_________(填化学式),通入该气体的目的是_________________________________;进行此步操作时应关闭_________,打开_________ (填K1、K2或K3)。
(3)关闭K1、K2,打开K3,由分液漏斗向D中滴加浓硝酸。待Cu和浓硝酸反应结束后,再通过分液漏斗向D中加入CCl4至满。则D中一定发生反应的离子方程式为:_______________________________________________________________________。
(4)若E中出现倒吸,可采取的应急操作是_________________________________。
(5)Ⅰ.从E装置所得溶液中取出25.00mL,加两滴酚酞,用0.1000 mol·L-1的NaOH溶液滴定,当滴定完成后消耗NaOH溶液18.00mL,则E容器中所得硝酸的物质的量浓度为__________________ mol·L-1。
Ⅱ.若实验测得F装置所收集到的气体体积为139.00 mL,则铜和一定量的浓硝酸反应___________(填“有”或“无”)NO生成,其依据是(请用数据和文字说明)__________________________________________________________________________________________________________________________________________________________________________________________________________________________。
查看习题详情和答案>>